В данной статье описано исследование экспериментального парамагнитного контрастного соединения GDOF-Mn-DTPA. В исследовании проводится оценка основных свойств препарат при взаимодействии с тканью печени и в водном растворе.
Ключевые слова: магнитно-резонансная томография, контрастные соединения, релаксивность.
Актуальность
МРТ как метод диагностики введенный в клиническое использование в 1972 году поднял уровень медицины на качественно новый уровень.
Однако, данный метод нуждался в доработке. Уже в 1978 году была исследована возможность использования контрастных препаратов в МРТ. На основе работ Блоха (1944) с парамагнитным ускорением релаксации воды, математического описания процесса релаксации протонов при добавлении парамагнетика, произведенного Соломоном (1955) и доработанного Блюмбергеном (1957), получилось изменить сигнал магнитного резонанса протонов миокардиоцитов собаки с помощью внутривенного введения соли марганца. Данный эксперимент был осуществлен создателем МРТ Полом Лаутербуром [7].
При дальнейших исследованиях различных соединений на животных было выявлено влияние на релаксацию протонов со стороны хелатных комплексов металлов (исследования проводились компанией Siemens) [7]. Лучшими показателями обладало соединение гадолиния и пентетовой 7кислоты (диэтилентриаминпентауксусной кислоты) — Gd-DTPA [7]. В последствие данный комплекс, прошедший лабораторные и клинические испытания, был представлен в качестве лекарственной формы с названием Магневист® (Шеринг АГ, Германия). Магневист® — первый представитель современного класса контрастно-диагностических средств.
Дальнейшие исследования в области контрастирования позволили создать и изучить больший спектр контрастных средств для МРТ.
Современные контрастные соединения в большинстве своем являются хелатными комплексами иона гадолиния. Многочисленные лабораторные и клинические исследования показали, что гадолиний в комплексе не наносит вред здоровью пациента [7].
Однако, было доказано, что свободный ион гадолиния, не имея естественного связывающего агента в организме человека, может активировать пролиферацию фиброцитов и вызывать повышенный синтез коллагена, а также активировать иммунный ответ путем фагоцитоза макрофагами тканей и дальнейшей презентацией с выработкой специфических цитокинов (рис. 1) [2, 3, 7]. Оба эти пути способствуют фиброзу различных органов, в частности, нефрофиброзу [2, 3, 7].
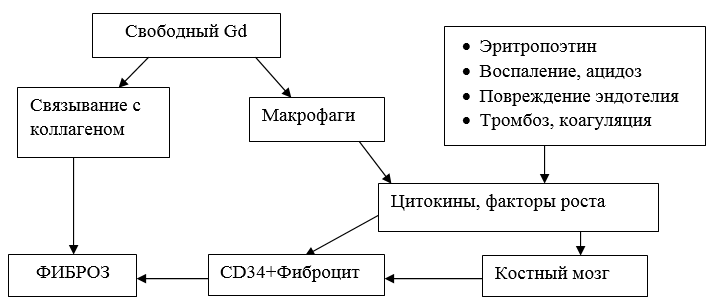
Рис. 1. Токсическое действие свободного иона гадолиния
При изучении различных соединений было доказано, что такой микроэлемент как марганец имеет близкие парамагнитные свойства с гадолинием и при этом является одним из микроэлементов, содержимся в тканях организма и имеющим свой естественный метаболизм [3]. Марганец участвует в синтезе и обмене нейромедиаторов в нервной системе, обеспечивает стабильность клеточных мембран, обеспечивает развитие соединительной ткани, хрящей и костей и ряд других функций присущи данному микроэлементу [6].
Исследования комплексов двухвалентного иона марганца с хелатирующими соединениями показали, что Mn-DTPA, более устойчивый химически, имеет близкие значения релаксивности с Gd-DTPA, а, следовательно, схожими парамагнитными и контрастирующими свойствами [2, 3, 5, 8, 9]. При проведении клинических испытаний были получены результаты того, что для комплексов марганца единственным побочным эффектом является субъективное ощущение тепла в теле при введении контрастного соединения [1, 2, 3, 5]. Способность к визуализации патологических образований (опухолей головного мозга), на основе сравнения контрастирования анатомических и патологических структур, соответствовала комплексам гадолиния [2, 3, 5].
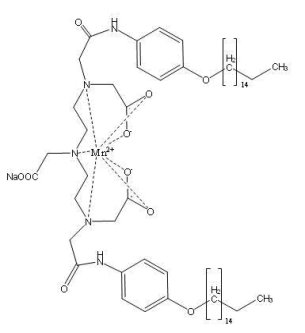
Рис. 2. Контрастное соединение GDOF-Mn-DTPA
На основе данных исследованиях были синтезирован препарат с марганцем — Пентаманг® [5]. Данный препарат относится к Т1 внеклеточным препаратам, основное применение которого — диагностика патологий головного мозга [5].
Описываемое в данной статье иследование исследование проводилась с маргенец-содержащим соединением GDOF-Mn-DTPA (рис. 2), полученное на кафедре биотехнологии и органического синтеза Томского Политехнического Университета.
В ранее проведенных исследованиях была доказана высокая гепатотропоность данного контрастного соединения, что позволяет использовать данный препарат как специфичное контрастное средство для исследований печени [4].
Однако, в основу данных выводов легли результаты качественных исследований изменения интенсивности сигнала после введения препарата крысам.
Дальнейшее исследование лежит в области количественного исследования взаимодействия препарата с тканью печени и изменения его свойств, и использование полученных данных в следующих исследованиях.
Цель и задачи исследования
Была поставлена цель оценить свойства соединения GDOF-Mn-DTPA и их изменения при контакте с печенью.
Основной задачей было определение релаксивности, как основного параметра, прямо определяющего контрастный эффект, препарата GDOF-Mn-DTPA в фантомах печени крыс.
Дополнительной задачей было оценить возможность использования полученного значения релаксивности как калибровочного значения при расчете концентрации препарата.
Материал и методы
В эксперименте использовался коллоидный раствор контрастного- препарата GDOF-Mn-DTPA в концентрации 50 ммоль/мл и значением рН = 8–9.
Исследование выполнялось на крысах Wistar с средней массой тела 270–310 г. Масса печени, взятой у крыс, составила в среднем 14,4 грамма.
С цель исключения влияния на препарат белков крови и распределения препарата в других тканях были использованы фантомы печени крыс, приготовленные по следующей методике: двойная гомгенизация с последовательным добавлением 5 мл и 4 мл 0.9 % раствора NaCl. Было приготовлено 7 проб гомогената с концентрацией контрастного препарата от 0 до 1.0 ммоль/мл.
Так же было проведено исследование препарата в водном растворе в такой же концентрации в качестве контроля.
Опыт проводился на базе высокопольного МРТ Toshiba Excellart с индукцией магнитного поля 1.5 Тл.
Подготовленные фантомы печени крыс и водных растворов контрастного соединения GDOF-Mn-DTPA помещались на штативе в камеру МРТ в квадратурной катушке для исследования коленного сустава.
Использовалась импульсная последовательность TurboSE с инверсией-восстановлением. Инвертирующий импульс подавался в диапазоне от 20 до 4000 мс.
На основе полученных значений интенсивности с помощью нелинейного приближения определяли время Т1-релаксации, а затем обратное ему значение релаксивности.
Для оценки корреляции полученных значений использовался ранговый коэффициент корреляции Спирмена вследствие того, что данный критерий нечувствителен к закону распределения выборки.
Результаты и обсуждение
В ходе исследования были получены следующие результаты (рис. 3) взаимосвязи параметра релаксивности от концентрации контрастного соединения в фантомах гомогенатов печени крыс и водных растворах.
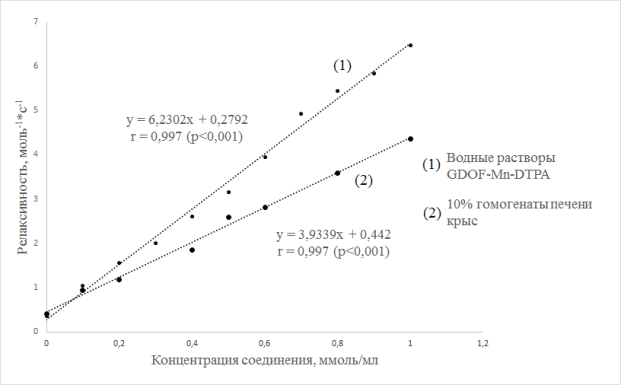
Рис. 3. Зависимость релаксивности от концентрации препаратов в фантомах
Между этими параметрами была найдена сильная статистически достоверная связь, описываемая линейной функцией.
Как хорошо видно на графике релаксивность водных растворов значительно выше, чем для гомогенатов печени крыс, что свидетельствует о изменении свойств препарата в гомогенатах. Возможно структура парамагнетика в гомогенате изменилась под влиянием внутриклеточных факторов ткани печени, что привело к снижению его концентрации, либо изменилось соотношение молекул воды на внутренней и внешней сфере молекулы соединения в пользу внешней сферы, что обязательно вызывает снижение общей релаксивности. Кроме того, количество внутриклеточных факторов ограниченно и должен быть эффект насыщения и нелинейная зависимость релаксивности от концентрации парамагнетика, чего в нашем случае не наблюдается.
Однако, значение общей релаксивности для фантомов гомогенатов печени, равное 3.93±0,125 ммоль-1*с-1, близко по значению к релаксивности гадолиний-содержащего препаратов, например, Магневист®, релаксивность которого 4,4 ммоль-1*с-1, что свидетельствует о сохранении контрастирующих свойств препарата в ткани.
При расчете концентрации препарата в фантомах печени и водных растворов с использованием обозначенных выше зависимостей релаксивности от концентрации были получены данные представленные на гистограмме (рис. 4).
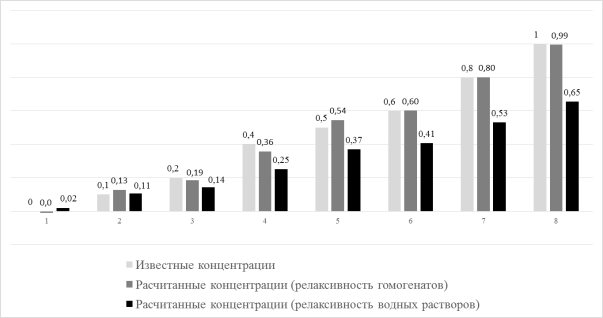
Рис. 4. Добавленные и рассчитанные концентрации соединения GDOF-Mn-DTPA в гомогенатах печени, ммоль/мл
Как видно на гистограмме расчеты на основе релаксивности фантомов гомогенатов печени, обозначенные темно-серым цветом, имеют значительно более близкие значения к исходным известным концентрациям препарата. Средняя относительная погрешность составила 6 %.
С другой стороны, использование значений релаксивности водных растворов, черный цвет на гистограмме, дает большую относительную погрешность — среднее значение 37 % и является менее точным способом расчета концентрации GDOF-Mn-DTPA.
Таким образом при определении концентрации следует использовать калибровочный график релаксивность-концентрация, полученный на основе исследования фантомов печени крыс.
Выводы
Таким образом доказано, что при взаимодействии с тканью печени экспериментальный контрастный препарат GDOF-Mn-DTPA изменяется либо вследствие воздействия факторов ткани, либо вследствие изменения собственной структуры, сохраняя при этом достаточные для контрастирования свойства.
Дальнейшее исследование препарата лежит в области оценки характера влияния тканей: изменяются ли свойства препарат в других тканях схожим образом, либо эффект зависит от исследуемой ткани.
Так же необходимо получение количественной характеристики биораспределения соединения, с использованием полученных калибровочных значений релаксивности, что позволит более точно определить класс данного препарата.
Литература:
1. Доклиническое токсикологическое изучение пентаманга и мангаскана [Текст] / А. А. Чурин, Г. В. Карпова, Т. И. Фомина и др. // Экспериментальная и клиническая фармакология. — 2008. — № 4. — С. 49–52.
2. Применение Mn-диэтилентриаминпентацетата (ДТПА) для парамагнитного контрастирования при магнитно-резонансной томографии — результаты доклинических исследований и сравнение с Gd-ДТПА [Текст] / В. Ю. Усов, М. Л. Белянин, О. Ю. Бородин и др. // Медицинская визуализация. — 2007. — № 4. — С. 134–142.
3. Разработка и доклиническое исследование парамагнитных контрастных препаратов на основе органических комплексов марганца (II) для магнитно-резонансной томографии [Текст] / В. Ю. Усов, М. Л. Белянин, М. Првулович и др. // Сибирский медицинский журнал. — 2007. — № 3. — С. 16–23.
4. Санников, М. Ю. Экспериментальное исследование контрастирующего эффекта нового Mn-содержащего высоколипофильного соединения при МРТ [Текст] / М. Ю. Санников, К. А. Кофанова, П. Е. Бушлатова // Медико-биологические науки: достижения и перспективы: сб. материалов I Всероссийской научной студенческой конференции. — Томск, 2011. — С. 90–91.
5. Синтез и оценка мангапентетата как парамагнитного контрастного препарата для МР-томографии [Текст] / М. Л. Белянин, М. Првулович, Г. В. Карпова и др. // Диагностическая интервенционная радиология. — 2008. — № 1. — С. 75–86.
6. Скальных, А. В. Химические элементы в физиологии и экологии человека [Текст] / А. В. Скальных. — Москва: Издательский дом «ОНИКС 21 век»: Мир, 2004. — 216 с.
7. Шимановский, Н. Л. Контрастные средства [Текст]: руководство по рациональному применению / Н. Л. Шимановский. — Москва: ГЭОТАР-Медиа, 2009. — 464 с.
8. Hamm, B. Contrast material for computed tomography and magnetic resonance imaging of the gastrointestinal tract / Hamm B., Wolf K. J. // Curr Opin Radiol. — 1991. — Vol. 3, N 3. — P. 474–482.
9. Hepatic uptake of the magnetic resonance imaging contrast agent Gd-EOB-DTPA, role of human organic anion transporters / M. Leonhardt, M. Keiser, S. Oswald et all // Drug Metab Dispos. — 2010. — Vol. 57, N 7 — P. 1024–1028.







