При травмах различных частей тела помимо различных тканей могут повреждаться нервные волокна вплоть до разрыва. В настоящее время разрабатываются различные методы восстановления проводимости поврежденных нервов, в основном связанные с хирургическим вмешательством. В данной статье будут представлены некоторые методики восстановления проведения импульса от высших нервных центров до органов-эффекторов.
Известен способ лечения дефекта периферического нерва путем невролиза, расщепления его проксимального конца на две равные части соответственно размеру дефекта, отсечения и перемещения одной из частей на место дефекта, наложения эпиневральных швов (см. рис.1).
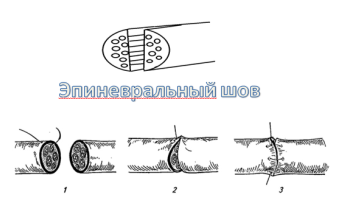
Рис. 1. Наложение эпиневрального шва
Недостатком известного способа является использование здорового участка нерва для замещения поврежденного участка, что не обеспечивает полного восстановления функции поврежденного нерва. Следует также отметить, что известным способом возможно восстановление относительно небольших участков поврежденного нерва.
Существует способ восстановления функции поврежденного нерва, включающий введение лекарственных средств в зону повреждения и электрическую стимуляцию нервного ствола (см. рис. 2).
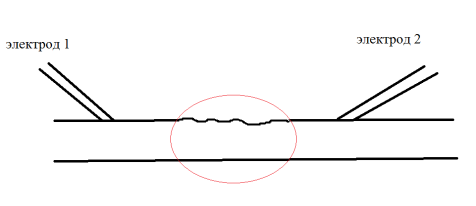
Рис. 2. Сочетание электростимуляций и применения лекарственных препаратов. Декомпрессия и электростимуляция
Однако указанный способ обладает рядом недостатков: известным способом возможно восстановление относительно небольших, до 8 см, дефектов нерва, электроды накладываются на нервный ствол, что не гарантирует постоянного и полного контакта с аксонами нерва, причем часто наблюдается миграция электродов, специальная конструкция электродов-нитей, выполненная из углеродистой нити по своим свойствам не апирогенна, параметры электрического тока недостаточны для восстановления больших, 20 см и более, дефектов нервов.
Способ лечения компрессионных поражений нервных стволов включающий хирургическую декомпрессию и электростимуляцию через имплантированные в зону поражения электроды с установленными пороговыми величинами амплитуды, длительности и частоты импульсов (см. рис. 3).
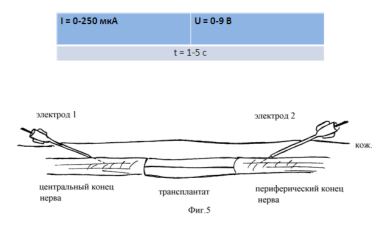
Рис. 3. Хирургическая декомпрессия и электростимуляция через имплантированные в зону поражения электродов
Недостатком известного способа является осуществление электростимуляции импульсным током (параметры тока: амплитуда от 1 до В; частота от 30 до 80 Гц; длительность от 0,5–0,75 мс), хирургическая декомпрессия исключает компенсацию больших анатомических дефектов нервов, что не позволяет восстановить периферическую проводимость.
Согласно последнему способу дефект периферического нерва замещается нервным аутотрансплантатом, взятым из n.suralis. Выше и ниже повреждения субэпиневрально внедряются электроды, изготовленные из серебряной проволоки диаметром 0,1 мм, в послеоперационном периоде (с первых суток) осуществляют электростимуляцию постоянным электрическим током, изменяющим свое направление. Длительность действия в различных направлениях изменяется от 1 до 5 секунд друг от друга. Величина силы тока изменяется от 0 до 250 мкА при изменении напряжения от 0 до 9 В. Данный способ позволяет восстановить болевую и тактильную чувствительность начиная с 3–5 суток послеоперационного периода, с последующим восстановлением всех видов чувствительности. Сущность этого метода заключается в следующем: во время оперативного вмешательства обнажают участок анатомического дефекта периферического нерва. После иссечения дистального и проксимального концов нерва в пределах «здоровых» тканей определяют истинный дефект нерва. Размер дефекта, необходимый для замещения, может быть более 20 см. Производится забор нейроаутотрансплантата (n.suralis) с голени, в три раза превышающей величину дефекта. Забранный трансплантат делят на три равные части, укладывают в виде «кабеля» и закрепляют швом нитью с использованием операционного микроскопа. Затем трансплантат укладывают в подготовленное ложе и подшивают к центральному и периферическому концам поврежденного нерва (см. рис. 4). Осуществляют гемостаз.
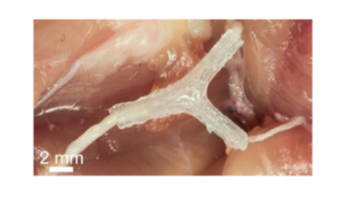
Рис. 4. 3D-печать
Вне кожной раны, к центральному и периферическому концам поврежденного нерва, имплантируют электроды субэпиневрально. Электроды выполнены из серебряной проволоки диаметром 0,1 мм. Электроды крепят к коже двумя шелковыми швами. Как вариант, в качестве электрода может использоваться серебряная игла для иглорефлексотерапии. Каждую рану зашивают. Конечность иммобилизуют; в послеоперационном периоде, начиная с первых суток, дважды в день до 30 минут проводят электростимуляцию нерва постоянным током, изменяющим свое направление. Длительность действия тока от 1 до 5 секунд. Величину силы тока изменяют от 0 до 250 мкА при изменении напряжения от 0 до 9 В, в зависимости от субъективных ощущений больного в виде покалывания в области трансплантата и дистальнее него, что обеспечивает восстановление болевой и тактильной чувствительности уже на 30-сутки после операции. Через 10–15 дней, в зависимости от скорости восстановления чувствительности, электроды извлекают без повторного оперативного вмешательства.
Предлагаемый способ лечения при экспериментально-клиническом излучении применяли у 12 больных с дефектами периферических нервов от 15 до 20 см. Во всех случаях лечение проводилось в отдаленные сроки после травмы (до 3 лет). У всех больных после проведенного лечения отмечалось восстановление функции нерва.
Существует еще одна интересная методика восстановления проведения нервного импульса. Она основана на сшивании дистантного конца поврежденного нерва с другим, здоровым, нервом. Для лучшего понимания данного процесса мы приведем пример: из-за травмы у пациента произошло нарушение целостности одного из нервов предплечья. При этом стал невозможным контроль первых двух пальцев руки. Благодаря применению новой методики, врачи смогли срастить отмерший нерв, который контролировал связку указательного и большого пальцев, с еще работающим нервом в предплечье. То есть врачи смогли обойти зону повреждения.
Также есть предположение, что нервные центры, при повреждении их проводящих путей, могут усиливать подаваемые импульсы и посредством иррадиации передавать их на другой нервный центр. Дистальный конец поврежденного нерва будет также сшиваться со здоровым нервом, проксимальный удаляется. Нервный центр, получивший новые, незнакомые ему импульсы, посылает и свои, и чужие по своим нервным волокнам, но дифференцирует их и, дойдя до места сшивания, нервные сигналы, идущие от другого нервного центра, будут уходить на дистальный участок поврежденного, а «свои» импульсы будут идти к эффектору по своим волокнам.
Литература:
- Пат. 2169016 Российская Федерация. Способ восстановления проводимости периферических нервов при больших анатомических дефектах / Е. А. Мокров, В.Н. Кустов, М. А. Щербаков; заявитель и патентообладатель: Научно-исследовательский институт физических измерений [Электронный ресурс] http://www.findpatent.ru/patent/216/2169016.html (дата доступа: 14.12.15).
- Повреждение периферических нервов [Электронный ресурс] /Детская пластическая реконструкция и хирургия.- режим доступа: http://www.hand-surgery.ru/index.php/arkhiv/stati/55-povrezhdenie-perifericheskikh-nervov.







