Бурые угли могут явиться ценным сырьем для получения целого ряда продукции нетопливного назначения, в том числе гуминовых кислот. Направления их использования определяются их составом и свойствами. Нами были получены гуминовые соединения из угля «Кумыс — Кудукского» месторождения разных концентраций. Полученные 0,51н гумат аммония, 1,74н гумат калия, 0,64н гумат натрия модифицируются аскорбиновой кислотой. Для исследования на вольтамперометрическом анализаторе ТА-2 в комплекте с ПК в работе использован метод катодной вольтамперометрии, в качестве модельной реакции рассматривался процесс ЭВ О2, который идентичен восстановлению кислорода в клетках и тканях организма. Для оценки влияния исследуемых веществ рассмотрена зависимость предельного тока от концентрации вещества. Наблюдалось проявление каталитической и антиоксидантной активности на вольтамперметрическом приборе.
После исследования антиоксидантной активности модифицированных аскорбиновой кислотой гуминовых соединений, нами были проведены опыты, которые направлены на исследование влияния модифицированных аскорбиновой кислотой гуминовых соединений на прорастаемость семян. Сущность исследования заключается в том, что проросшие семена помещают в чашки Петри на фильтровальную бумагу, смоченную вытяжкой модифицированных аскорбиновой кислотой гуматов в 10 повторений. Параллельно смотрят на второй вариант, где вытяжку из гуминовых соединений заменяют дистиллированной водой. Ежедневно фильтровальную бумагу смачивают гуматом, модифицированным витамином С, при комнатной температуре. Необходимо обеспечивать постоянную вентиляцию в чашках Петри, а затем по истечению 7 суток отделяют корешки и зеленую массу, проросших семян овеса.
Ключевые слова: гуминовые соединения, антиоксидантная активность, аскорбиновая кислота, витаминизирование, модифицирование.
Цель эксперимента — изучить модификации гуминовых соединений, а также выявить характерные особенности влияния продуктов модификации на рост семян.
В ходе исследования были решены следующие задачи:
Извлечены гуминовые соединения из окисленного бурого угля Кумыс — Кудукского месторождения;
Получены витаминизированные гуминовые соединения;
Исследовано влияние витаминизированных гуминовых соединений на рост семян;
Изучено влияние различных технологических параметров на химические процессы.
Гуминовые соединения, образующиеся в результате сложных биохимических процессов разложения флоры и фауны под воздействием различных микроорганизмов, влаги и кислорода, широко распространены в природе [1, с. 27].
Овощные культуры, как и другие садовые растения, очень чутко реагируют на применение гуминовых стимуляторов.
Лучше всего использовать стимуляторы совместно с удобрениями. Подобный подход позволяет в разы увеличить потребление минеральных удобрений растениями [2, с. 39]. Традиционный метод извлечения ГК из сырья с помощью щелочных растворов рассматривается, как процесс образования солей, имеющих большую степень ионизации в водных растворах, если сравнивать их с кислотами.
В подготовленной аналитической пробе бурого угля Кумыс — Кудукского месторождения, определены влажность по ГОСТ 27314–91 [3], зольность по ГОСТ 11022–95 [4] и общий выход гуминовых кислот по ГОСТ 9517–94 (ИСО 5073–85) [5].
Исследовано влияние следующих факторов на выход гуминовых соединений из окисленного бурого угля Кумыс — Кудукского месторождения:
температуры нагрева реакционной смеси, ºС (при 20; 50; 75; 100);
концентрации щелочного раствора пирофосфата натрия, г/л (при 11,2; 22,3; 44,6; 89,2).
типа реагента, при обработке остатка до экстракции на водяной бане (КОН, NH4OH и NaOH);
типа реагента, при экстракции на водяной бане (КОН, NH4OH и NaOH);
размера фракций пробы угля под сито, мм (0,25; 0,50; 1,00; 3,00; 5,00).
Для получения необходимых гуминовых соединений была взята методика «Определение выхода гуминовых кислот из бурого угля» по ГОСТу 9517–94 [5], сущность метода заключается в обработке аналитической пробы топлива щелочным раствором пирофосфата натрия, осаждение гуминовых кислот избытком минеральной кислоты и определении массы полученного осадка. Для анализа используют реактивы квалификации ч. д.а., дистиллированную воду или воду эквивалентной чистоты, 1 %-ный раствор гидроксид натрия, 1 %-ый раствор гидроксид калия, 4 %-ный раствор гидроксид аммония, пирофосфат натрия по ГОСТ 342 (Na4P2O7·10Н2О) [6], 5 %-ный раствор соляной кислоты по ГОСТ 3118–77 (по объему) [7].
Экстракцию гуминовых соединений проводят следующим образом: Определяют массу в пересчете на сухую беззольный вес. Навеску помещают в коническую колбу А, В, С вместимостью 250 см3, приливают 100 см3 раствора гидроксида натрия, калия и аммония, и нагревают на кипящей водяной бане в течение 2 ч. После охлаждения до комнатной температуры содержимое колбы А центрифугируют в течение 15 мин при 210 с-1. Раствор декантируют, собирая в коническую колбу A1, B1, C1 вместимостью 500 см3. Нерастворившийся остаток промывают соответсвенно двумя порциями 100 см3 1 %-ный раствор NaOH, 1 %-ный раствор KOH, 4 %-ный раствор NH4OH. Центрифугируют суспензию после каждого промывания, собирая промывной раствор в колбу A1, B1, C1.
Полученные гуминовые соединения количественно переносятся в коническую колбу, вместимостью 1000 дм3 и доводится до отметки дистиллированной водой, а затем определяется концентрация гуминовых соединений в полученных растворах.
Определения концентраций гумата аммония (№ 1), гумата калия (№ 2), гумата натрия (№ 3), приведены ниже:
|
(№ 1) |
(№ 2) |
(№ 3) |
|
1000 дм3 — х г 50 дм3–0,258 г,
х=5,16 г, см=5,16/10=0,51н |
1000 дм3 — х г 50 дм3–0,87 г,
х=17,4 г, ск=17,4/10=1,74н |
1000 дм3 — х г 50 дм3–0,320 г,
х=6,4 г, ск=6,4/10=0,64н |
Полученные 0,51н гумат аммония, 1,74н гумат калия, 0,64н гумат натрия модифицируются аскорбиновой кислотой таким образом: готовятся растворы 0,0001н, 0,001н, 0,01н концентрации гумата натрия, гумата калия и гумата аммония по 10 мл и в каждые из них для дальнейшей модификации аскорбиновой кислотой добавляются 0,001 г аскорбиновой кислоты и перемешиваются. Были получены такие аликвоты веществ как, 0,0001н модифицированной аскорбиновой кислотой гумат натрия, калия, аммония, 0,001н модифицированной аскорбиновой кислотой гумат натрия, калия, аммония и 0,01 модифицированной аскорбиновой кислотой гумат натрия, калия, аммония [8, с. 95].
В Сетевом центре коллективного использования ТПУ на элементном анализаторе CHNSFlash2000 был проведен количественный анализ модифицированных гуминовых соединения содержания водорода, углерода, азота и серы. Получены следующие результаты:
Таблица 1
Результаты количественного анализа модифицированных гуминовых соединений
|
№ п/п |
Наименование образца |
Cодержание элементов |
|||
|
N, % |
C, % |
H, % |
S, % |
||
|
1 |
Гумат кальция, модифицированный витамином С |
0.63 |
37.1 |
0.66 |
- |
|
2 |
Гумат кальция, модифицированный витамином В1 |
0.49 |
35.1 |
0.68 |
- |
Образцы 1 и 2 были модифицированы витамином С и витамином В1, а данные элементного анализа подтверждают содержание аскарбиновой кислоты и витамина В в содержании гуминовых соединений.
Исследования проведены на вольтамперометрическом анализаторе ТА-2 в комплекте с ПК. В работе использован метод катодной вольтамперометрии, в качестве модельной реакции рассматривался процесс ЭВ О2, который идентичен восстановлению кислорода в клетках и тканях организма. Для оценки влияния исследуемых веществ (гумат Na, гумат K, гумат NH3, модифицированные гуматы с макро-микро элементами и витаминным комплексом) рассмотрена зависимость предельного тока от концентрации вещества. Наблюдалось проявление каталитической и антиоксидантной активности на вольтамперметрическом приборе. Кинетические критерии установлены следующим образом: 3-х электродная ячейка, активация 120 с, -0,4, кинетическая энергия Е= 0.0 — -0,8 В, мощность W=30 мВ/с, перемешивание 10с, успокоение 20с, 0В фон 10 мл, фосфатный буфер рН 6.86, 2 электрода: вспомогательный ЭВЛ-1М3.1 (хлорсеребряный) ХСЭ и индикаторный РПЭ, объем аликвоты V=0.5 мл.
Зависимость высоты волны на вольтамперограмме от времени приведены в следующей таблице.
Таблица 2
Зависимость высоты волны на вольтамперограмме от времени
|
Зависимость высоты волны на вольтамперограмме от времени |
|||
|
T, мин |
J1, мкА |
J2, мкА |
J3, мкА |
|
0 |
24,151 |
23,824 |
25,298 |
|
3 |
24,135 |
23,920 |
25,457 |
|
6 |
24,182 |
23,934 |
25,419 |
|
9 |
24,602 |
24,006 |
25,547 |
Таблица 3
Критические значения Т для R1, R2, R3
|
T, мин |
R1 |
R2 |
R3 |
|
0 |
0,000 |
0,000 |
0,000 |
|
12 |
-0,019 |
-0,008 |
-0,010 |
В таблице 3 приведены критические значения Т для R1, R2, R3. Проведен теоретический анализ закономерностей процесса ЭВ О2, даны количественные критерии экстремальной проверки, определены константы скорости химических реакции взаимодействия с активными кислородными радикалами. Особенности добавления витамина аскорбиновой кислоты в гуминовые соединения неминуемо приводят к проявлениям антиоксидантной активности [9, с. 32].
Механизм действия наиболее распространённых антиоксидантов предполагает обрыв реакционных цепей: молекулы антиоксиданта взаимодействуют с активными радикалами с образованием малоактивных радикалов. Окисление замедляется также в присутствии веществ, разрушающих гидроперекиси. В этом случае падает скорость образования свободных радикалов. Даже в небольшом количестве (0,01–0,001 н) антиоксиданты уменьшают скорость окисления, поэтому в течение некоторого периода времени (период торможения, индукции) продукты окисления не обнаруживаются. В практике торможения окислительных процессов большое значение имеет явление синергизма — взаимного усиления эффективности антиоксидантов в смеси, либо в присутствии других веществ.
Пики гумата натрия и калия концентрации 0,01н на вольтамперметрическом приборе показаны на рисунке 2 и 3.
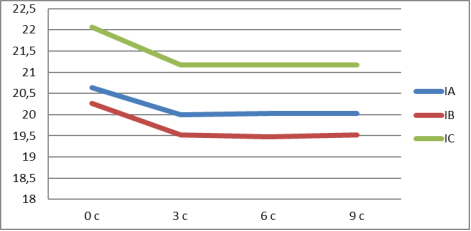
Рис. 1. Пик модифицированного 0,01 н гумата калия аскорбиновой кислотой
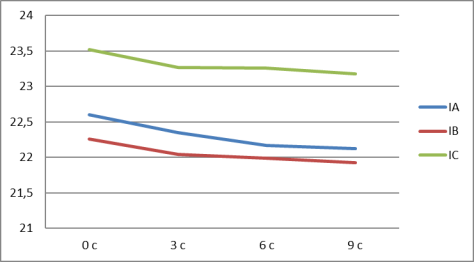
Рис. 2. Пик модифицированного 0,01 н гумата натрия аскорбиновой кислотой
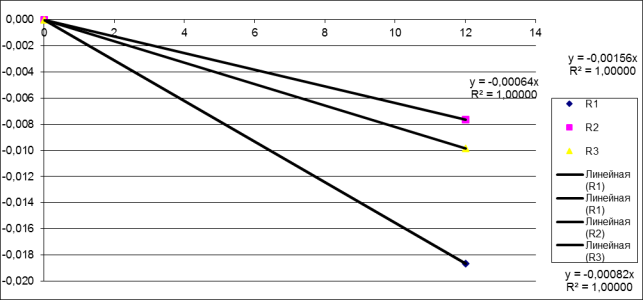
Рис. 3. Зависимость предельного тока от концентрации
Зависимость предельного тока от концентрации, приведенная выше, демонстрирует антиоксидантную активность, полученных гуминовых соединений.
После исследования антиоксидантной активности модифицированных аскорбиновой кислотой гуминовых соединений, нами были проведены опыты, которые направлены на исследование влияния модифицированных аскорбиновой кислотой гуминовых соединений на прорастаемость семян. Сущность исследования заключается в том, что проросшие семена помещают в чашки Петри на фильтровальную бумагу, смоченную вытяжкой модифицированных аскорбиновой кислотой гуматов в 10 повторений. Параллельно смотрят на второй вариант, где вытяжку из гуминовых соединений заменяют дистиллированной водой. Ежедневно фильтровальную бумагу смачивают гуматом, модифицированным витамином С, при комнатной температуре [10, с. 84]. Необходимо обеспечивать постоянную вентиляцию в чашках Петри, а затем по истечению 7 суток отделяют корешки и зеленую массу, проросших семян овеса. На рисунке 4 показан рост семян овса на контрольном варианте.

Рис. 4. Проклюнувшиеся семена на контрольном опыте

Рис. 5. Проклюнувшие семена на растворе аскорбиновой кислотой гумата натрия концентрации 0,01н.
На рисунке 5 показана прорастаемость семян, модифицированных аскорбиновой кислотой гумата натрия концентрации 0,01н.
Полученные данные о прорастаемости семян овса на растворе модифицированных аскорбиновой кислотой гумата натрия и гумата калия приведены в таблице 4.
Таблица 4
Прокленувшиеся семена на растворе гумата натрия концентрации 0,01н модифицированного аскорбиновой кислотой гумата натрия и гумата калия
|
№ образца |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
К+AK |
число |
5 |
0 |
5 |
6 |
2 |
8 |
5 |
5 |
6 |
4 |
4,6 4,6±1,1 |
|
% |
50 |
0 |
50 |
60 |
20 |
80 |
50 |
50 |
60 |
40 |
||
|
Na+AK |
число |
4 |
6 |
4 |
6 |
3 |
6 |
5 |
4 |
7 |
5 |
5 5±1 |
|
% |
40 |
60 |
40 |
60 |
30 |
60 |
50 |
40 |
70 |
50 |
||
После получения данных этого эксперимента можно сделать вывод о том, что наибольшую биологическую активность проявляет модифицированной аскорбиновой кислотой гумат натрия и гумат калия концентрации 0,01н.
На сегодняшний день в Республике Казахстан проводится множество экспериментов, направленных на изучение гуминовых соединений в кормах для животных, но данная исследовательская работа была посвящена получению гуминовых соединений с помощью модифицированного витамином С гуминовых соединений, так как в этой области не было масштабного изучения проблемы. Полученные витаминизированных гуминовых соединений в дальнейшем имеет смысл исследовать на вольтамперметрическом приборе СТА методом добавок и контроля концентраций.
Литература:
- Забрамный Т. Д., Победоносцева О. И., Победоносцева Н. И. Гуминовые кислоты и их использование. — Ташкент: Изд-во Фан, 2009–151 с.
- Колокольцев С. Н. Природные энергоносители и углеродные материалы: Состав и строение. Современная классификация. Технология производства и добычи. — М.: Книжный дом «Либроком», 2013. — 224 с.
- ГОСТ 27314–91 Топливо твердое минеральное. Методы определения влаги.
- ГОСТ 11022–95 Топливо твердое минеральное. Методы определения зольности.
- ГОСТ 9517–94 (ИСО 5073–85) Топливо твердое. Методы определения выхода гуминовых кислот.
- ГОСТ 342 Реактивы. Натрий пирофосфат 10-водный. Технические условие.
- ГОСТ 3118–77 Реактивы. Кислота соляная. Технические условия
- Александрова И. В. Взаимодействие структурных единиц и прочность их закрепления в молекулах гуминоподобных веществ// Почвоведение.- 2010. — № 12. — С.451.
- Зайковский А. В., Шендрик Т. Г., Саранчук В. И. Структурные преобразования соленых углей в процессе выделения гуминовых кислот// Химия твердого топлива. — 2011. — № 4. — С. 137.
- Комиссаров И. Д., Логинов Л. Ф. Структурная схема и моделирование макромолекул гуминовых кислот // Гуминовые препараты: научные труды. — Тюмень: Изд-во ТСХИ, 2011. — Т. 14. — С. 142.







