Целью настоящего исследования был синтез новых азометиновых производных госсипола с ароматическими аминосоединениями, и перевод этих азометинов в водорастворимое состояние.
Ключевые слова: госсипол, аминосоединение, иммуностимулятор, интерферон.
В настоящее время одной из основных проблем является синтез новых биоактивных веществ на основе природных соединений, получаемых из местных растений, и применение их в разных направлениях народного хозяйства.
Использование вещества госсипола, находящегося в составе хлопчатника, привело к созданию новых лекарственных препаратов. Известно, что само вещество госсипол и его производные имеют интерферон-индукторные свойства. Следуя из этого, можно получить основания Шиффа из госсипола с аминосоединениями, выбрав из них наиболее биоактивные вещества и применить их в медицине в виде лекарственных средств [1-2].
Многие производимые лекарственные препараты – антибиотики теряют свое действие на вирусы и бактерии. Поэтому синтез новых лекарственных веществ с повышенной чувствительностью в отношении вирусов и бактерий, имеющих интерферон-индукторные свойства и применение их в практической медицине остается одной из основных проблем на миравом уровне.
Известно, что первым низкомолекулярным индуктором интерферона является госсипол – желтый пигмент семян хлопчатника. Это уникальный не только по своему строению, но и по биологической активности полифенол. На основе самого госсипола и некоторых его производных создан ряд лекарственных препаратов противовирусного действия (3% линимент госсипола, 3% мазь мегосина, таблетки гозалидона, рагосина, мебавина). В основе специфической активности этих, разрешенных к широкой медицинской практике препаратов, лежит их способность индуцировать в самом организме , и - интерфероны. Поэтому производные госсипола, влияя на систему интерферона, оказывают опосредовано свое противовирусное действие [3-4].
Синтез новых азометиновых производных госсипола осуществляли по следующей схеме:
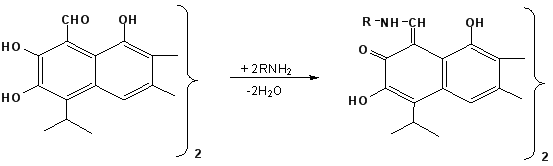
Таблица 1
Физико-химические характеристики азометиновых производных госсипола
|
Соединение |
Радикал –R |
Тпл, 0С |
Rf |
Выход прод. реак. в %-ах |
Цвет вещест. |
||
|
1 |
2 |
3 |
|||||
|
I |
|
263-64 |
0,57 |
0,87 |
0,77 |
95,15 |
Темно красный |
|
II |
|
248-49 |
0,54 |
0,86 |
0,75 |
74,68 |
Темно желт. |
|
III |
|
264-65 |
0,57 |
0,81 |
0,76 |
89,9 |
Желт. |
|
IV |
|
266-67 |
0.52 |
0,85 |
0,63 |
90,5 |
Желт. |
|
V |
|
267-68 |
0,51 |
0,80 |
0,72 |
92,35 |
Желт. |
|
VI |
|
269-70 |
0,51 |
0,76 |
0,64 |
93,95 |
Светло желт |
|
VII |
|
238-39 |
0,49 |
0,56 |
0,44 |
70,3 |
Желт. |
|
VIII |
|
206-07 |
0,50 |
0,78 |
0,56 |
98 |
Светло желт |
|
IX |
|
256-57 |
0,62 |
0,84 |
0,51 |
79,4 |
Оранж. |
|
X |
|
263-64 |
0,50 |
0,84 |
0,73 |
82,96 |
Оранж. |
Системы:1гексан-ацетон (2:1);2бензол-ацетон(5:1);3бензол-ацетон(4:1)
Была выявлена растворимость синтезированных веществ в ниже указанных растворителях как этиловый спирт, ацетон, бензол, хлороформ, диэтилэфир, гексан. Определено, что производное госсипола с фенилгидрозином хорошо растворяется в бензоле, ацетоне, хлороформе, ДМСО и ДМФА, но в этиловом спирте и гексане плохо растворяется. Производное госсипола с орто-толуидином хорошо растворяется в бензоле, ацетоне, хлороформе, гексане, а в этиловом спирте плохо растворяется. Производное госсипола с 2,4 ди NO2 нитро фенил гидразином хорошо растворяется в бензоле, ацетоне, хлороформе, а в этиловом спирте и гексане плохо растворяется. При проверке полученных веществ методом тонко-слойной хромотографии в системах гексан:ацетон (3:1,5), бензол:ацетон (5:1), бензол: ацетон (4:1) было выявлено значение Rf этих веществ в пределах интервала (0,44-0,87).
Строение и чистота синтезированных соединений установлены на основании ИК- и ПМР- спектров, в том числе РСА.
ИК-спектр самого госсипола и некоторых его иминосоединений имеют характерные полосы поглощения в области – 2140-2040, 1630-1605 и 1460-1430 см-1. В этой области дают сигнал ароматические ядра и азометиновые связи во всех изученных веществах. Для всех изученных веществ полоса поглощения изопропильной группы при С5 составляет величину 1180-1170 см-1. Валентные колебания СН3группы во всех соединениях дают сигнал в области 2970-2860 см-1, а деформационные колебания в области 1430-1380 см-1 [5-6].
В качестве спектрального критерия прохождения реакции между госсиполом и перечисленными аминами были выбраны спектры их ПМР. Для снятия ПМР спектров синтезированных веществ в качестве растворителя использовали CDC13. Изменение химсдвигов протона и проявления сигнала протона в положении 15 молекулы госсипола (альдегидной группы), лежит в пределах от 11 м.д. до 11,3 м.д., а для протона азометиновой группы (CH=N) в молекулах его производных в пределах от 9,40 до 10,40 м.д.. Поэтому исчезновение сигнала протона альдегидной группы и появление вместо него сигнала протона азометиновой группы однозначно свидетельствовало о прохождении реакции между госсиполом и амином. В спектрах ПМР также имеются сигналы соответствующие таким группам как, -ОН, -СООН, -СН, -СН2, -СН3 и др. находящихся как в самой молекуле госсипола так и в молекулах соответствующих аминосоединений [7,8,9].
Ди-2,5-ксилидингоссипол образует с ацетоном стабильный клатрат. Кристаллографические параметры монокристалла следующие: кристаллы моноклинные, пр.гр. Р21/n, C46H48O6N2C3H6O, a= 13.5738(3) Å, b=12.4839(3) Å, c=26.1622(5) Å, β= 98.277(2), V= 4387.11(17) Å3, M= 782.94, Z=4, Dвыч.= 1.185 г/см3. R=0.0666 для 5500 отражений. Молекулы ди-2,5-ксилидингоссипола образуют бесконечные цепочки с помощью Н-связей элементом симметрии плоскостью скользящего отражения. Укладка этих цепочек приводит к хозяйскую матрицу с небольшими полостями. К каждой хозяйской молекулы водородно связана одна молекула ацетона, которая заполняет одну из межклеточной полости.
В целях изучения биологической активности производных госсипола с помощью компьюторной программы анализа QSAR производится моделизирование, и это нам даёт теоретическую информацию о синтезируемых веществах до точности около 70-85%, которое помогает при изучении биологической активности веществ в практике.
Список полученных производных госсипола для проверки в анализе QSAR:
- Госсипол2. Ди-2,4-динитрофенилгидразингоссипол
3. Ди-фенилгидразингоссипол4. Ди-о-толуидингоссипол
5. Ди-п-толуидингоссипол6. Ди-2,4-ксилидингоссипол
7. Ди-2,5-ксилидингоссипол 8. Ди-п-метиламинофенолгоссипол
9. Ди-о-нитроанилингоссипол10. Ди-нафтиламингоссипол
11. Ди-бензидингоссипол
На этих рисунках показаны производные госсипола QSAR в моделированых анализах.
|
Рис 1. |
Рис 2. |
|
Рис 3. |
|
Рис.1. – свойства антиоксиданта; Рис.2 - активность против вируса герпес; Рис.3 – активность интерферон индуктора; Рис 4 – иммуномодуляторные активности.
Литература:
1. Хаитбаев А.Х., Тилябаев З., Ачилова Г.Ш., Хаитбаев Х.Х., Ауелбеков С.А. Синтез и биологическая активность некоторых производных госсипола // Химия природн. соедин. – Ташкент, 1995. – №1. – С.56-58.
2. А.И. Глушенкова, И.П. Назарова. Госсипол, его производные и их использование. Ташкент, Фан, 1993, 88 с.
3. Барам Н.И., Исмаилов А.И., Зияев Х.Л., Режепов К.Ж. Биологическая активность госсипола и его производных // Химия природн. соедин. – Ташкент, 2004. – №3. – С.171-176.
4. Хакбердиев Ш.М., Далимов Д.Н., Маманазарова Н., Хаитбаев А.Х., Талипов С.А., Ибрагимов А.Б. “Синтез азометиновых производных госсипола с ароматическими аминосоединениями” // Узбекский химический журнал. – Ташкент, 2013. №2. – С. 8-11.
5. Wang J., Cooper G., Tulumello D., Hitchcock A.P. J.Phys.Chem. A.,Vol.109, P.10886-10896 (2005).
6. Siemens; XP. Molecular Graphics Program. Version 5.03. Siemens Analytical X-Ray Instruments Inc., Madison, Wisconsin, USA, 1994.







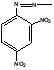
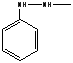
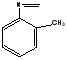
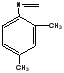
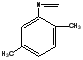
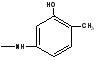
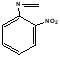
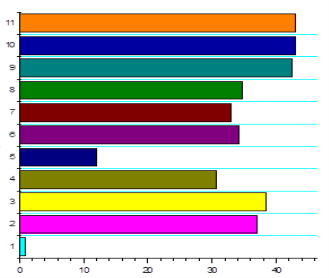
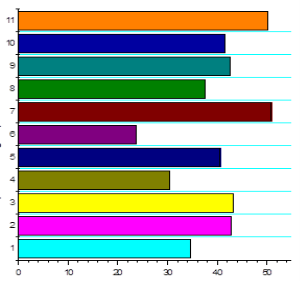
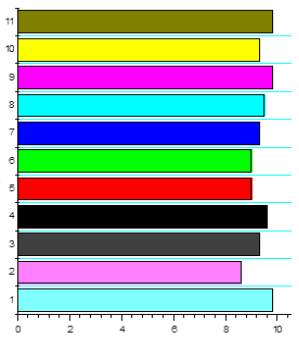
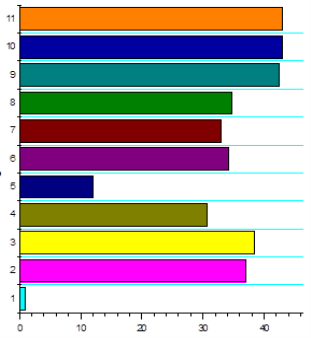 Рис 4.
Рис 4.
