Коррозией металлов называют самопроизвольное разрушение металлических материалов вследствие химического или электрохимического взаимодействия их с окружающей средой. Коррозионный процесс протекает на границе раздела двух сред металла и окружающей среды, т. е. является гетерогенным процессом взаимодействия жидкой или газообразной среды с металлом (рис. 1).
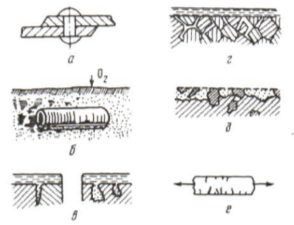
Рис. 1. Некоторые типы гетерогенности поверхности корродирующего металла: а –контакт разнородных металлов; б –дифференциальная аэрация; в –образование щелей и питтингов; г –межкристаллитная коррозия; д –структурно-избирательное разрушение; е –коррозионное растрескивание, или коррозионная усталость, при приложении нагрузки.
Способность металлов сопротивляться воздействию среды называется коррозионной стойкостью, или химическим сопротивлением материала. Металл, подвергающийся коррозии, называют корродирующим металлом, а среда, в которой протекает коррозионный процесс, — коррозионной средой. В результате коррозии изменяются свойства металла и зачастую происходит ухудшение его функциональных характеристик.
Металл при коррозии может частично или полностью разрушаться. Химические соединения, образующиеся в результате взаимодействия металла и коррозионной среды, называют продуктами коррозии. Продукты коррозии могут оставаться на поверхности металла в виде оксидных пленок, окалины или ржавчины. В зависимости от степени адгезии их к поверхности металла наблюдаются различные случаи. Например, ржавчина на поверхности железных сплавов образует рыхлый слой, процесс коррозии распространяется далеко в металлы может привести к образованию сквозных язв и свищей. Напротив, при окислении алюминия на поверхности образуется плотная сплошная пленка оксидов, которая предохраняет металл от дальнейшего разрушения [1–5, 9, 15, 24].
Первопричиной коррозии металлов является их термодинамическая неустойчивость в различных средах при данных внешних условиях, т. е. самопроизвольный переход металла в более устойчивое окисленное состояние за счет уменьшения термодинамического потенциала системы, которое достигается в результате реакции:
металл + окислительный компонент среды = продукт коррозии
Термодинамика дает исчерпывающие сведения о возможности или невозможности самопроизвольного протекания коррозионного процесса при определенных условиях. Термодинамические потенциалы могут быть использованы для количественной оценки движущих сил химических или электрохимических коррозионных процессов, а также для расчета скоростей этих процессов и практических методов защиты от коррозии, т. е. создания условий, уменьшающих или полностью исключающих возможность протекания коррозионного процесса.
Однако термодинамика не дает ответа на вопрос, с какой скоростью будет протекать термодинамический возможный коррозионный процесс. Рассмотрением этого вопроса, а также установлением влияния различных факторов на скорость коррозии и характер коррозионного разрушения металлов занимается кинетика (учение о скоростях) коррозионных процессов. Отличительной особенностью коррозионных процессов является их сложность и много стадийность. Обычно коррозионный процесс состоит из трех основных стадий:
1) перенос реагирующих веществ к поверхности раздела фаз;
2) собственно гетерогенная реакция;
3) отвод продуктов реакции из реакционной зоны.
Каждая из этих стадий может протекать последовательно или параллельно с образованием на поверхности металла продуктов коррозии. Реакция окисления происходит, когда металл соединяется с атомом или группой молекул, теряя при этом электроны, либо когда он переходит из одной степени окисления в другую, более высокую. Суммарная реакция окисления этого типа может быть представлена как две реакции, протекающие одновременно [1]:
окисление ![]() электронов;
электронов;
восстановление ![]() электронов
электронов 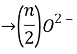 ;
;
суммарная реакция ![]() .
.
Одновалентный металл будет образовывать один оксид, многовалентный может формировать, как правило, несколько различных оксидов, число которых определяется валентностью металла. Оксиды электрически нейтральны, имеют определенную кристаллическую структуру, состоят из зерен (кристаллов), свойства которых подобны свойствам металлов. Оксид способен к рекристаллизации, росту зе-рен и может подвергаться пластической деформации, особенно при высоких температурах. Для всех металлических изделий, испытывающих механическую нагрузку, наиболее опасными являются локальные виды коррозии. Это демонстрирует график зависимости потерь прочности дюралюминия от коррозионных потерь веса при различных видах коррозионного разрушения (рис. 2).
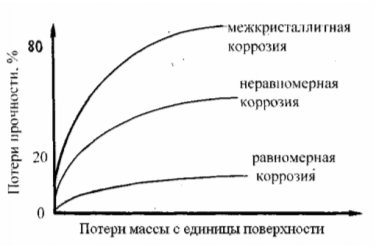
Рис. 2. График зависимости изменения прочности от коррозионных потерь
В зависимости от того, как распространяются коррозионные трещины, коррозионные разрушения принято делить на транскристаллитные, когда разрушение протекает по телу зерен и интеркристаллитные или межкристаллитные, когда разрушение происходит по границам зерен. В межремонтный период происходят утечки нефти, газа и воды вследствие коррозионных повреждений, из-за отложения продуктов коррозии ухудшается теплопроводность поверхностей теплообмена, уменьшение проходных сечений трубопроводов из-за отложения ржавчины требует повышения мощности насосов — все это обходится в миллионы долларов в год. Загрязнение продукции также оценивается в миллиарды долларов, например, небольшое количество меди, поступившее в систему в результате коррозии медного трубопровода или латунного оборудования, может испортить целую партию продукта. Следы металлов могут изменять цвет красителей. Свинцовое оборудование не может быть использовано для приготовления и хранения пищевых продуктов из-за токсичности солей свинца. Мягкая вода, проходящая по свинцовым трубопроводам, небезопасна для питья. По заключению Бюро продуктов питания и лекарственных препаратов, допустимая концентрация свинца в пище не должна превышать 1 мг/л.
К этой же группе потерь относится порча продуктов питания из-за ржавления металлических емкостей. Один из заводов, консервирующих фрукты и овощи, терпел убытки около миллиона долларов в год до тех пор, пока не были выявлены и устранены металлургические факторы, приводившие к локальной коррозии. Другая компания, использующая металлические крышки на стеклянных консервных банках, теряла 0,5 млн долларов в год из-за точечной коррозии крышек, что приводило к бактериальному заражению продукции. При расчете толщины стенки аппаратов и его проектировании используются допуски на коррозию. В тех случаях, когда скорости коррозии неизвестны, а методы борьбы с коррозией неясны, задача оптимального проектирования значительно усложняется. Надежные данные о скорости коррозии позволяют более точно оценить срок эксплуатации оборудования и упрощают его проектирование. Например, расчетная толщина стенки трубопровода диаметром 200 мм и длиной 362 км с учетом коррозии составляет 8,18 мм. А применение соответствующей защиты от коррозии позволяет снизить эту величину до 6,35 мм, что приводит к экономии 3700 т стали и увеличению полезного объема трубопровода на 5 %. Отсюда видно, что косвенные потери составляют существенную часть общих коррозионных потерь, однако их подсчет представляет собой трудную задачу даже в рамках одной отрасли промышленности. В ряде случаев потери вообще не могут быть выражены в денежных единицах. К ним относятся аварии, связанные с взрывами, разрушением нефтехимического оборудования, или вызванные коррозией катастрофы самолетов, поездов, автомобилей, приводящие к потере здоровья или гибели людей.
Литература:
- Кац Н. Г., Стариков В. П., Парфенов С. Н. Химическое сопротивление Материалов и защита оборудования нефтегазопереработки от коррозии. М.: Машиностроение. -2011 г.
- Жук Н. П. Курс теории коррозии и защита металлов: учеб. Пособие/ Жук Н. П. -2-е изд., стереотипное. Перепечатка издания 1976.-М:. ООО ТИД «Альянс», 2006.-472.
- Сухотина А. М., Шрейдера А. В., Арчакова Ю. И.-Коррозия и защита химической аппаратуры. Нефтеперерабатывающая и нефтехимическая промышленность. Под.ред-М.: Химия, 1974г-576 с.
- Клинов И. Я. Коррозия химической аппаратуры. Коррозионностойкие материалы. Учеб.пособие/ -М.: Машинастроение, 1976.-462 с.







