Изучено алкилирование о-ксилола трет-бутанолом на цеолитах типа У модифицированных переходными элементами. Установлена высокая активность цеолитных катализаторов содержащих два многозарядных катиона (FeCaNaY, CrCoCaNaY и CoCaNaY) и показано, что переходные элементы влияют на активность катализаторов путем регулирования протонных и апротонных кислотных центров. Критерием эффективной работы катализатора является равенство отношений интенсивностей п. п. 3650 см-1 и 3550 см-1, которая достигается при содержании катионов железа в составе FeCaNaY порядка 55–60 %.
Ключевые слова: алкилирование, о-ксилол, трет-бутанол, цеолит типа У
4-Третбутилортоксилол (4-ТВОК) предложен в качестве исходного вещества для получения высококачественных фталоцианиновых пигментов пластификаторов, фотоматериалов и других ценных продуктов [1–3]. Разработка технологичного, высокопроизводительного, экологически чистого метода синтеза 4-ТВОК представляет несомненный практический интерес. Одним из перспективных направлений синтеза 4-ТВОК является алкилирование о-ксилола трет-бутанолом на цеолитах [4,5]. В работах [5,6] исследованы способы регулирования активности, селективности и стабильности цеолитных катализаторов в реакции алкилирования о-ксилола трет-бутанолом. Установлено, что каталитические свойства цеолитных систем зависят не только от присутствия протонных центров, но и от их доступности для реагирующих молекул, поскольку расположены они главным образом внутри полостей кристаллов, к которым ведут окна молекулярных размеров. Низкую активность среднепористых Н-пентасилов и Н-морденита в алкилировании о-ксилола трет-бутанолом по мнению авторов [6] связано торможением, десорбцией и диффузией, таких объемных молекул как 4-ТВОК в полостях и каналах этих цеолитов.
В настоящей работе изучено влияние природы и концентрации катионов переходных металлов на каталитические и кислотные свойства цеолита типа Y в реакции алкилирования о-ксилола трет-бутанолом.
Экспериментальная часть
Катализаторы готовили из порошкообразного цеолита NaYс мольным соотношением SiO2/Al2O3 равным 5,0, методом ионного обмена из растворов NH4+, Ca2+,Ni2+, Cr3+и Fe3+. Бикатионные формы цеолитов получали из цеолита 0,86 CaNaY путем ионного обмена по методике, описанной в работе [7]. Степени обмена Na+ и Men+указаны числами перед соответствующими катионами в символе цеолитов.
Перед использованием цеолиты прогревали в токе воздуха при 5000С в течение 4ч. Активность образцов изменялась во времени в ходе каталитического процесса. Опыты проводили на лабораторной проточной установке с кварцевым реактором с загрузкой 5см3 катализатора при атмосферном давлении в интервале температур 130–2000С, мольном отношении С6Н4(СН3)2: С4Н9ОН равном 4:1 и объемной скорости 2,0 ч-1.
ИК-спектры снимали на спектрометре FTIR-7600. по методике, включающей получение таблеток с КВr. Полупрозрачные таблетки получали при тщательном перемешивании тонко-измельченной пробы цеолита с порошком КВr (в соотношении 1:10) с последующим прессованием смеси в пресс-форме. Таблетки толщиной 8–10 мг/см2 помещали в кювету, дегидратировали в токе осушенного воздуха при 5000С в течении 4ч. охлаждали под откачкой до 0,066 Па и напускали пиридин (Ру). Условия контактирования образцов Ру: 20 и 1500С, давление паров 1733,2 Па, 30 мин. Перед регистрацией спектров удаляли физически сорбированной Ру откачкой.
Результаты иих обсуждение
Каталитические свойства цеолита Y существенно зависят от природы обменного катиона в цеолите. NaY практически не проявляет активность в реакции алкилирования, но при 2000 С на нем наблюдается 68 %-ная конверсия спирта, практически полностью в направлении дегидратации. Замещение Na+ на катионы Са2+ и переходных металлов резко увеличивает активность катализатора. Так, на 0,74 FeNaY при 1400С выход 4-ТВОК достигает 64,5 %. Са-форма цеолитов проявляет более низкую активность, чем цеолиты содержащие катионы переходных металлов. Так, если на цеолите 0,86 CaNaY при 1400С выход 4-ТВОК составляет 49,6 %, то на Со-, Cr- и Fe- формах цеолита выход 4-ТВОК составляет 62,7–66,2 %. Среди исследуемых катионных форм наибольшую активность и селективность проявляет Fe-форма цеолита типа Y.
Таблица 1
Влияние степени ионного обмена иприроды катионов вцеолите Yна его каталитические свойства валкилировании о-ксилола трет-бутанолом
v=2ч-1, С6Н4 (СН3С4Н9ОН=4:1(мольное)
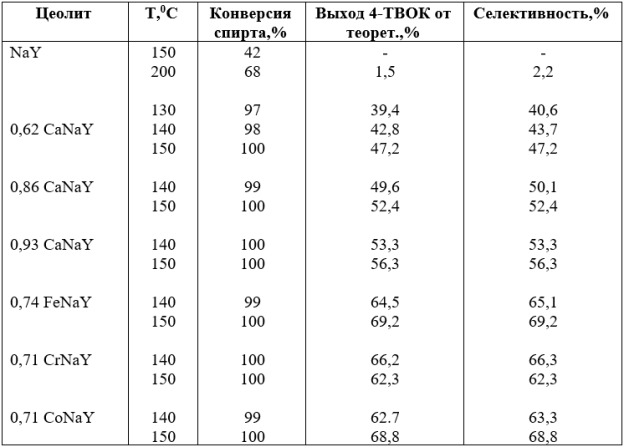
Са-форма цеолитов проявляет более низкую активность, чем цеолиты содержащие катионы переходных металлов. Так, если на цеолите 0,86 CaNaY при 1400С выход 4-ТВОК составляет 49,6 %, то на Со-, Cr- и Fe- формах цеолита выход 4-ТВОК составляет 62,7–66,2 %. Среди исследуемых катионных форм наибольшую активность и селективность проявляет Fe-форма цеолита типа Y. На цеолите 0,74 FeNaY при 1400С выход и селективность по 4-ТВОК составляет 69,2 %. Природа катиона также сильно влияет на стабильность цеолитного катализатора. Чем больше заряд катиона, тем меньше скорость падения алкилирующей активности катализатора после достижения максимума за 2–4 ч работы образцов. (табл.2)
Для цеолита 0,86 CaNaY максимальный 4-ТВОК выход (49,6 %) достигается после достижения 2 ч. работы, после чего наблюдается резкое снижение его активности. После достижения 6 ч. работы выход 4-ТВОК составляет всего 2,1 %. В отличие от цеолита 0,86 CaNaY на цеолите 0,74 FeNaY и 0,71 CrNaY до достижения 4 ч. работы наблюдается рост активности и селективности. При этом выход 4-ТВОК возрастает с 51,2–53,2 % до 74,7–76,3 %. Увеличение продолжительности работы до 6 ч. заметно снижает активность и селективность этих образцов.
Таблица 2
Изменение каталитических свойств катионных форм цеолитов типа Yво времени впроцессе алкилирования о-ксилола трет-бутанолом
Т=1400С, v=2ч-1, С6Н4:СН3С4Н9ОН=4:1(мольное)
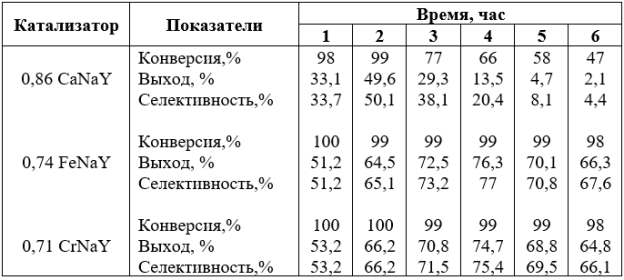
Рост активности в начальный период процесс обусловлен, по-видимому, кинетическими особенностями протекания реакций алкилирования на цеолитных катализаторах [2,3]. Вода, выделяющаяся в процессе алкилирования, может оказывать большое влияние не только на активность, но и на стабильность цеолитного катализатора. При большей плотности катионов металлов вода удерживается в цеолите прочнее, изменяя адсорбционно-десорбционное равновесие в системах реагент-цеолит-продукт. По-видимому, этим можно объяснить более высокую стабильность FeNaY и CrNaY по сравнению с CaNaY при прочих равных условиях наибольшей селективностью и стабильностью обладает цеолит 0,74 FeNaY (табл.2).
Отсутствие в ИК-спектре Na-формы цеолита Y п. п. в области 1550 см-1,т. е. полосы, характеризующей образование пиридиний-катиона (РуН+), свидетельствует об отсутствии бренстедовских кислотных центров у этого цеолита. Замещение катионов Na+ на многозарядные катионы приводит к появлению п. п. в области 1550 см-1. Интенсивность этой полосы существенно зависит от природы катиона.
В ИК-спектре Ca-формы цеолита наблюдается п. п. с очень слабой интенсивностью. На Fe и Cr-формах цеолитов Y наблюдается существенный рост п. п. в области 1550 см-1, что указывает на возникновение более сильных бренстедовских кислотных центров. Характер изменения активности катионных форм цеолита типа У коррелирует с изменением силы и концентрации бренстедовских кислотных центров.
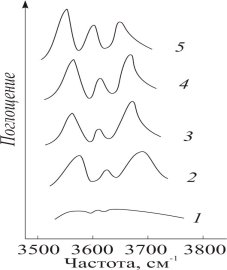
Рис 1. ИК-спектры в области валентных колебаний гидроксильных групп катализаторов: 1-NaY; 2-CaNaY; 3-CoNaY; 4-CrNaY; 5-FeNaY
Введение в состав катализатора 0,86 CaNaY 20 % катионов переходных металлов (Fe3+, Co2+, Cr3+) приводит к существенному росту его алкилирующей активности. Например, если при 1400С на монокатионных формах цеолита У выход 4-ТВОК составляет 49,6–64,5 %, то на бикатионных формах цеолита У выход 4-ТВОК составляет 68,5–74,5 % (табл.3).
Таблица 3
Алкилированиео-ксилола трет-бутанолом на бикатионных формах цеолита типа Y, Условия: Р=1 атм, V=2 ч-1, С6Н4 (СН3)2/С4H9ОН=4:1
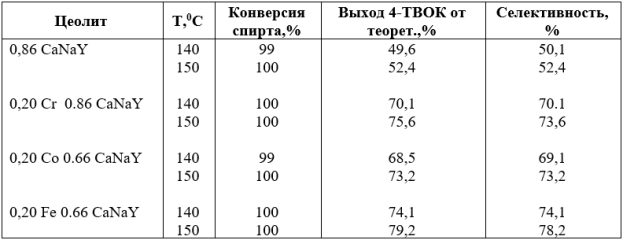
Следовательно, катионы переходных металлов оказывают промотирующее действие на активность катализатора 0,86 CaNaY. Наиболее сильное промотирующее действие на активность катализатора 0,86 CaNaY оказывают катионы Fe3+. При температуре реакции 1500С выход 4-ТВОК на бикатионных формах цеолита У содержащих катионы Cr3+, Co2+ и Fe3+составляет 73,2–79,2 %. Каталитическая активность бикатионных форм цеолитов У зависит также от концентрации катионов Fe3+ в составе катализатора CaNaY. Видно, что увеличение степени обмена катионов Cа2+ на катионы Fe3+до 55 % способствует возрастанию выхода 4-ТВОК до 86,3 % (рис.1) Увеличение степени обмена катионов Fe3+ в составе катализатора CaNaY выше 60 % приводит к снижению его активности. На катализаторе, содержащем 76.0 % катионов Fe3+ выход 4-ТВОК снижается до 72,2 %.
Введение в кальциевую форму катионов Fe3+ приводит к появлению п. п. при 3550, 3610 и 3650 см-1. Наиболее высоким комплексом каталитических свойств в реакции алкилирования обладает тот катализатор, ИК-спектр которого характеризуется близкими величинами интенсивности п. п. при 3650 и 3550 см-1.
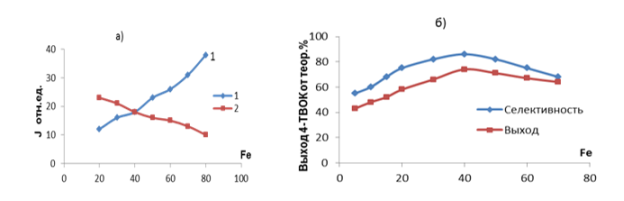
Рис. 2. Влияние содержания жeлеза на генезис гидроксильных групп с. п.п. 3650 см-1 (1) и 3550 см-1(2) катализатора FeCaNaY (а), на выход и селективность по 4-TBOK (б)
Так, при изменении содержания Fe3+в цеолите У с 40 % до 90 % (катализатор приготовлен в условиях термального ионного обмена) наблюдается уменьшение интенсивности п. п. при 3650 см-1 и рост интенсивности п. п. при 3550см-1 (рис.2), причем при содержании Fe3+ порядка 55–60 % эти полосы равноинтенсивны. Из условия равенства интенсивностей п. п. гидроксильных групп как необходимого условия получения активно и стабильно работающего катализатора вытекает вывод о необходимости сочетания в катализаторе FeCaNaY апротонной и протонной кислотности и об участии в реакции алкилирования кислотных центров различной природы.
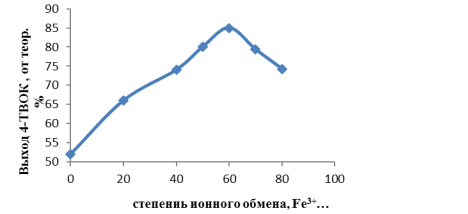
Рис. 3. Влияние степени ионного обмена Fe3+ в составе цеолита FeCaNaY на выход
4-ТВОК
Таким образом, критерием эффективности работы катализатора на основе бикатионной формы (FeCaNaY) является определенное сочетание протонных и апротонных кислотных центров в составе активного центра. Качественной оценкой его может служить равенство интенсивностей п. п. при 3650 и 3550 см-1
Литература:
- Rakusan J, Marakovskaya G. M., Zelenka J., Kozlova T.S, //Aut Cert 256147 (Czechoslavakia). Chem. Abstrs. -1989.
- Исаков Я. И., Миначев Х. М., Позднякович Ю. В. Способ получения 1,2-диметил-4-третбутилбензола: А.с. 1778107СССР //РЖХим. -1993. -14Н57П
- Исаков Я. И., Миначев Х. М., Калинин В. П., Исакова Я. И. Алкилированиео-ксилолатретбутанолом на цеолитных и цеолитсодержащих катализаторах // Нефтехимия, -1994,-т.34.,- № 1, -с.42–49.
- Yadav G. D., Kambee S. B. Fridel-Krafts green alkylation of xylenes with tert-butanol over meseporonssuperalid UDCAT-5//Chem.Eng.Res. and Design,-2012,-v 90 -p.1322–1334.
- İsakov Y. İ., Minachev Kh. M, Kalinin V.P, İsakova T. A. Selective alkylation of xylenes by alcoholos on zeolite catalysts // Russian Chemical Bulletin. -1996 -V.45, -N2, -p. 2763–2768.
- Исаков Я. И.,Миначел Х. М., Калинин В. Л., Исакова Т. А.,Селективный катализ алкилироввния кслилолов спиртами на цеолитах. //ДАН, -1994, -г.335, -№ 3, -с. 322–325.
- G. X. Valiyeva, S. E. Mammadov, E. I. Ahmadov. Tert-butylation of o-xylene over dealuminated mordenite. //Journal of environmental science, Computer Science and Engineering & Technology\\ JECET; -2016; -Sec. -A; -Vol.5. -No.1, -с.149–154.







