Медицина — отрасль, в которой, как и во многих других, огромное значение имеет человеческий фактор. Начиная от уровня знаний и квалификации конкретного врача/медицинской сестры, заканчивая утомлённостью и разнообразными личными переживаниями, которые могут сказаться на восприятии и привезти к неправильным выводам и ошибкам.
Если в других отраслях, ошибка может быть обнаружена и исправлена на следующих этапах взаимодействия (например: тестовый прогон двигателя или краш-тест автомобиля), то в медицине, ключевой пункт взаимодействия — пациент и если произошла врачебная ошибка, то исход вполне может быть фатальным, а ошибка может быть так и не замечена, что в свою очередь на перспективе может привести к множественному повторению данной ошибки.
В век современных технологий скорость и эффективность лечения можно существенно повысить за счёт автоматизации различных процессов в медицинской практике. Ключевым инструментом автоматизации в медицинской среде являются разнообразные информационные системы.
Информационные системы решают множество медицинских задач и применяются как в качестве решения для комплексной (онлайн-запись, автоматизация регистратуры, рабочее место врача, касса и финансы, дистанционная диагностика, управленческая отчетность, складской учет, телефония, многое другое), так и точечной автоматизации в медицинских учреждениях, поликлиниках, клиниках общего профиля, стоматологических клиниках, косметологических центрах, стационарах, санаториях, отделениях скорой помощи, лабораториях, отделениях или кабинетах частных врачей.
На текущий момент активно развиваются системы информационного обеспечения здравоохранения. Одним из ключевых векторов развития современного этапа информатизации сферы, является разработка компьютеризированных систем поддержки принятия врачебных решений (СППВР). Информационных системы, которые используются врачами в процессе принятия ими лечебно-диагностических решений включают в себя множество программных средств. К СППВР могут быть отнесены специализированные медицинские базы данных, системы обработки медицинских изображений, библиографические информационно-поисковые системы, телемедицинские и обучающие системы и т. д.
Под термином «экспертные системы» в медицине обычно подразумеваются системы, которые помогают врачу поставить диагноз. Некоторые авторы [2] отмечают, что в настоящее время, происходит смещение классического понятия «экспертная система» из области постановки диагноза в область систем, обеспечивающих качество медицинской помощи, помогающих врачу принимать наиболее эффективные решения в процессе лечения пациента.
Все экспертные системы построены на различных моделях (макет, изображение, схема, карта, словесное описание, математическое представление), которые позволяют выделить главное в реальном объекте, не отвлекаясь на детали. Среди моделей, которые используются в медицине можно выделить: биологический, физико-химический и математический.
Методом моделирования можно изучить и исследовать объекты и процессы построением и описанием системы, которая может быть использована вместо реальной системы при решении некоторых научных или практических задач.
Математическое моделирование является наиболее адекватным (приемлемым) инструментом фармакологии. Фармакология делится на 2 раздела: фармакодинамика и фармакокинетика.
Фармакодинамика — раздел фармакологии, изучающий эффекты лекарственных веществ на системы организма, либо на организм в целом. Исследователя интересует зависимость эффекта ЛВ от времениE(t).
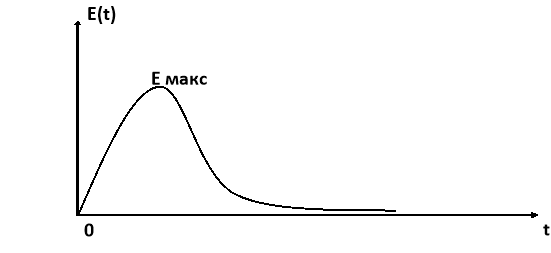
Фармакокинетика — один из разделов фармакологии, где изучается то, как организм влияет на лекарственные вещества (ЛВ) (т. е. распределение ЛВ, его всасывание, метаболизм, выделение из организма). В фармакокинетике исследователя интересует зависимость концентрации препарата от времени C(t).
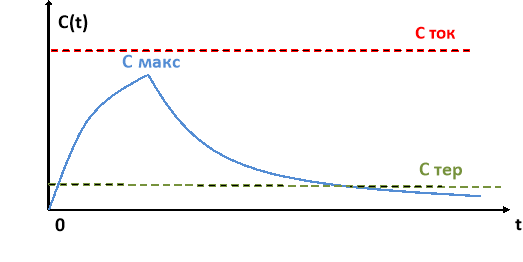
Традиционно фармакокинетика основывается на математическом моделировании динамики концентрации введенного в организм препарата.
Математическая модель, достаточно точно описывающая закономерность формирования концентрации в крови вводимого лекарственного препарата, позволяет при выбранной дозе препарата заранее просчитать (вычислить), выйдет ли его концентрация в крови за пределы коридора, ограниченного двумя фармакокинетическими константами — минимальными терапевтической (Стер) и токсической (Стокс) концентрациями.
Если максимальная концентрация окажется больше Стокс, то, уменьшая назначаемую дозу, можно в численном эксперименте с моделью на компьютере подобрать допустимую дозу, при которой концентрация не превысит токсического уровня. На этой же модели можно определить, когда нужно ввести последующую (поддерживающую) дозу, чтобы не допустить снижения концентрации ниже терапевтического уровня, то есть выбрать интервал введения препарата. Таким образом, мы используем математическую модель вместо того, чтобы проводить подбор режима введения непосредственно у пациента, измеряя концентрацию препарата в крови после введения начальной дозы и убедившись, что она слишком велика, в следующий раз ввести меньшую дозу и т. д.
Описание процесса внутривенного введения препарата
При внутривенном введении препарата всегда имеется некоторый интервал времени, в течение которого, плавно надавливая на шприц, врач (медсестра) с постоянной скоростью вводит в вену определенное количество раствора с препаратом или для облегчения труда может быть использована капельница с разведенным в физ. растворе. Более того, для некоторых препаратов в инструкции по способу введения указывается, например, «вводить медленно в течение 5 минут».
Таким образом, можно считать, что скорость введения препарата имеет определенную форму: она постоянна в течение некоторого периода (например, 5 минут), а далее скорость введения равна нулю (так как введение прекращено). Изменения концентрации препарата в крови, происходящие синхронно с изменениями скорости введения.
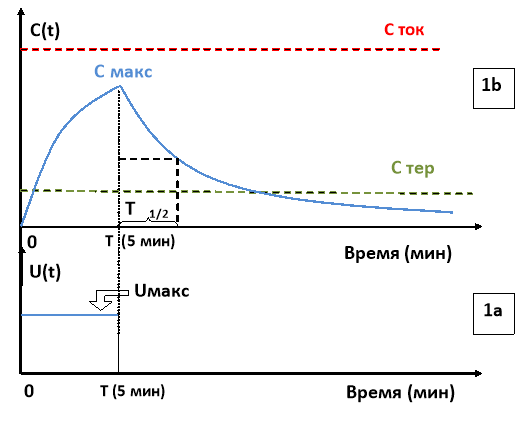
Основными характеристиками кривой C(t) являются следующие:
‒ Максимальное значение концентрации Cmax, которое достигается в момент прекращения введения препарата;
‒ Время полувыведения T 1/2, определяемое по нисходящей части графика C(t), как период времени, за который концентрация препарата снижается в два раза.
Описанные на рис. процессы могут быть представлены в виде схемы
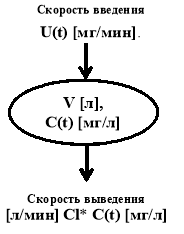
- Объем (кажущийся), в который вводится препарат, обозначен величиной V [л].
- Скорость введения препарата — Uввед(t) [мг/мин].
Скорость введения препарата задается врачом: определив дозу (D) и время его введения (Т), врач тем самым определяет величину Umax, которая равна отношению D / T. Например, если за 5 минут требуется ввести 500 мг препарата, то максимальная скорость введенияUmax = 500 / 5 = 100 [мг/мин].
- Концентрация препарата в крови — C(t) [мг/л].
- Скорость выведения препарата — Uвывед(t) [мг/мин] пропорциональна концентрации препарата в объеме V, то есть будем считать, что эта скорость равна концентрации C(t), умноженной на некоторый коэффициент, который в фармакокинетике называется общим клиренсом препарата, — Uвывед (t) = Cl * C(t).
‒ Кажущийся объем V [л] это такой гипотетический объем, в котором нужно было бы растворить введенное количество препарата, чтобы его концентрация оказалась равной концентрации, реально наблюдающейся в крови.
Следует отметить, что если бы объем V совпадал бы с объемом крови (5 литров у пациента с массой тела 70 кг), то к концу введения 500 мг препарата ожидаемая максимальная концентрация (на 5-й минуте) должна была бы составить 100 [мг/л], то есть весь введенный препарат целиком оставался бы в крови. Однако, цель внутривенного введения препарата заключается в его доставке в органы мишени и, следовательно, к 5-й минуте часть препарата перейдет в другие объемы, в которых помимо крови он распределяется (ткани-мишени, печень, почки и др.). Таким образом, в крови должно остаться существенно меньше препарата, то есть его концентрация в крови в действительности будет меньше, чем 100 [мг/л]. Поэтому на схеме, представленной на рис 1, в качестве объема, в который вводится препарат, рассматривается условный объем, в котором к концу введения препарат оказывается распределенным и концентрация препарата во всех частях которого равна концентрации реально наблюдаемой в крови. Этот объем является важной фармакокинетической характеристикой препарата, которая носит название кажущийся объем.
‒ Клиренс — Cl [л/мин] — это количество плазмы в литрах, освобождаемое (очищаемое) от препарата за единицу времени;
при внутривенном введении препарата пациенту со сниженным клиренсом можно использовать те же дозы, что и при нормальном клиренсе, но интервал между повторным введением тем больше, чем меньше клиренс
‒ Минимальная терапевтическая концентрация — это минимальная концентрация препарата, ниже которой препарат перестает оказывать терапевтическое действие;
‒ Минимальная токсическая концентрация — это минимальная концентрация препарата, выше которой препарат начинает оказывать токсическое действие.
Построение математической модели
Для вывода математической модели используется закон сохранения вещества: скорость изменения количества вещества в каждой камере равна разнице между скоростями всех веществ, поступивших в камеру и веществ, покинувших камеру за данный момент времени.
Отсюда имеем математическую модель внутривенного введения препарата:
![]()
Для реализации работы математической модели на компьютере необходимо преобразовать формулу в другой вид:
![]()
![]()
![]()
Получаем необходимую формулу:
![]()
На основании описанной выше математической модели, была разработана информационная система (ИС), которая позволяет вносить в неё исходные данные по пациенту и препарату, автоматически производя необходимые вычисления.
Рис. 1. Основное окно программы без добавленных препаратов
После запуска программы необходимо внести данные пациента и добавить препарат с указание входящих данных.
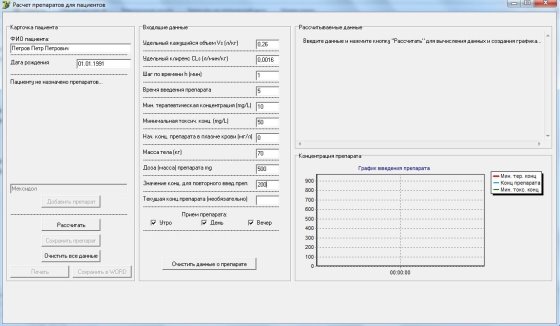
Рис. 2. Входные данные введены
После нажатия на кнопку «Рассчитать» ИС производит автоматические расчеты и выводит на экран график введения препарата и график введения препарата.
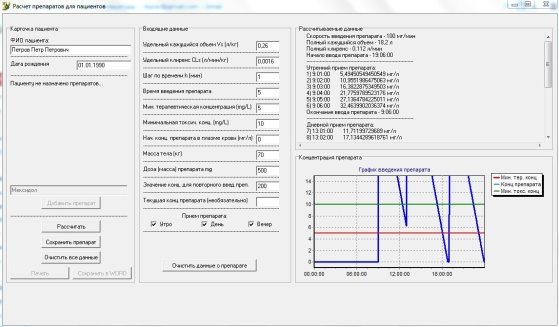
Рис. 3. Результат расчета ИС
Кроме возможности автоматического расчета, ИС содержит функционал, который позволяет сохранить данные для последующей распечатки (рис. 4) и сохранения данных в формате WORD (рис. 5). В качестве выводных данных используется «лист назначений» и график введения препарата.
Рис. 4. Функция печати.
Рис. 5. Функция сохранения в формате WORD.
Внедрение системы автоматического расчёта дозирования возможно с использованием имеющихся вычислительных мощностей уже интегрированных в ЛПУ, таким образом процент используемого потенциала оборудования увеличится, но останется в приемлемых пределах, а эффективность работы ЛПУ существенно повысится.
Человеческие ошибки в назначении дозирования являются довольно распространенной проблемой при лечении. Программный комплекс после тщательной проработки и тестирования в условиях, приближенных к реальным, — полностью исключит возможность ошибки на этапе расчёта дозировки, связанные с человеческими факторами, в том числе переутомлением и монотонностью выполняемого труда.
Литература:
- Кобринский Б. А., Зарубина Т. В. Медицинская информатика. — М.: Академия, 2009. — 192 с.
- Радченко С. В. Информационные технологии поддержки принятия врачебных решений//Информационные технологии в здравоохранении. — 2002. — № 13–14.
- Черников Е. Э., Зарецкий ММ, Черникова Н. М. Врачебная ошибка: невежество или халатность?//Украинский медицинский журнал. — 2009. — № 2(70).
- Как часто ошибаются врачи? // РОССИЙСКАЯ ГАЗЕТА. URL: https://rg.ru/2007/02/16/mediki.html (дата обращения: 28.04.2017).







