Кроветворение представляет собой тонко регулируемый процесс последовательных дифференцировок родоначальных клеток, приводящий к образованию зрелых форм всех 8 линий (эритроциты, клетки миелоидный ряд: базофильные, нейтрофильные, эозинофильные гранулоциты, мегакариоциты, моноциты-макрофаги, лимфоидный ряд: Т- и В-лимфоциты). Кроветворные клетки у млекопитающих образуются и распределяются в органах кроветворения. Они разделяются на эмбриональные органы кроветворения (желточный мешок, эмбриональная печень, селезенка и костный мозг) и взрослые (костный мозг, селезенка, тимус, лимфатические узлы и пейеровы бляшки).
Существует несколько уровней регуляции кроветворения: геномно-ядерный; внутриклеточный; межклеточный; организменный.
Эти системы работают в тесном взаимодействии. Наряду с регуляторными факторами, вырабатывающимися в самом организме, на гемопоэз оказывает стимулирующее влияние ряд экзогенных факторов.
В жизни клеточных популяций значительную роль играет программируемая гибель клеток (апоптоз) — своеобразный механизм клеточного убийства. Апоптоз ответственен за поддержание правильной численности клеток в быстро размножающихся тканях эмбриона (например, в головном мозге). Кроме того, он запускается практически всегда, когда происходят нарушения прохождения клеточного цикла (задержка в митозе, неправильная репликация ДНК). Нарушение механизма программируемой клеточной гибели характерно для многих опухолевых клеток и, возможно, является одним из фундаментальных отличий их от нормальных.
На базе БУ РКБ г. Чебоксары имеется гематологический центр, единственный в республике, оказывающий высококвалифицированную помощь гематологическим больным в условиях поликлиники и отделения гематологии и химиотерапии. Динамика гематологической заболеваемости за последние 3 года с учетом пола, возраста, нозологии отражена на следующих графиках (Рисунки 1–6).
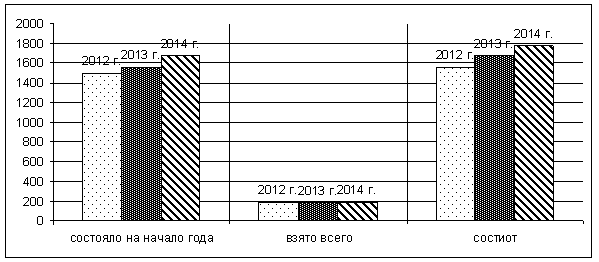
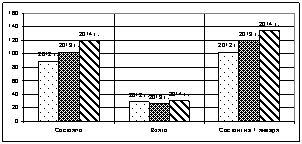
Рис. 1. Количество больных, состоящих на диспансерном учете у гематолога за 2012–2014 гг.
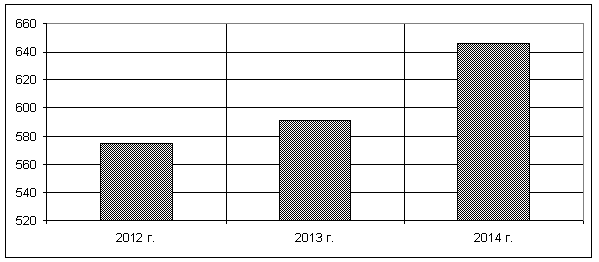
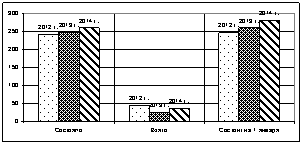
Рис. 2. Количество анализов на миелограмму за 2012–2014 гг.
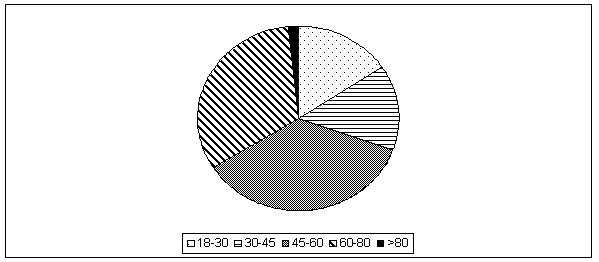
Рис. 3. Распределение анализов на миелограмму по возрастам за 2015 г.
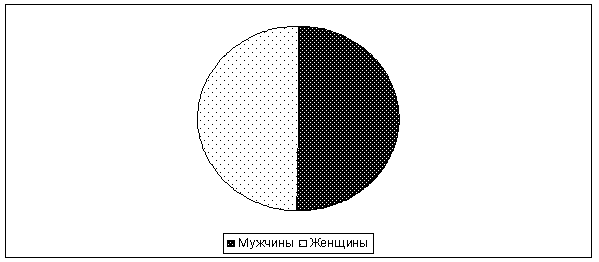
Рис. 4. Распределение анализов на миелограмму по полу за 2015 г.
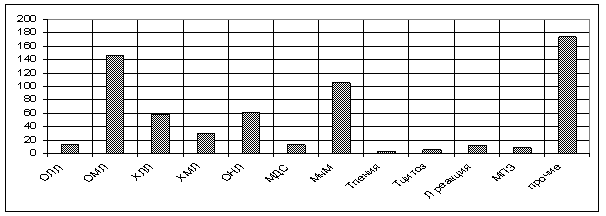
Рис. 5. Распределение анализов на миелограмму по нозологическим заболеваниям за 2015 г.
Острый лейкоз Хронический лимфолейкоз
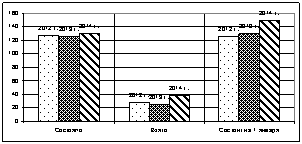
Хронический миелолейкоз Множественная миелома
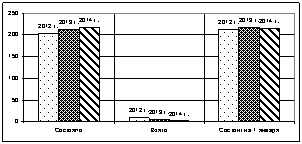
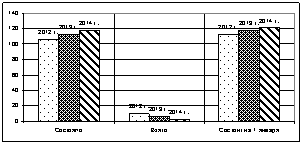
Первичный эритроцитоз В12 дефицитная анемия
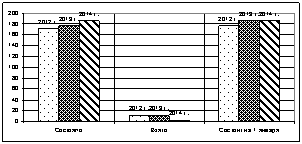
Тромбоцитопения Эритремия
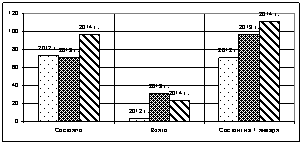
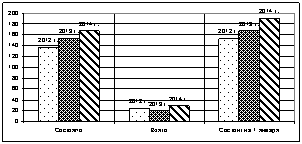
Рис. 6. Больные, состоящие на диспансерном учете по нозологическим заболеваниям за 2012–2014 гг.
В настоящее время биопсия костного мозга стала обязательным методом диагностики в гематологии, так как она позволяет принципиально оценивать тканевые соотношения в костном мозге, выявить гипоплазию/гиперплазию тех или иных клеточных серий, лейкозные инфильтраты, раковые метастазы и другие атипичные структуры, а также диагностировать отдельные виды костной патологии. На базе ЦКДЛ БУ РКБ налажена методика исследования костного мозга методом проточной цитометрии на цитометре FC-500. Наряду с этой методикой не теряет своей актуальности и подсчет миелограммы.
Выводы:
Исходя из данных за 2012–2014 годы отмечается увеличение количества гематологических больных, состоящих на «Д» учете на 13,8 %.
Число миелограмм за последние 3 года увеличилось на 10,9 %. При анализе подсчитанных миелограмм за 2015 год по возрастным категориям:
От 45–60 лет — 35,8 %
От 60–80 лет — 32,2 %
От 30–45 лет — 14,7 %
От 18–30 лет — 15,6 %
От 80 лет и старше — 1,7 %. Количество миелограмм, проведенных лицам женского и мужского пола, примерно одинаковое. По нозологическим заболеваниям — превалируют анализы по поводу миелолейкоза, острого недифференцированного лейкоза, а также миеломной болезни в совокупности с g-патиями.
Литература:
- «Гематологический атлас» С. А. Луговская, М. Е. Почтарь. Москва, 2011.
- «Руководство по гематологии» I том Л. Д. Гриншпун, П. А. Воробьев, С. К. Кравченко.
- «Анализы. Полный справочник. Москва, 2006 г. Г. Р. Колоколов, к.м.н. Е. В. Герасика, О. Л. Ананьев.







