В статье приведены материалы по изучению использования получения винилхлорида и хлоропрена из ацетилена и установлены некоторые кинетические закономерности процесса гидрохлорирования ацетилена, а также разработана технология осуществления процесса.
Совместный каталитический синтез винилхлорида и хлоропрена гидрохлорированием ацетилена является актуальной задачей синтетической органической химии.
Гидрохлорирование ацетилена проводили в реакторе, представлявшей собой трубку из нержавеющей стали с внутренним диаметром 12 мм и длиной 800 мм.
Жидкие и газообразные продукты синтеза подвергали газохроматографическому анализу с использованием пламенно-ионизационного детектора в следующих оптимальных условиях: Неподвижная фаза 15 %-ный лестосил на хроматоне N –AW с размером частиц 0,250–0,315 мм, стекляная колонка размером 2 х 0,004 м, температура термостата колонок от 40 до 1500 С с нагревом со скоростью 100С /мин, расход газа носителя- азота -30 мл/мин [3–4].
Качественный анализ продуктов проводили методом «свидетелей» и на основе структурно-групповых составляющих системы «сорбент-сорбат», а количественный–методом внутренней нормализации.
Каталитическую активность полученных образцов в реакции гидрохлорирования ацетилена определяли проточным методом.
Исследования по подбору катализатора проводили в стандартных условиях, характеризующихся следующими параметрами: температура 1650C, объёмное соотношение C2H2:HCl =1:1,1, величина объёмной скорости V=210 час-1. Исследованные катализаторы готовили «золь-гель» методом.
Наибольший выход винилхлорида получен при t=1650C. Повышение температуры по сравнению с оптимальной приводило к ухудшению показателей процесса. При этом уменьшается выход по винилхлориду и снижается селективность.
Влияние парциального давления ацетилена (
Всестороннее изучение кинетических закономерностей реакции гидрохлорирования ацетилена с хлористым водородом в присутствии разработанного катализатора в дифференциальном реакторе позволяет предложить следующую схему стадийного механизма этого процесса:
-
C2H2 +Z
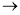 C2H2 ·Z
C2H2 ·Z
-
HCl + Z
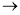 HCl · Z
HCl · Z
-
C2H2Z +C2H2Z
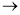 CH2 = CH— C
CH2 = CH— C 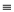 CH ·Z +Z
CH ·Z +Z
-
C2H2 ·Z +HCl·Z
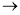 C2H3Cl·Z +Z
C2H3Cl·Z +Z
-
CH2 = CH –C
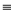 CH · Z + HCl ·Z
CH · Z + HCl ·Z 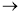 CH2 =CH –CCl = CH2·Z +Z
CH2 =CH –CCl = CH2·Z +Z
-
C2H3Cl ·Z
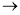 C2H3Cl +Z
C2H3Cl +Z
-
CH2 = CH— CCl =CH2 ·Z
 CH2 = CH— CCl = CH2 +Z
CH2 = CH— CCl = CH2 +Z
Z-активный центр катализатора.
Для интерпретации полученных экспериментальных данных необходимо было найти кинетическое уравнение, удовлетворяющее изменению параметров (скорость реакции, константа скорости реакции, адсорбционные коэффициенты и парциальные давления), в широком интервале.
На основе представлений о механизме реакции можно получить кинетическое уравнение, включающее в себя константы скоростей элементарных стадий и адсорбционные коэффициенты. Поскольку примяемые представления о механизме реакции основаны на предположениях, то в зависимости от вида выбранного механизма для одной реакции можно получить различные кинетические уравнения. После определения кинетических параметров этих уравнений можно судить о том, какое из них удовлетворяет экспериментальным данным.
Значения вычисленных для определенных кинетических констант и коэффициентов адсорбции использовались для определения скорости реакции образования винилхлорида с помощью различных кинетических уравнений.
Анализируя полученные и литературные данные, можно показать, что найденным закономерностям отвечает следующее кинетическое уравнение: 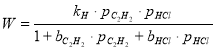
Таким образом, изучен жидкофазный процесс получения винилхлорида и хлоропрена из ацетилена и установлены некоторые кинетические закономер-ности процесса гидрохлорирования ацетилена, а также разработана технология осуществления процесса.
Литература:
- Козлова Г. А., Думина Р. С., Собержинова М.М// Кинетика и катализ. 1992. Т.33. № 3. С691.
- Хоанг Ким Бонг., Фомичева Т. В., Шестаков Г. К., Темкин О.Н// Журн Прикл. Химии. 1997. Т.20. № 11. С,1782.
- Хоанг Ким Бонг., Абанто Чавез Х. Й., Ныркова А. Н., Шестаков Г. К., Темкин О.Н// Журн. Прикл.химии.1998.. Т. 71. № 1. С.92.
- Файзуллаев Н. И., Мурадов К. М.// Хим. Пром-ть. 2004. Т.81. № 3. С. 136–138.







