Полимерлі фосфаттар ғылым мен техниканың түрлі салаларында кеңінен қолданылады. Бастапқы мономерлік фосфаттардың конденсациясы барысында әртүрлі дәрежедегі алмастырылу дәрежесіндегі тармақталған құрылымдар пайда болады, онда белгілі бір синтез жағдайында бөлшектердің әр түрлі өлшемдері бар тесіктер ұйымдастырылуы мүмкін. Нәтижесінде полимерлі, оның ішінде түрлі металдардың тотықтарымен түрлендірілген фосфаттар нано-, микро — және мезопордың реттелетін арақатынасы бар синтетикалық сорбенттерді алу үшін, сондай-ақ органикалық және бейорганикалық текті әртүрлі ластағыштарға іріктелуі үшін өте перспективалы қосылыстар болып табылады.
Ғылыми–техникалық әдебиеттің талдауынан көптеген бейорганикалық сорбенттердің құрамына фосфаттар, гидроксидтер, силикаттар немесе алюминий силикофосфаттары, сондай-ақ кальций кіреді. Кейбір ғылыми жұмыстарда [1–3] натрий, кальция силикополифосфаттар негізіндегі жүйеде тежегіш және сорбициялық қасиеттері бар кеуекті материалдардың алыну мүмкіндігі айтылған. Алайда, бұл өнімдер суда өте жоғары ерігіштікке ие, бұл оларды сорбент ретінде қолдануға мүмкіндік береді. Силикофосфатты қосылыстардың ерігіштігін төмендету үшін синтезделген силикополифосфаттардың құрамына ерігіш өнімдердің пайда болуына ықпал ететін қосылыстар енгізу қажет. Бұл тұрғыда ең перспективалы және қолжетімді алюминий тұздары болып табылады. Силикополифосфат материалдарын түрлі әдістермен, соның ішінде гидратталған монофосфаттарды термиялық поликонденсациялаумен алуға болады. Жоғары температуралы конденсация арқылы кристалды полифосфаттарды алу тәсілі.
Кесте 1
Химиялық құрамы мен температураға тәуелді үлгілердің салмақ жоғалтуы
|
Үлгі құрамы |
Cинтез температурасы, оС |
|||
|
200 |
300 |
400 |
500 |
|
|
Массаның жоғалуы, ∆m, салыс.% |
||||
|
Ca(H2PO4)2 Ca(H2PO4)2:Al(H2PO4)3=3:1 Ca(H2PO4)2:Al(H2PO4)3=1:1 Ca(H2PO4)2:Al(H2PO4)3=1:3 Al(H2PO4)3 |
0,15 0,18 0,21 0,26 0,34 |
0,20 0,34 0,30 0,25 0,37 |
0,41 0,41 0,42 0,44 0,59 |
0,45 0,45 0,63 0,52 0,49 |
Қатты фазадағы монофосфаттар қазіргі уақытта препараттық химияда да, өнеркәсіптік өндірісте да кең тараған болып табылады. Жалпы түрде термиялық поликонденсация процесін келесідей ұсынуға болады:
nH2PO4- → (PO3-)n+nH2O
Әдетте, кальций дигидромонофосфатының термиялық сусыздануының соңғы өнімі әртүрлі модификациялардағы — γ- Ca(PO3)2 және β — Ca(PO3)2 полифосфаттар болып табылатыны белгілі [4–5]. Ал Al(H2PO4)3 алюминий дигидрофосфатының термиялық поликонденсациясы кезең-кезеңмен жүзеге асырылады және құрамы дегидратация процесінің температурасымен анықталатын өнімдердің қоспасын алуға әкеледі [5]. Осылайша, 200–225оС температура аралығында қышқыл ди- және трифосфаттардан тұратын өнімдер қоспасы түзіледі: Al8H12(P2O7)9 және H2(AlP3O10). Температураның 450°С дейін көтерілуі алюминий Al(PO3)3 полифосфатының түзілуіне әкеледі, ол 450–500°С температура аралығында Al2P4O6 циклогексафосфатына өтеді. 600оС Al2P6O12алюминий тетрафосфат Al4(P4O12)3 цикліне ауысады. Осылайша, бастапқы жеке кальций дигидрофосфатын және алюминийді сусыздандыру соңғы өнімдері белгілі. Алайда, құрамында кальций, алюминий фосфаты және суда еритін силикаттар бар күрделі көп компонентті жүйелерде термиялық поликонденсация өнімдерінің молекулалық құрамы мен қасиеттері әдебиетте сипатталмаған. Осыған байланысты өнімдер «Ca(H2PO4)2-Al(H2PO4)3» және «Ca(H2PO4)2-Al(H2PO4)3-Na2O∙2,7SiO2» жүйелерінде 400–600о С температура аралығында синтезделді. Эксперимент барысында синтез кезінде бастапқы үлгілердің және олардың қоспаларының массасының жоғалуы анықталды. Нәтижелер кестеде берілген (1-сурет). Жоғарыда келтірілген деректерден қалай (1-кесте) кеуекті кальций-алюмополифосфатты сорбенттерді синтездеу кезіндегі су шығыны көбінесе аддитивті сипатта болады, бұл қоспа құрамының өзгеруі кезінде дегидратация процесі жылдамдығының елеулі өзгеруінің жоқтығын көрсетеді, яғни үлгілер массасының жоғалуы бойынша тәжірибелік деректер теориялық есептелген нәтижелермен сәйкес келеді.
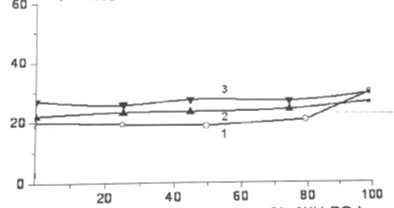 ∆m,сал.%
∆m,сал.%
Ca(H2PO4)2→mol% Al(H2PO4)3
Сурет 1. Құрамы мен температурасына байланысты кальций алюмофосфаттарын синтездеу кезінде массаның жоғалуы: 1–4000С; 2–5000С; 3– 6000С.
Жалпы алғанда аддитивтен шамалы ауытқулар, яғни теориялық эксперименттік мәндер эксперимент қателіктерімен байланысты және кальций мен алюминийдің бастапқы дигидромонофосфаттарын поликонденсациялау үдерістері механизмінің өзгеруін айқын көрсете алмайды. Сұйық шыны қоспаларының қатысуымен кальций дигидрофосфаты үшін массаның жоғалуының қисық өзгеруі, сондай-ақ термоөңдеу температурасының барлық диапазонында тікелей сызықтан іс жүзінде ауытқымайды. Термоөңдеу температурасының жоғарылауымен алюминий дигидрофосфаты үшін массаның жоғалуының қисық өзгеруі.
Алынған нәтижелер негізінде синтез барысында компоненттердің өзара реакциясының жүретіндігі дәлелденеді және одан әрі компоненттердің қасиеттеріне әсер ететін дегидратация өнімдерінің түзілуі мүмкін. Осылайша, «Ca(H2PO4)2-Al(H2PO4)3» жүйесінде синтез температурасы 400оС дейін болғанда, негізінен қышқыл кальций мен алюминийдің қышқылды ди-,үш- полифосфаттарынан тұратын өнімдер қоспасы түзіледі. Ал термоөңдеу температурасының өсуімен және сусыздандыру процесінің тереңдеуімен қышқыл сызықты полифосфаттар орта тұзға өтіп, жартылай циклденеді. Айтылған болжам ИК-спектроскопиялық және рентгенофазалық талдаулардың деректерімен расталды. Мысалы, Ca(H2PO4)2-Al(H2PO4)3 жүйесінде 400оС-та синтезделген өнімдердің ИҚ-спектрлерінде 458, 513, 736, 767, 1645 см-1 аймағында сіңіру жолақтары болады, мысалы Ca3H2(P2O7)2 кальцийдің қышқылды дифосфатына тән.
Термоөңдеу кезінде бастапқы компоненттердің калцияалюминийдің аралас фосфаттарының пайда болуымен өзара әрекеттесуі орын алады, бұл қоспаның бастапқы жеке компоненттерінің термоөңдеу өнімдерін сіңірудің негізгі жолақтарының ығысуы мен қарқындылығының өзгеруінде пайда болады. «Ca(H2PO4)2-Al(H2PO4)3» жүйесінде алынған үлгілердің дифрактограммалары Ca(H2PO4)2: Al(H2PO4)3=3:1 арақатынасында және 400оС температурасында да бастапқы компоненттердің кальций-алюминийдің қышқыл фосфаттарының түзілуімен өзара әрекеттесуімен дәлелденеді, сонымен қатар жаңа рефлекстер пайда болады. Сондай-ақ, термоөңдеу өнімдері аморфты қоспалар екенін атап өткен жөн. Термоөңдеу температурасының өсуімен қышқыл фосфаттар өзінің құрылымдық-байланысқан суын жоғалтады. Жүйенің фосфатты компоненттерінің бірін сұйық шынымен ауыстырып, натрий силикаты құрамын ұлғайтқанда және синтез температурасын жоғарылатқанымызда, жүйеле кристалдық поликонденсация өнімдерінің дәрежесі артатыны анықталды.
Әдебиет:
- Жусупова Л. А., Тапалова А. С., Джусипбеков У. Ж., Фишбейн О. Ю. Синтез и свойства кристаллических силикополифосфатов кальция // Проблемы химической технологии неорганических, органических, силикатных и строительных материалов и подготовки инженерных кадров: сб. тр. Междунар. научно-практ. конф. — Шымкент, 2002. — Т. 2. — С. 35–39.
- Жусупова Л. А., Жакитова Г. У., Джусипбеков У. Ж. Переработка фосфорных шлаков на сорбенты для очистки производственных вод от нефтепродуктов // Сб. тез. докл. научно-практ. конф. По актуальным вопросам химизации сельского хозяйства. -Ташкент, 2002. — С. 109.
- Жусупова Л. А., Капралова В. И., Жакитова Г. У., Губайдуллина Г. М. Исследование ингибирующих свойств растворимых продуктов поликонденсаций системы «Ca(H2PO4)2- NaH2PO4- Na2O∙mSiO2» // Изв. НТО «Кахак». — 2003. — № 2 (9). — С. 44–48.
- Кузьменков М. И., Плышевский С. В., Печковский В. В. и др. Разработка технологии производства метафосфата алюминия // Химическая промышленность. — 2004. — № 10. — С. 595–597.
- Капралова В. И. Коррозионная стойкость металлов в водных растворах с добавками растворимых силикофосфатов // Высокие технологии-залог устойчивого развития. Тр. Межд. научн конф. — Алматы, КазНТУ, 20137 — Т. 27. — С. 100–103.







