В статье приведен ретроспективный анализ историй развития новорожденных, получавших антибактериальную терапию в условиях отделении реанимации и интенсивной терапии и патологии новорожденных. Учитывали обоснованность назначения препаратов, безопасность, наличие доказательной базы. По результатам отображены основные принципы назначения антибактериальной терапии новорожденных и ее рациональность. Указаны возможные тактические ошибки при смене препаратов, в связи с чем даны рекомендации.
Ключевые слова: антибактериальная терапия, новорожденные, инфекционные заболевания, ОРИТН, ОПН.
Актуальность: Несмотря на значимые достижения в неонатологии, роль инфекционно-воспалительного процесса в структуре заболеваемости новорожденных не уменьшается. Согласно проведенным эмпирическим исследованиям, на разных этапах выхаживания новорожденных в структуре заболеваний, инфекционно-воспалительные заболевания встречаются у 50–60 % новорожденных, в том числе и у недоношенных [1]. Успех лечения тяжело протекающих бактериальных инфекций во многом зависит от своевременной и рациональной антибактериальной терапии.
Антибиотикотерапия новорожденных в первую очередь требует обоснованного назначения и строгого соблюдения алгоритма рациональной антибактериальной терапии, исходя из результатов микробиологии, клинической фармакологии [2]. Длительная и нецелесообразная терапия только увеличивает риск развития НЭК и позднего неонатального сепсиса, значительно увеличивает стоимость лечения новорожденных и способствует формированию резистентной микрофлоры. Чрезмерное назначение антибактериальных препаратов в акушерских стационарах связано с затруднением выявления возбудителя, неспецифичность клинических проявлений воспалительного процесса, что приводит к гипердиагностике внутриутробных инфекции и к трудности верификации госпитальной инфекции [3].
Цель исследования: Целью данного исследования является оценка обоснованности и адекватности антибактериальной терапии новорожденных в условиях Отделения реанимации и интенсивной терапии (ОРИТН) и Отделения патологии новорожденных (ОПН) ЦП и ДКХ г.Алматы.
Материалы иметоды исследования: Исследование проводилось путем ретроспективного анализа медицинской документации на базе ЦП и ДКХ г.Алматы, отделении реанимации и интенсивной терапии новорожденных и патологии новорожденных. Было включено 203 новорожденных, поступивших с октября по декабрь 2018г., из них выбраны 94 историй развития новорожденных, в качестве окончательного диагноза которых, было указано то или иное инфекционно-воспалительное заболевание (ИВЗ) с проведением антибактериальной терапии.
При анализе назначения антибактериальной терапии учитывали:
− наличие доказательной базы препарата при данной нозологической форме; специфичность действия, т. е. соответствие антимикробного спектра активности предполагаемого или идентифицированного возбудителя инфекционного процесса;
− сведения о существующей микробной резистентности;
− особенности возрастной фармакокинетики и фармакодинамики;
− •безопасность (нежелательные побочные эффекты, реакции лекарственного взаимодействия);
− назначение препаратов не по показаниям (off label);
Проведено анонимное анкетирование лечащих врачей отделений ОРИТН и ОПН, с целью определения тактики применения антибиотиков. При оценке терапии неонатологи опирались на инструкции по применению препарата, формулярную информацию и клинические рекомендации ВОЗ, клинические протоколы МЗ РК, руководства по антибактериальной терапии и алгоритмы международных стандартов.
Результаты исследования: По результатам, у всех новорожденных в качестве стартового курса антибактериальной терапии использовали сочетание препаратов пенициллинового ряда широкого спектра действия (ампициллин) и аминогликозидов (гентамицин). Однако, учитывая только клинико-лабораторные данные, на третий день жизни пенициллиновая группа широкого спектра, была заменена без показаний и без результата бактериологического посева, на цефалоспорины III поколения (у 32 детей — 34,0 %).Перечень антибиотиков, применяемых в условиях ОРИТН и ОПН представлен в таблице 1.
Таблица 1
Перечень антибиотиков
|
Цефтриаксон +Гентамицин; |
21 % |
|
Меропенем + Ванкоген; |
5 % |
|
Ванкоген; |
9 % |
|
Меропенем; |
1 % |
|
Метрид; Цефтриаксон; Метрид + пенициллин + меропенем; |
8 % |
|
Ампициллин + Гентамицин; |
56 % |
Вместо цефалоспоринов I поколения в подавляющем большинстве случаев при смене антибиотиков были назначены цефалоспорины III поколения — цефтриаксон (37,5 %), связи с отсутствием в октябре цефазолина (5,5 %) что является нарушением алгоритма антибактериальной терапии новорожденных.
Комбинации гликопептидов (ванкоген) с карбапенемами (меропенем) 8,3 % в среднем, с цефалоспоринами до 8,7 % случаев.
Один случай (1,0 %) использования сочетания метронидазола, карбапенема и пенициллина: высеян злостный возбудитель Leuconostoc mesenteroides ssp cremoris — резистентной флоры, что является результатом длительной и беспорядочной антибактериальной терапии у мамы при беременности. Основным показанием к назначению гликопептидов и карбапенемов была неэффективность лечения бактериальной инфекции у новорожденных из группы высокого риска по реализации бактериальной инфекции (ОАГА).
Выбор эмпирической антибактериальной терапии основывался на анализе результатов бактериологического мониторинга, проведенного в ОРИТН и ОПН и определении возбудителей при взятии смывов из зева, слизистой полости рта и интубационной трубки. По результатам смывов чаще всего высевали Klebsiella pneumonia (7,5 %), St. haemoliticus (в 4,1 % случаев), St.hominiss (1,0 %) и один случай E.coli (1,0 %)
Курс антибиотикотерапии (до 7 дней) использовали у 47,8 % новорожденных >7 дней — у 52,2 %; максимальная продолжительность курса составила 17 дней (ванкоген).
Один курс антибиотиков получили 50 новорожденных (53,1 %), 44 новорожденных от 2 до 4 курсов (46,8 %).
Выводы: При определении показаний к стартовой антибиотикотерапии в основном превалируют лишь факторы риска внутриутробного инфицирования, не нозологические формы, что не соответствует алгоритму антибактериальной терапии новорожденных и клиническим протоколам МЗ РК. Были случаи профилактического назначения антибактериальных препаратов (АБП) новорожденным при катетеризации центральных сосудов, проведении искусственной вентиляции легких (ИВЛ), мекониальной аспирации, без проявления симптомов инфекции у новорожденного, что не рекомендуется многоцентровыми исследованиями. Результаты бактериальных посевов на флору и чувствительность антибиотиков в ОРИТН И ОПН из лаборатории бывают готовыми не раннее 7–10 суток, вследствие чего повторна смена антибиотиков проводится без учета чувствительности к ним, без консультации клинического фармаколога.
Анализ медицинской документации позволил установить несвоевременный контроль диагностики (выделение возбудителя — есть или нет рост возбудителя через 48часов) лечащими врачами, включая контроль за соблюдением сроков микробиологического исследования. Проводится ранняя смена стартовой терапии на цефалоспорины III поколения (на 3-и сутки) при стабильной динамике состояний новорожденных, без бактериологического посева, лишь по общему анализу крови (ОАК) и С-реактивной белок (С-реактивный белок (СРБ) не является специфическим маркером инфекции).
Нет систематизированного подхода к антибиотикотерапии при различных нестандартных ситуациях (при нормальной лейкограмме и наличии высоких показателей СРБ с нормальным показателем повторного определения СРБ, отсутствие клиники ИВЗ с умеренными показателями ОАК и СРБ, пребывание новорожденных на ИВЛ без уточненных диагнозов ИВЗ, наличие у новорожденных мекониальной аспирации без подтверждения аспирационной пневмонии лабораторными данными и рентгенологической картины и т. д.)
Были установлены тактические ошибки: необоснованное назначение антибактериальной терапии отмечено в 18,6 % случаев, нерациональная смена антибактериальной терапии — в 9,9 %, необоснованная длительность курса — в 9,3 % (рисунок 1)
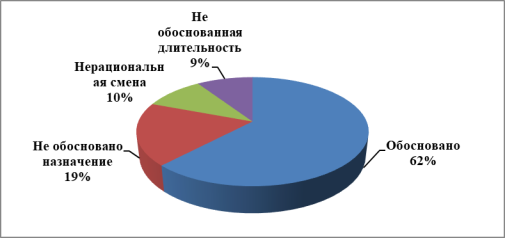
Рис. 1. Обоснованность назначения антибактериальных препаратов
Результаты исследования подтвердили актуальность соблюдения основных принципов рационального назначения антибактериальной терапии новорожденным. Выбор антибактериальной терапии должен основываться исходя из локализации инфекционного процесса (эмпирическая терапия) и наличия данных о виде выделенного и идентифицированного патогенного микроорганизма (целевая/целенаправленная терапия), предполагаемого диагноза ИВЗ. Нерациональная эмпирическая антибактериальная терапия у новорожденных повышает риск летальности в 1,5 раза. Длительная эмпирическая терапия повышает риск некротизирующего энтероколита и смерти у новорожденных с очень низкой массой тела.
Безусловно, назначение антибиотиков в неонатологической практике в каждом случае зависит от наличия теоретических знаний, клинического мышления и опыта врача. Однако на современном этапе медицина должна быть основана на доказательных данных, что определяет необходимость создания протоколов и практических руководств, которые должны базироваться на особенностях каждого лечебного учреждения.
Практические рекомендации: При антибиотикотерапии инфекционно-воспалительных заболеваний новорожденных основными принципами должны быть обоснованность и правильный выбор антибиотика, исходя из установленных диагнозов ИВЗ, локализации инфекционного процесса и наличия данных выделенного, идентифицированного патогенного микроорганизма, т. е. терапия должна быть этиотропной.
В ОРИТН и ОПН должны быть протоколы тактики антибиотикотерапии с учетом профиля, специфических особенностей лечебно-профилактического процесса, подбор антибиотиков с учетом предыдущего опыта микробиологического мониторинга у пациентов данного отделения, финансовых и материальных ресурсов.
Литература:
- Капура Н. Г., Гнедько Т. В., Печкурова О. Н. «Анализ эффективности антибактериальной терапии у новорожденных с перинатальными инфекциями» Современные перинатальные медицинские технологии в решении проблем демографической безопасности: сб. науч. тр. / ред.кол.: К. У. Вильчук. — Минск: ГУ РНМБ, 2011. — 242c.
- Заячникова, Н. В. Деларю, А. В. Чебаткова «Алгоритм стартовой антибактериальной терапии при заболеваниях у новорожденных», Вестник ВолгГМУ, выпуск № 4 (52) — 2014г., стр. 51–55.
- Patel SJ, Saiman L. «»Principles and strategies of antimicrobial stewardship in the neonatal intensive care unit» Semin Perinatol. 2012 December; 36(6): 431–436







