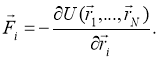Цель данной статьи — исследование образования пор в DPPC-мембране, используя силовое поле Martini.
Ключевые слова: DPPC-мембрана, силовое поле Martini, метод молекулярной динамики, электрическое поле.
Введение
Изучению биологических мембран посвящено множество работ. Одной из важнейших функций биологических мембран является транспорт вещества сквозь мембрану. Исследования липидов PE и PC, показывают, что молекулы PE могут образовывать внутри- и межмолекулярные связи, в том числе совместно с другими типами липидов, где группа амина (водород-донор) может сильно взаимодействовать с фосфатными / карбонильными группами или водой (водородно-акцепторной). Эти сильные межмолекулярные взаимодействия приводят к увеличению температуры фазового перехода жидкость — кристалл, тем самым влияя на проницаемость мембраны, устойчивость и другие биологические свойства, как правило, связанные с функциональной работой внутренних клеточных органелл. Все эти аспекты исследования липидов становятся очень привлекательными, с точки зрения мембранной организации и функциональных возможностей, в частности, в структурных и динамических свойствах [1–3]. Полагается, что приложение внешнего электрического поля способствует образованию поры в мембранной структуре.
Поры в мембранах, образованные благодаря электрическому полю, могут стать предметом для исследования, такой процесс называется электропорацией. Электропорация обычно используется в молекулярной биологии и биотехнологии и недавно нашла применение в медицине, изучался транспорт лекарственных средств через мембрану [4–5].
Методы
Дипальмитоилфосфатидилхолин (DPPC) — фосфолипид из группы насыщенных фосфатидилхолинов, один из главных компонентов лёгочного сурфактанта. Данный липид часто используется в моделях билогических мембран [6]. Липид обычно состоит из полярной головки и липидного хвоста [7]. Схематическое изображение липидного бислоя представлено на рисунке (1):
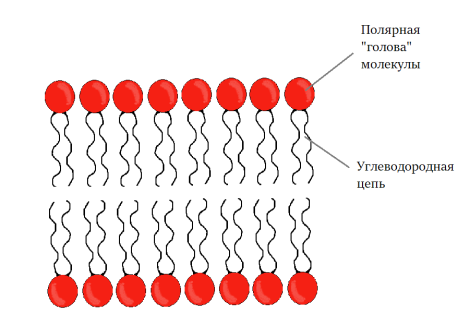
Рис. 1. Схема липидного бислоя
При приложении электрического поля вдоль мембраны, мембрана деформируется, в мембране образуются поры [8].
Расчет процессов в мембранах производится с помощью метода молекулярной динамики (МД). В основе метода МД представлена модель многоатомной молекулярной системы, в которой все атомы представлены материальными точками, движение которых описывает уравнение Ньютона. Таким образом, имеется система, состоящая из N точечных частиц, каждая из которых имеет массу, скорость и радиус-вектор ![]() .
.
Численное решение системы классических уравнений движения:
|
|
(1) |
где ![]() — масса i-ой частицы, N — число частиц. Левая часть уравнения (1), есть произведение массы на ускорение, где:
— масса i-ой частицы, N — число частиц. Левая часть уравнения (1), есть произведение массы на ускорение, где:
|
|
(2) |
Уравнение (1) есть не что иное, как представление второго закона Ньютона, для системы, состоящей из N числа частиц.
Граничные условия системы задаются уравнениями (3):
|
|
(3) |
Свойства системы определяются выбором потенциала:
|
|
(4) |
Рассмотрим поведение при постепенном сближении двух частиц. На очень большом расстоянии частицы не взаимодействуют. По мере сближения частиц между ними возникает сила притяжения. Она постепенно увеличивается и достигает некоторого максимального значения, а затем частицы начинают отталкиваться друг от друга.
Таким образом, получаем, что зависимость энергии взаимодействия между частицами от расстояния r, аналогично кривой потенциальной энергии двух молекул. Каждой точке потенциальной кривой соответствует потенциальная энергия неподвижной системы из двух частиц, находящихся на расстоянии r друг от друга.
Электрическое поле ![]() в системе не эквивалентно приложенному полю, а рассчитывается из соображений:
в системе не эквивалентно приложенному полю, а рассчитывается из соображений:
![]() , (5)
, (5)
где
Молекулярно-динамическое моделирование
Для моделирования мембраны выбрано силовое поле martini22p, полярные аминокислоты Martini 2.2, липиды Martini 2.0 и поляризуемая вода. Количество липидов 512 (256 липидов на каждый слой), имеется водяной слой с обеих сторон мембраны.
Создавался файл равновесия, в котором мембрана приводилась к состоянию равновесия (рисунок 2).

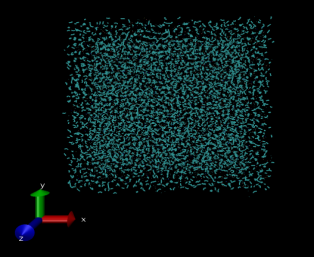
Рис. 2. Бислой липидов DPPC
Бислой мембраны DPPC окружен молекулами воды.
Затем вдоль оси z (поперек) мембраны было приложено электрическое поле E=0,3 B/нм. Время моделирования системы 300 нс. Динамика поведения DPPC мембраны под действием электрического поля представлена на рисунке 3.

Рис. 3 Динамика подвижности DPPC липидов под действием электрического поля
Полости, которые представлены на рисунке 3, заполнены молекулами воды, для рассмотрения полостей, образованных за счет электрического поля, мы удалили молекулы воды на изображении.
Заключение
В исследовании была построена модель двухслойной мембраны DPPC по 256 липидов на каждый слой, окруженная молекулами воды. Было выбрано силовое поле martini22p.
Исследования показали, что при приложении внешнего электрического поля вдоль мембраны, образуются поры, сквозь которые могут диффундировать молекулы воды. Липидные головки под действием электрического поля находятся в движении, то есть они не имеют жесткую структуру, в которой находились бы статично на протяжении всего времени моделирования.
Рисунок 3 показывает, что в различные моменты времени липиды принимают различное положение. Исследование по данной тематике будет продолжено, планируется рассмотреть поведение мембраны при различных напряженностях поля и временах моделирования.
Литература:
- L. Sukit, K. S. Amadeu. Molecular Simulation Study of Structural and Dynamic Properties of Mixed DPPC/DPPE Bilayers // Biophys. J. — 2009. — V. 90. — C. 3951–3965.
- R. Jahn, H. Grubmu. Membrane fusion // Curr. Opin. Cell Biol. — 2002. — 14: C. 488–495.
- M. Dyck, P. Kruger, M. Losche. Headgroup organization and hydration of methylated phosphatidylethanolamines in Langmuir monolayers // Phys. Chem. Chem. Phys.- 2005. — 7. — C. 150–156.
- M. Tarek. Membrane Electroporation: A Molecular Dynamics Simulation // Biophys. J. — 2005. — V. 88. — C. 4045–4053.
- T. J. Lewis. A model for bilayer membrane electroporation based on resultant electromechanical stress // IEEE Trans. Dielec. Elec. Insul.- 2003. — 10. — C. 769–777.
- Y. Qianqian, S. Xinyuan, D. Haiou, D. Xingxing, W. Guang, O. Yanjiang. Interactions of Borneol with DPPC Phospholipid Membranes: A Molecular Dynamics Simulation Study // Int. J. Mol. Sci. — 2014. — 15. — C. 20365–20381.
- G. F. Chen, Y. Y. Chen,, N. N. Yang,, X. J. Zhu, L. Z. Sun, G. X. Li. Study of the interaction between curcumin and mimetic biomembrane // Sci. China Life Sci. — 2012. — 55. — C. 527–532.
- C. A. López, Z. Sovova, F.J. van Eerden, S. J. Marrink. Martini force field parameters for glycolipids // J. Chem. Theory Comput. 2013, 9, 1694–1708.