Впервые бактерии были обнаружены голландским натуралистом Антони ван Левенгуком в 1676 году при помощи микроскопа. На основе данного открытия была создана микробная теория инфекционных заболеваний, которую доказали Луи Пастер и Роберт Кох.
После ученые стали активно искать способ борьбы с патогенными микроорганизмами. Это удалось британскому бактериологу Александру Флемингу, который в 1928 году выделил пенициллин. Позднее химики разработали полусинтетические антибиотики, научились улучшать и усиливать их свойства. XX век ознаменовался победой над микробами. Но тем не менее, согласно данным ВОЗ, патогенные бактерии — одна из основных причин смертности в современном мире.
В чем же дело? Почему сильнейшие лекарства вдруг становятся бесполезными?
Дело в том что, микроорганизмы – древнейшая форма существования жизни на Земле, что говорит об их высокой адаптационной способности. Вследствие чрезмерного и, довольно часто, неоправданного употребления антибиотиков, происходит все больше мутаций, и как результат – возникновение новых штаммов бактерий, невосприимчивых к лекарствам. Это называется резистентностью.
Механизмы резистентности
Антибиотик уничтожает бактерию следующими путями:
– нарушает целостность мембраны паразита;
– нарушает синтез белка;
– нарушает синтез нуклеиновых кислот;
– ингибирует работу дыхательных ферментов;
– нарушает синтез клеточной стенки.
Следовательно, основные механизмы резистентности это:
− Изменение строения мембраны
То есть мутирует рецепторный белок на поверхности мембраны, в результате антибиотик не может «прикрепиться» и разрушить ее;
− Эффлюксные насосы
Антибиотик, который проникает в клетку бактерии, активно ею же и «выкачивается», из-за чего лекарство не может достигнуть необходимой концентрации и уничтожить микроорганизм;
− Пенициллазы
Бактерия синтезирует ферменты пенициллазы, которые могут расщеплять антибиотики, за синтез данных белков ответствен ген blaNDM-1;
− Грамотрицательные патогены
Формирование дополнительной мембраны поверх клеточной стенки бактерии, что обеспечивает повышение устойчивости ко внешним факторам;
− Гены ermB и mef
Обеспечивают устойчивость к макролидам – препаратам, нарушающим синтез белка в бактерии.
Подобные мутации возникают из-за чрезмерного использования антибиотиков, часто даже без необходимости. Также это случается из-за неполного прохождения курса, назначенного врачом, вследствие бактерии получают воздействие лекарственного средства, но не уничтожаются, а лишь ослабевают, мутируют и становятся устойчивыми к данному препарату.
Современные разработки новых методов борьбы с бактериями
На данный момент ученые находятся в поиске организмов – продуцентов новых антибиотиков.
Спектр поиска расширился от низших до высших грибов, растений, а также животных. Исследуются соединения, образованные древоразрушающими видами грибов: омфалотусом – Omphalotus olearius, вешенкой – Pleurotus ostreatus, серно-желтым трутовиком – Laetiporus sulphureus, дубовой губкой – Daedalea quercina). Особое внимание направлено на черных муравьев-древоточцев. Они обустраивают свое жилище, проделывая ходы в пнях и отмерших деревьях. Насекомые измельчают древесину, а бактерии ее разлагают. Но каким-то образом муравьи контролируют этот процесс и не позволяют микроорганизмам полностью разрушить свой будущий дом. Оказалось, что они выделяют антибиотик нибомицин. Согласно исследованиям, он способен подавлять рост колоний самого устойчивого патогена- золотистого стафилококка (Staphylococcus aureus).
Ученые ищут также и принципиально новые методы борьбы с резистентными бактериями. В Дании научились определять наличие в мембране бактерий специфичных транспортных белков. Транспортные белки необходимы для проведения внутрь клетки определенных веществ и ионов. Зная, какие соединения бактерия может продуцировать сама, а какие должна получать извне, можно создать эффективные антибиотики узкой направленности. К примеру, стало известно, что возбудитель гастрита и язв двенадцатиперстной кишки- Helicobacter pylori, нуждается в витамине B1 для поддержания нормальной жизнедеятельности, при этом сама синтезировать его не может. Идет разработка препарата, который будет ослаблять или уничтожать транспортный белок, ответственный за захват витамина.
Следующее перспективное направление- изучение бактериофага.
Бактериофаг — вирус, поражающий бактериальные клетки, является облигатным внутриклеточным паразитом. Имеет своеобразное сложное строение, которое позволило проникать через ригидную клеточную стенку жертвы.
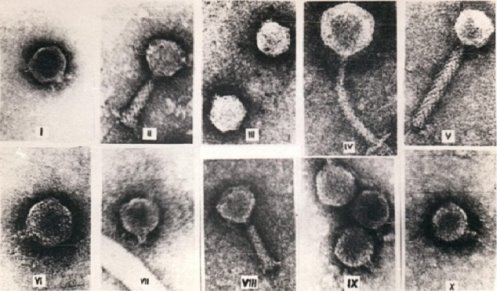
Рис.1. Различные варианты строения бактериофага
Выделяют умеренные и вирулентные фаги. Умеренные фаги проникают в клетку и взаимодействуют с геномом хозяина. В результате синтез белка паразита происходит синхронно с синтезом белка бактерии. Вирулентные фаги нарушают синтез ДНК, РНК и белков хозяина, осуществляют синтез собственного протеина при помощи его рибосом. Далее происходит лизис клетки, и паразит выходит. Преимуществом в этом методе является то, что бактерии хоть и видоизменяются, приобретая иммунитет к паразитам, но бактериофаги, будучи живыми существами, тоже приспосабливаются и при помощи точечных мутаций способны поражать простейших вновь и вновь.
Единственная проблема заключается в том, что вирус способен поражать не все штаммы бактерий. Но над этим идет работа, ученые увеличивают спектр их действия при помощи генной инженерии.
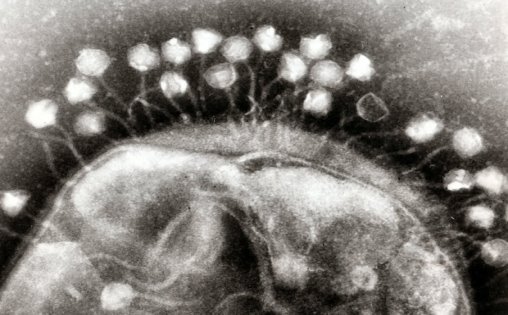
Рис. 2. Бактерия, пораженная фагами
Заключение
Таким образом, в современной медицине остро стоит проблема резистентности бактерий. Для ее решения необходимы разработки принципиально новых методов борьбы с ними. Однако очень важными являются и просветительные работы с пациентами, ограничение продажи антибиотиков.
Литература:
- Студенческая библиотека (Электронный ресурс). Режим доступа- https://students-library.com/library/read/29861-mehanizmy-dejstvia-antibiotikov
- The National Center for Biotechnology Information advances science and health by providing access to biomedical and genomic information (Электронный ресурс). Режим доступа-https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3414030/
- Блог Massmedica (Электронный ресурс). Режим доступа- https://massmedika.in.ua/b-lactamic-resistance-mechanism/
- https://www.sciencedirect.com/science/article/pii/S0300908419300495?via=ihub
- American Journal of Therapeutics (Электронный ресурс). Режим доступа https://journals.lww.com/americantherapeutics/Abstract/2017/05000/Antimicrobial_Resistant_Streptococcus_pneumoniae__.15.aspx







