В настоящее время лечение и предупреждение когнитивных нарушений и нейродегенеративных болезней представляет интерес для научного сообщества, поскольку заболеваемость ими неуклонно растет. О терапевтическом применении препаратов солей лития для лечения биполярных расстройств и депрессий известно более полувека. Недавние исследования показали наличие у солей лития нейропротекторного действия, которое основано на способности лития модулировать сразу несколько метаболических процессов в головном мозге: обмен нейротрофического фактора, окислительный стресс, воспаление и функциональная активность митохондрий. Существенный потенциал применения препаратов лития в неврологии обусловлен преимущественным накоплением лития в нервной ткани (в частности, в лобной коре) [1].
Материалы и методы
Исследование проведено на 90 белых крысах массой 200–250 г. Животных содержали в стандартных условиях вивария при естественной суточной смене день/ночь. Содержание животных соответствовало правилам лабораторной практики и Приказу МЗ и СР РФ от 23 августа 2010 г. № 708 н «Об утверждении Правил лабораторной практики». В эксперименте животные случайным образом разделены на 9 групп: I — VIII группы — животные (n=10) получавшие лития цитрат per os (из расчета 1 мг Li/кг однократно); IX группа — (контрольная) — животные (n = 10), не получавшие никаких солей лития. Цитрат лития производства DSM Nutritional Products AG (Швейцария).
Для определения уровней лития были получены гомогенаты тканей исследованных биосубстратов. При проведении масс-спектрометрии, в качестве внутреннего стандарта в растворы вводили индий в концентрации 25 мкг/л. Калибровочные растворы были приготовлены из стандартных растворов фирмы VTRC с известным содержанием в диапазоне от 5–1000 мгк/л (10–7 %). Полученные растворы анализировались на масс-спектрометре с ионизацией в индуктивно-связанной плазме «Plasma Quad PQ2 Turbo» (VG Elemental, Англия). Проводилось от 3 до 10 экспозиций каждого образца, время интегрирования сигнала составило 60 сек. В ходе настоящего анализа был использован метод фармакокинетического анализа с использованием электронных таблиц Excel, дополненного модулями программного пакета PKSolver [2].
Результаты
Бескамерный анализ позволяет охарактеризовать повсеместно используемые фармакокинетические параметры соединения как максимальная концентрация лития в биосубстрате (Cmax), время достижения максимальной концентрации (tmax), последняя измеренная концентрация лития (Clast), площадь под кривой (AUCt), среднее время удержания (MRTt), наклон участка финального выведения (Lz), период полувыведения (T1/2), клиренс (CL).
В результате проведения фармакокинетического эксперимента были получены зависимости концентраций от времени для цельной крови и гомогенатов различных органов.
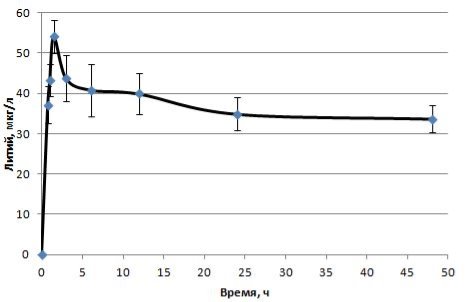
Рис. 1. Фармакокинетическая кривая содержания лития в цельной крови
Визуальный анализ фармакокинетической кривой (Рисунок 1) показывает, что Cmax в цельной крови после его введения per os крысам в дозе 1 мг/кг достигает через 1,5 часа (tmax) и составляет 54,11 мкг/л. Lz, составляет 0,0048 1/ч. T1/2 цитрата лития после его введения per os составляет 145,86 ч.
Низкое значение Lz и высокое значение T1/2 указывает на поддержание стабильных концентраций иона лития в цельной крови.
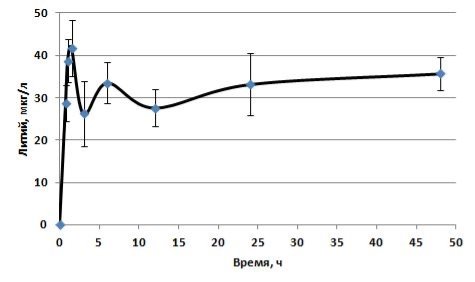
Рис. 2. Фармакокинетическая кривая содержания лития в гомогенате головного мозга
Cmax после его введения per os крысам в дозе 1 мг/кг достигает через 1,5 часа (tmax) и составляет 41,77 мкг/л. CL составил 0,0044 л/(час) после введения per os в дозе 1 мг/кг. Lz составляет 0,0012 1/ч. T1/2 цитрата лития после его введения per os составляет 602,62 ч (Рисунок 2).
Характерное низкое значение Lz, высокое значение T1/2 и наиболее низкое значение CL именно для этого биосубстрата свидетельствует о накоплении иона лития в головном мозге крыс.
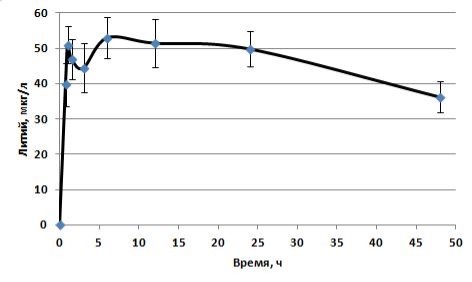
Рис. 3. Фармакокинетическая кривая содержания лития в гомогенате лобной доли головного мозга
При анализе фармакокинетической кривой (Рисунок 3) мы видим, что Cmax цитрата лития в лобной доле головного мозга после его введения per os крысам в дозе 1 мг/кг достигает через 6 часов (tmax) и составляет 52,98 мкг/л.
Clast составила 36,23 мкг/л. MRT после введения per os составило 22,32 часа. AUCt составила 2230,21 мкг/л*ч.
При анализе результатов мы видим, что литий накапливается в лобной доле, Clast=36,23 мкг/л — одно из самых высоких значений концентрации. Этот вывод подтверждает и AUCt, для лобной доли оно составило 2230 мкг/л*ч. MRT также было достаточно высоким — 22,23 часа, выше, чем у других биосубстратов.
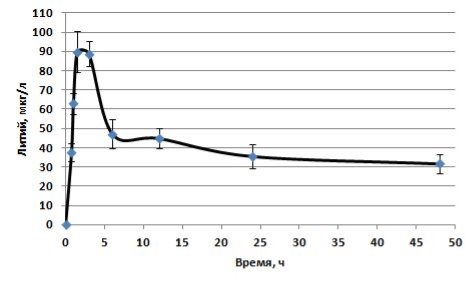
Рис. 4. Фармакокинетическая кривая содержания лития в гомогенате печени
Анализ фармакокинетической кривой (Рисунок 4) показывает, что Cmax после его введения per os крысам в дозе 1 мг/кг достигает через 1,5 часа (tmax) и составляет 89,83 мкг/л.
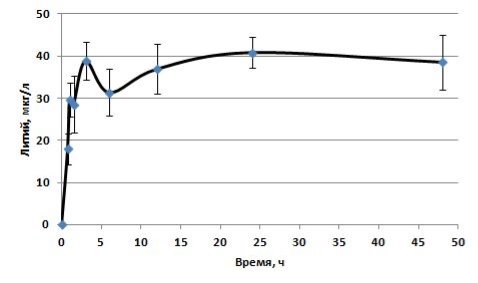
Рис. 5. Фармакокинетическая кривая содержания лития в гомогенате бедренной кости
Визуальный анализ фармакокинетической кривой показывает (Рисунок 5), что Cmax цитрата лития в бедренной кости после его введения per os крысам в дозе 1 мг/кг достигает через 24,0 часа (tmax) и составляет 40,79 мкг/л. CL составил 0,0026 л/(час) после введения per os в дозе 1 мг/кг. Lz, составляет 0,0008 1/ч. T1/2 цитрата лития после его введения per os составляет 916,90 ч.
Полученные в рамках бескамерного анализа значения фармакокинетических параметров цитрата лития подтверждают сделанные выше выводы:
– tmax составило 1–1,5 ч для большинства биосубстратов, кроме селезёнки, аорты, надпочечников, лёгких и бедренной кости, в которых tmax составило 12–24 ч.;
– низкое значение наклона участка финального выведения (Lz) и высокое значение периода полувыведения (Т1/2) были характерны для всех биосубстратов, особенно для цельной крови (Lz=0,005 1/ч, Т1/2=146 ч), головного мозга (Lz=0,001 1/ч, Т1/2=602 ч), почек (Lz=0,0006 1/ч, Т1/2=1143 ч) и бедренной кости (Lz=0,0008 1/ч, Т1/2=918 ч);
– накопление лития в головном мозге и в кости подтверждается наиболее низкими значениями клиренса именно для этих биосубстратов (головной мозг — CL=0,004 л/ч; бедренная кость — CL=0,0026 л/ч);
– цитрат лития способствует поддержанию стабильных концентраций иона лития в цельной крови и в головном мозге, что важно для осуществления профилактического и терапевтического потенциала лития.
Литература:
- Пронин А. В., Громова О. А., Торшин И. Ю., Гоголева И. В., Жидоморов Н. Ю., Сардарян И. С., Волков А. Ю. Доклиническое изучение фармакокинетики аскорбата лития. Фармакокинетика и фармакодинамика. 2016. № 2. С. 18–25.
- Ferreira, A. J. M. (2009). MATLAB Codes for Finite Element Analysis. Springer. ISBN 978–1-4020–9199–5.







