В статье рассмотрена кинетика конденсации трет-бутанола с формальдегидом в присутствии ортофосфорной кислоты и углеродных нанотрубок. Рассчитаны значения констант скоростей расходования формальдегида и накопления 4,4-диметил-1,3-диоксана.
Ключевые слова: формальдегид, трет-бутанол, 4,4-диметил-1,3-диоксан, углеродные нанотрубки, селективность, реакция Принса.
Одним из основных способов получения изопрена является диоксановый метод [1], включающий термокаталитическое разложение 4,4-диметил-1,3-диоксана (ДМД), который, в свою очередь, получают взаимодействием изобутилена или трет-бутанола и формальдегида по реакции Принса в присутствии ортофосфорной кислоты [1]. Однако, указанный метод синтеза изопрена имеет существенный недостаток: наряду с ДМД, наблюдается образование побочных продуктов — гидрированных пиранов, диолов (до 30 % масс.).
В связи с этим, целью представленной работы являлось выявление эффективности углеродных нанотрубок для увеличения селективности образования 4,4-диметил-1,3-диоксана (ДМД) при взаимодействия трет-бутанола с формальдегидом в условиях реакции Принса.
Реакцию проводили в присутствии 5 % масс. фосфорной кислоты и 5 % масс. углеродных нанотрубок при 120ºC.
На рис. 1 представлены экспериментальные кинетические кривые расхода формальдегида в реакции с трет-бутанолом.
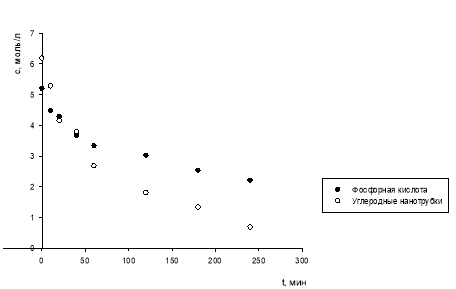
Рис. 1. Кинетические кривые расхода формальдегида в реакции с трет-бутанолом при 120ºС в присутствии ортофосфорной кислоты ([CH2O]0 = 5,20 моль/л) и углеродных нанотрубок ([CH2O]0 = 6,18 моль/л)
На рис. 2 представлены полулогарифмические анаморфозы кинетических кривых расхода формальдегида.
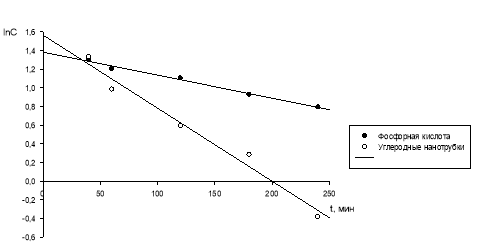
Рис. 2. Полулогарифмические анаморфозы кинетических кривых расхода формальдегида в реакции с трет-бутанолом при 120ºС в присутствии ортофосфорной кислоты ([CH2O]0 = 5,20 моль/л) и углеродных нанотрубок ([CH2O]0 = 6,18 моль/л)
Установлено, что кинетические кривые расходования формальдегида при конденсации трет-бутанола с формальдегидом в присутствии углеродных нанотрубок удовлетворительно (R = 0,98–0,99) линеаризуются в координатах lnC−t, что свидетельствует о первом порядке реакции по формальдегиду. Значения констант скоростей расходования формальдегида приведены в табл. 1.
Таблица 1
Значения константскоростей расходования формальдегида вприсутствии углеродных нанотрубок (5% масс., 120ºС)
|
Константа скорости расходования, k×10–3 мин-1 |
|
|
Фосфорная кислота |
3,16±0,20 |
|
Углеродные нанотрубки |
8,32±0,58 |
Также нами установлены значения констант скоростей накопления ДМД для реакции Принса с добавками углеродных нанотрубок (Табл. 2). Кинетику реакции накопления ДМД изучали хроматографическим методом (внутренний стандарт — 4,4,5-триметил-1,3-диоксан).
На рис. 3 представлены кинетические кривые накопления ДМД в реакции трет-бутанола с формальдегидом в присутствии фосфорной кислоты и углеродных нанотрубок.
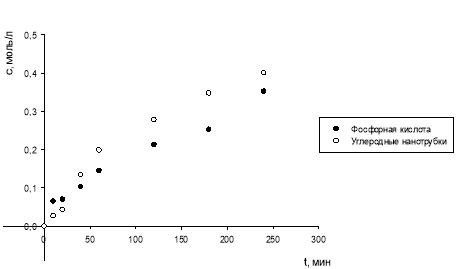
Рис. 3. Кинетические кривые накопления ДМД по реакции трет-бутанола с формальдегидом в присутствии ортофосфорной кислоты и углеродных нанотрубок при 120ºС
На рис. 4 представлены полулогарифмические анаморфозы кинетических кривых накопления ДМД.
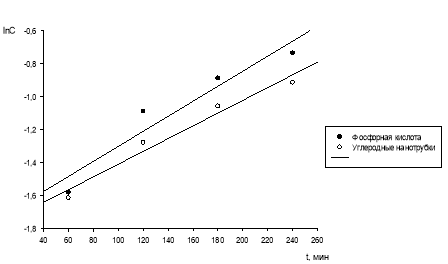
Рис. 4. Полулогарифмические анаморфозы кинетических кривых накопления ДМД по реакции трет-бутанола с формальдегидом в присутствии ортофосфорной кислоты и углеродных нанотрубок при 120ºС
Значения констант скоростей накопления ДМД приведены в табл. 2.
Таблица 2
Значения констант скоростей накопления ДМД иего содержание в присутствии углеродных нанотрубок (5% мас., 120ºС)
|
Константа скорости реакции накопления ДМД, k×10–3 мин-1 |
Соотношение ДМД и гидрированных пиранов |
|
|
Фосфорная кислота |
1,60±0,09 |
3/2 |
|
Углеродные нанотрубки |
4,10±0,20 |
16/1 |
На рис. 5 и 6 представлены аррениусовские зависимости для реакции трет-бутанола с формальдегидом как в присутствии 5 % масс. фосфорной кислоты, так и с добавлением 5 % масс. углеродных нанотрубок.
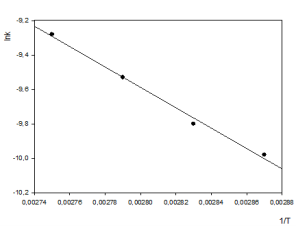
Рис. 5 Аррениусовская зависимость для реакции трет-бутанола с формальдегидом в присутствии 5 % масс. фосфорной кислоты (R = 0,99)
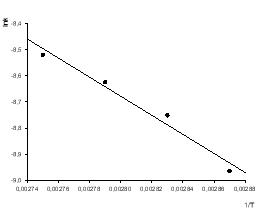
Рис. 6 Аррениусовская зависимость для реакции трет-бутанола с формальдегидом в присутствии 5 % масс. фосфорной кислоты и углеродных нанотрубок (R = 0,99)
По полученным данным определено значение энергии активации реакции взаимодействия трет-бутанола с формальдегидом с добавлением углеродных нанотрубок (92 кДж/моль), которое на 10 кДж/моль меньше энергии активации для реакции, проводимой только в присутствии ортофосфорной кислоты. Уменьшение энергии активации реакции при добавлении углеродных нанотрубок свидетельствует о том, что последние оказывают каталитический эффект на рассматриваемую реакцию.
Таким образом нами установлено, что добавка углеродных нанотрубок приводит к увеличению скорости образования ДМД и повышению избирательности его образования по реакции Принса с участием трет-бутанола.
Экспериментальная часть
Методика проведения кинетических экспериментов
В реактор, оборудованный загрузочным отверстием, помещают 5,2 г раствора формалина с концентрацией формальдегида 16,1 масс. % (0,028 моль), 0,018 моль трет-бутанола, 0,29 г 81 %-ной фосфорной кислоты и 5 % масс. углеродных нанотрубок. Мольное соотношение формальдегид/трет-бутанол, равно 1,8:1. Реактор закрепляют на перемешивающем устройстве и помещают в теплоноситель с заранее установленной температурой. Далее включают перемешивание. В реакторе выдерживают температуру 120°С. Реакционную массу выдерживают при постоянном перемешивании в течение 10, 20, 40, 60, 120, 180 и 240 минут. По окончании опытов реактор, охлаждают до 25–30°С, выгружают реакционную массу из реактора, отделяют фильтрованием углеродные нанотрубки от реакционной массы, далее органический и водный слои отдельно подвергают дальнейшей переработке. Из органического слоя ДМД выделяют экстракцией метил-трет-бутиловым эфиром (5 мл). Все эксперименты проводили в кинетической области.
Методы анализа
В работе использовались углеродные нанотрубки с диаметром пор 7–11 Å (ООО «Томский завод катализаторов», г. Томск). Хроматографический анализ проводили на хроматографе «Кристалл-5000» с пламенно-ионизационным детектором на стеклянной колонке, длина колонки 3,0 м, неподвижная фаза — силикон SE-30 (5 %), рабочая температура колонки 50–220°С. В качестве газа-носителя использовали азот (30 мл/мин). Анализ проводили при температуре испарителя 160°С, температуре детектора 220°С и температуре колонки 120°С. Растворители сушили по стандартным методикам [2].
Определение концентрации формальдегида
Пробу взвешивали, нейтрализовывали расчетным количеством 0,1 н NaOH, разбавляли 2–3 мл дистиллированной воды и проводили определение формальдегида сульфитным методом [3].
Определение концентрации ДМД
Пробу взвешивали, нейтрализовывали 2–3 мл концентрированного аммиака, добавляли точно взвешенное количество 4,4,5-триметил-1,3-диоксана (внутренний стандарт) и проводили хроматографическое определение ДМД [4].
Литература:
- Платэ Н. А., Сливинский Е. В. // Основы химии и технологии мономеров. М: Наука, 2002. С. 696.
- Беккер Х., Беккерт Р. и др. // Органикум, Т. 1. М.: Бином, 2008. C. 504.
- Фадеева В. И., Шеховцова Т. Н., Иванов В. М. // Основы аналитической химии. Практическое руководство. М.: Высшая школа, 2003. С. 463.
- Айвазов Б. В. // Основы газовой хроматографии. М.: Высшая школа, 1977. С. 182.







