Карбонилирование — химическая реакция введения карбонильных групп С=О путём взаимодействия с оксидом углерода. Для проведения этих реакций обычно применяется гомогенный катализ и повышенные давления.
К реакциям карбонилирования также относят гидрокарбонилирование, окислительное и восстановительное карбонилирование. В гидрокарбонилирование входят гидроформилирование, гидрокарбоксилирование и подобные им реакции. [1]
Ключевые слова: уксусная кислота, карбонилирование, метанол, общая характеристика производства, схема технологическая, процесс, катализатор.
Внастоящее время карбонилирование является одним из важных направлений гомогенного металлокомплексного катализа в химической промышленности. Путем введение карбонильной группы в молекулу можно получить различные классы органических соединений: альдегиды, кетоны, карбоновые кислоты и их производные, карбонаты и другие. Достоинством оксида углерода, как реагента в реакциях карбонилирования, является его высокая реакционная способность, вызванная наличием свободной пары электронов у атома углерода, дешевизна и доступность. Процесс карбонилирования является более экономичным способом получения карбонильных соединений.
CH3OH + СО → CH3COOH
Уксусная кислота является важным продуктом, используемым в химической промышленности, имеет около 9 миллионов тонн мирового спроса в год. Основное применение этого химиката в изготовлении сортированных эстеров ацетата, фунгицида, органических смесей, органических растворителей и подготовки фармацевтической продукции, ацетата целлюлозы, духов и синтетических волокон.
Исследование рынка синтетической уксусной кислоты выявило большой разрыв между ее спросом и предложением. Производство уксусной кислоты является проблемой в глобальном масштабе, но последние данные показывают снижение производственных мощностей во всем мире. Поэтому надо увеличить масштаб производства синтетической уксусной кислоты более эффективным способам как карбонилированием метанола.
Первый коммерческий процесс карбонилирования метанола, применял кобальтовый катализатор, был разработан немецкой химической компанией BASF в 1963 году. В 1968 году был обнаружен катализатор на основе родия (цис- [Rh(CO)2I2]-), который мог эффективно функционировать при более низком давление практически без побочных продуктов. Первый завод, использующий этот катализатор, был построен американской химической компанией Monsanto Company в 1970 году, после этого карбонилирование метанола над родиевым катализатором стало доминирующим методом производства уксусной кислоты. В конце 1990-х годов химическая компания BP Chemicals коммерциализировала катализатор Cativa ([Ir(CO)2I2]-). Этот процесс, с использованием иридиевого катализатора, более экологичен и более эффективен и в значительной степени вытеснил процесс Monsanto, на тех же производственных предприятиях [2]. Однако большинство производств на сегодняшний день используют родиевый катализатор, не смотря на повышенную селективность иридиевого катализатора, из-за дороговизны катализатора Cativa.
Уксусная кислота важный оптовый химикат, с емкостью годового производства мира 7 млн. тонн. Основное использование (около 40 %) уксусной кислоты в изготовлении ацетата винила, большого использования в индустрии полимера.
Процесс фирмы «BASF»
Реакция карбонилирования метанола была открыта учеными фирмы BASF в 1913 году. В 1960 году эта компания запустила первый завод по производству уксусной кислоты с использованием этого метода. Катализатором превращения был йодид кобальта. Метод заключался в барботировании окиси углерода через смесь реагентов. Выход уксусной кислоты составил 90 % для метанола и 70 % для СО. Одна из установок была построена в Гейсмаре (шт. Луизиана) и долгое время оставалась единственным процессом BASF в Соединенных Штатах [3].
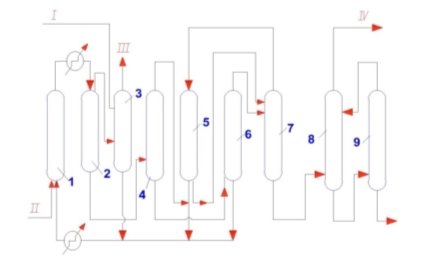
Рис. 1. Основная технологическая схема карбонилирования метанола по методике фирмы «BASF»: 1 — реактор; 2 — сепаратор высокого давления; 3 — скруббер; 4 — дегазатор; 5 — сепаратор низкого давления; 6 — колонна для отделения катализатора; 7 — водоразделительная колонна; 8, 9 — ректификационные колонны. Потоки: I — метанол; II — СO; III — абгаз; IV — уксусная кислота; V — побочные продукты
Синтез проводят при 250 °С и 70–75 МПа. Реакционную смесь из колонны синтеза сначала подают в сепаратор 2 высокого давления, а затем в сепаратор 3 низкого давления. Непрореагировавший монооксид углерода из сепаратора 3 возвращается в процесс. Жидкие продукты затем отделяются в колонне 4 от катализатора и направляются в ректификационную колонну 5. Раствор катализатора возвращается в колонну синтеза [4,5]. Непрореагировавший метанол берется из верхней части колонны 5, и неочищенная кислота подается в колонну 6, где извлекается уксусная кислота.
Недостатки
– Высокая температура и давление
– При этом процессе образуется многие побочные продукты.
Процесс фирмы «Monsanto»
В 1970 году фирмой Монсанто запущен новый метод производства синтетической уксусной кислоты путем каталитического карбонилирования метанола. В настоящее время этот процесс широко известен под названием «Процесс производства Монсантоуксусной кислоты» и является на сегодняшний день основным коммерческим методом получения уксусной кислоты. Используется родиевый катализатор.
Иодистый метил, необходимый для осуществления реакции, получается по уравнению:
CH3OH + HI → CH3I + H2O
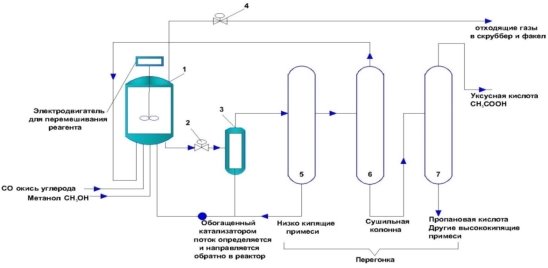
Рис. 2. Технологическая схема производства уксусной кислоты карбонилированием метанола фирмы «Монсанто»: 1 — реактор; 2,4– редукционный клапан; 3 — сепаратор; 5,6,7– ректификационные колонны
Реакцию карбонилирования проводят в непрерывных условиях при более низких температурах 150–200 °С и давлении 1–40 атмв реакторе с мешалкой 1. Жидкость выводится из реактора через редукционный клапан 2. Затем она поступает в адиабатический сепаратор 3, где легкие компоненты: метил– ацетат, метилиодид, некоторое количество воды и продуктовая уксусная кислота, отделяются в паровой фазе. Они поступают на установку ректификации для дальнейшей очистки. Оставшаяся жидкость, которая содержит растворенный катализатор, возвращается в реактор. Паровой поток из сепаратора 3 поступает в ректификационную колонну. В ней осуществляется первичное разделение смеси на три фракции. В качестве дистиллята отводятся гетероазеотропметилиодида с водой, метанол, HI. Уксусная кислота–сырец отводится боковым погоном. Кубовый продукт колонны 5, содержащий метилацетат, уксусную кислоту и растворенный в них катализатор, объединяется с потоком жидкости из сепаратора 3 и насосом возвращается в реактор 1. Каталитический цикл может быть представлен так: к плоскоквадратному комплексу [RhI2(CO)2]- (I) окислительно присоединяется иодистый метил с образованием шестикоординационного комплекса II, затем в результате внедрения СОпо связи метил-родий образуется ацетилродиевый комплекс (III). Восстановительное элиминирование иодангидрида уксусной кислоты регенерирует катализатор, а гидролиз иодангидрида дает уксусную кислоту. Готовый продукт отправляется на упаковку.
Преимущества
– Весь процесс использует меньше энергии, особенно для разделения и очистки продукта
– Имеет высокий выход приблизительно 98 % в расчёте на метанол
– Метанол более дешевое сырьё
– Хотя метанол обычно производится из синтез-газа, получаемого из нефти, его также можно получить из биомассы (древесины), бытовых отходов и сточных вод.
– Реакция очень быстрая, а катализатор имеет долгую жизнь.
Недостатки
– Металлический родий очень дорогой — дороже золота.
– Родий и йодид образует нерастворимые соли.
– Родий также катализирует побочные реакции.
Процесс фирмы «Cativa»
В 1996 году компания BP Chemicals внедрила метод «Cativa» с использованием катализатора на основе Ir с более высокими скоростями при низком содержании воды. Выдерживали давление 3–4 МПа, при температуре 150–180 °С, что обеспечивало высокую селективность 99 % (по метанолу).
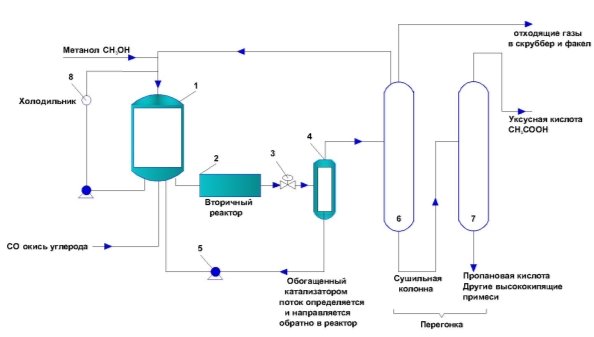
Рис. 3. Основная технологическая схема карбонилирования метанола по методике фирмы «Cativa»: 1 — реактор; 2 –вторичный реактор; 3 — дроссельный вентиль; 4 — сепаратор пар-жидкость; 5 — насос; 6,7- ректификационные колонны;8 — холодильник
В реактор 1 подаются сверху метанол, снизу СО. Перемешивание обеспечивается мешалкой. Реакционная масса из реактора 1 подается в реактор 2 трубчатого типа. Это позволяет увеличить время пребывания исходного сырья в зоне реакции и конверсию СОза один проход. Затем после снижения давления вентилем 3 парожидкостная смесь поступает в сепаратор пар–жидкость 4. Парогазовая смесь в дальнейшем поступает на ректификационное разделение, а жидкая фаза, обогащенная каталитическим комплексом, возвращается в реактор 1. Выделение товарной уксусной кислоты обеспечивается ректификационными колоннами 6 и 7. В колонне 6 в качестве дистиллята отделяют легкокипящие компоненты системы (HI, СН3ОН, CH3I, воду). В качестве кубового продукта отбирают уксусную кислоту с примесями тяжелокипящих побочных продуктов. Средним погоном отбирают раствор, обогащенный каталитическим комплексом. Его возвращают в реактор. Дистиллят колонны 7 разделяют на паровую и жидкую фазы. Жидкость возвращают в реактор, а парогазовую смесь (в основном СО, HI; пары органики по насыщению) направляют на санитарную очистку и каталитическое дожигание. Окончательную очистку уксусная кислота проходит в колонне7. [6,7]
Преимущества
– Иридий немного дешево родия
– Реакция происходить быстрее, а количество побочных продуктов значительно ниже, что снижает затрат на очистку.
– Некоторая конверсия СО в СО2 все еще происходит, но с гораздо меньше скоростью.
– Использование СО увеличено с 85 % до более 94 %.
Недостатки
ВЫВОД
Производство уксусной кислоты методом карбонилирования метанола стало технологией выбора на мировом рынке, таким методом получают около 75 % всей уксусной кислоты в мире. Сравнительный анализ методов карбонилирования метанола показал, что жесткие условия проведения процесса фирмой «BASF» являются существенным недостатком, ограничивающим его широкое промышленное применение. Поэтому выявленная фирмой «Monsanto» и «Cativa» способность родиевых и иридиевых соединений катализировать реакцию карбонилирования метанола имеет важное практическое значение.
Литература:
- Лапидус А. Л. Карбонилирование. Химическая энциклопедия. 1990 г. Т.2.-С. 324
- Березин, Б. Д. Курс современной органической химии / Березин Б. Д. — М.: Высшая школа, 2001. — 768с.
- Караханов, Э. А. Метанол и синтезы на его основе / Э. А. Караханов // Журнал химика. — 2007. — № 4. — С. 31–33.
- Hallinan, N. Carbonylation of Methanol and Methyl Acetate / N. Hallinan // Homogeneous Catalysis — 2008. — Pp. 109–124.
- Winkelmann, J. Diffusion coefficient of acetic acid in acetic acid ethyl ester / J. Winkelmann // Physical Chemistry — 2016. — Pp. 621–632.
- Nefedov, B. K. Carbonylation reactions / B. K. Nefedov, N. S. Sergeeva, T. V. Zueva, E. M. Shutkina, Ya. T. Eidus // Bulletin of the Academy of Sciences of the USSR, Division of chemical science — 2011. — Pp. 565–568.
- Ping, Y. Y. Oxidative carbonylation of organic compounds by carbon monoxide and transition-metal salt catalysts / Y. Y. Ping, A. L. Lapidus // Bulletin of the Academy of Sciences of the USSR, Division of chemical science — 2005. — PP. 327–230.







