В статье авторы изучают изменение электрофлотационной степени извлечения ионов Fe 3+ от концентрации неионогенных ПАВ.
Ключевые слова: электрофлотация, неионогенный ПАВ, ионы железа (III).
Метод электрофлотации используется в пищевой, нефтеперерабатывающей, машиностроительной промышленностях. Он применяется для очистки воды от разных примесей и растворенных в ней веществ.
Процесс электрофлотациии основан на пропускании постоянного электрического тока через воду. В результате чего образуются мелкодисперсные пузырьки кислорода и водорода, равномерно распределенные по всему объёму воды. Под действием выталкивающей силы эти пузырьки поднимаются наверх, по пути прилипая к загрязняющим веществам, и флотируются, образуя устойчивый пенный слой. Эффективность данного процесс зависит от числа и размера пузырьков выделяющихся газов. Главную роль здесь играют образующиеся на катоде пузырьки водорода, размер которых может достигать 10–40 мкм. Чем меньше их форма, тем лучше они растворяются в воде и больше захватывают мельчайших загрязняющих частиц. На размер пузырьков влияют: материал катода, его диаметр плотность тока и электропроводность. Изменяя плотность тока можно варьировать скорость флотации. Обычно, чем больше насыщение раствора пузырьками, тем выше скорость флотации, но до определенного предела. Увеличение плотности тока будет увеличивать поток пузырьков, и они начнут отрываться от частиц примесей. Электропроводность прямопропорционально влияет на размер пузырьков. Чем меньше она, тем меньше их размер [1,2,3].
Для процесса электрофлотации применялись электролиты, в состав которых входили растворы FeCl 3 (основной компонент), Na 2 SO 4 (компонент для улучшения электропроводности), Пенетрант ЛЖ-6А (ПАВ).
В колбу на 500 мл набирали немного дистиллированной воды, добавляли раствор FeCl 3 0,5 мл с конценрацией 50мг/л, раствор Na 2 SO 4 10 мл с концентрацией 1г/л, затем доводили до метки дистиллированной водой. Закрывали колбу, хорошо перемешивали и выливали содержимое в мерный стакан. Из мерного стакана отбирали 1 мл пробы в колбу на 50 мл и доводили до метки 2 % раствором HNO 3 . Далее из колбы выливали содержимое в специальную ёмкость, плотно закрываем крышкой и отправляли на анализ в другую лабораторию.
Стакан ставили на магнитную мешалку, добавляли по маленьким каплям щелочной электролит и с помощью показаний рН-метра смотрели за изменением рН нашего раствора. В качестве вспомогательных электролитов использовались H 2 SO 4 и NaOH. Начальный рН раствора колебался в диапазоне 3,5–4,0. Данная работа проводилась при рН=7.
После достижения нужного значения рН, раствор тщательно перемешивали стеклянной палочной и отправляли в лабораторный электрофлотатор, предварительно промытый дистиллированной водой. Далее включали источник постоянного тока и регулятором устанавливали заданную величину тока, отмечая время начала электрофлотации.
Для осуществления электрофлотационного процесса применялся непроточный трубчатый электрофлотатор с нерастворимыми анодами (рис. 1).
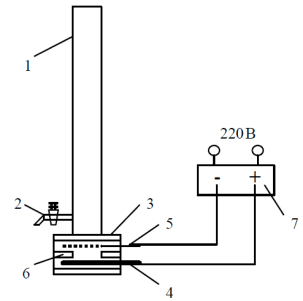
Рис. 1 . Схема лабораторной электрофлотационной установки периодического действия: 1 — колонна электрофлотатора; 2 — вентиль для отбора проб; 3 — электродный блок; 4 — анод; 5 — катод; 6 — резиновая прокладка; 7 — источник постоянного тока
Установка изготовлена из оргстекла в виде вертикальной колонны (1) с внутренним диаметром 40 мм и общей высотой 800 мм. В нижней части расположен электродный блок (3), состоящий из катода (5) и анода (4), расположенных, друг относительно друга горизонтально на расстоянии 10 мм, при этом сетчатый катод расположен сверху, а пластинчатый анод — снизу. Края электродов изолированы друг от друга с помощью резиновой прокладки (6). Материал катода выполнен в виде сетки из нержавеющей стали, размер сетчатых ячеек — 0,5 х 0,4 мм, толщина проволоки — 0,3 мм. Материал анода — титан, покрытый активным слоем из смешанных изоморфных оксидов титана, кобальта и рутения (ОРТА). По высоте колонны расположен вентиль (2) для отбора проб воды. Питание электродов осуществляется источником постоянного тока (7).
После проведения процесса электрофлотации через вентиль (2) отбирали 1 мл пробы в колбу на 50 мл и доводили до метки 2 % раствором HNO 3 . Далее из колбы выливали содержимое в специальную ёмкость, плотно закрывали крышкой и отправляли на анализ в другую лабораторию. Следующую пробу (1 мл) отбирали, предварительно пропустив раствор через фильтровальную бумагу. Далее проделывали те же самые действия, что и с предыдущей пробой.
Эффективность электрофлотационного процесса оценивается степенью извлечения α и рассчитывается по формуле:
α = (C исх -С кон )/ C исх * 100 %,
где C исх и C кон — исходная и конечная концентрации дисперсной фазы в водной среде, г/м 3 .
Данные эксперименты проводились с целью узнать при каком значении pH будет наилучшее извлечение ионов железа с начальной концентрацией Fe 3+ 50 мг/л. А также определить влияние неионогенного ПАВ (Пенетрант ЛЖ-6А) на степень извлечения частиц.
Остаточная концентрация ионов железа (III) после электрофлотации (ЭФ) и фильтрации (Ф) приведена в таблице 1.
Таблица 1
|
pH |
C Fe 3+ ( ост.) , мг/л |
|
|
ЭФ |
Ф |
|
|
9,0 |
44,7 |
2,6 |
|
7,0 |
4,2 |
2,7 |
Условия эксперимента: C
исх
(Fe
3+
)=50 мг/л;
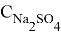
Степень извлечения Fe 3+ в процессе электрофлотации и последующей фильтрации приведена в таблице 2.
Таблица 2
|
pH |
α, % |
|
|
ЭФ |
Ф |
|
|
9,0 |
11 |
95 |
|
7,0 |
92 |
95 |
Условия эксперимента: C
исх
(Fe
3+
)=50 мг/л;
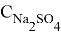
Сравнив экспериментальные данные таблиц 1 и 2 при различных pH, можно сделать вывод, что электрофлотационное извлечение ионов Fe 3+ при рН=7,0 без добавления ПАВ идёт лучше, чем при рН=9. Поэтому следующие эксперименты будут проводиться при рН=7.
Далее были проведены эксперименты по извлечению ионов железа в присутствии неионогенного ПАВ Пенетрат ЛЖ-6А с различной концентрацией 0,1‑100 мг/л. Остаточная концентрация ионов железа (III) после электрофлотации (ЭФ) и фильтрации (Ф) в присутствии ПАВ (Пенетрант ЛЖ-6А) приведена в таблице 3.
Таблица 3
|
pH |
С ПАВ (Пенетрант ЛЖ-6А) , мг/л |
C Fe 3+ ( ост.) , мг/л |
|
|
ЭФ |
Ф |
||
|
7,0 |
0,1 |
5,2 |
1,2 |
|
0,5 |
6,6 |
2,5 |
|
|
1,0 |
2,4 |
0,6 |
|
|
5,0 |
2,5 |
0,8 |
|
|
10,0 |
2,0 |
1,3 |
|
|
50,0 |
6,1 |
1,8 |
|
|
100,0 |
10,4 |
1,4 |
|
Условия эксперимента: C
исх
(Fe
3+
)=50 мг/л;
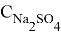
Степень извлечения Fe 3+ в процессе электрофлотации и последующей фильтрации приведена в таблице 4.
Таблица 4
|
pH |
С ПАВ (Пенетрант ЛЖ-6А) , мг/л |
α, % |
|
|
ЭФ |
Ф |
||
|
7,0 |
0,1 |
90 |
98 |
|
0,5 |
87 |
95 |
|
|
1,0 |
96 |
99 |
|
|
5,0 |
95 |
99 |
|
|
10,0 |
96 |
98 |
|
|
50,0 |
88 |
97 |
|
|
100,0 |
80 |
98 |
|
Условия эксперимента: C
исх
(Fe
3+
)=50 мг/л;
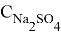
Сравнив полученные экспериментальные данные, было отмечено, что электрофлотационное извлечение частиц Fe
3+
будет наиболее эффективным при добавлении ПАВ (Пенетрант ЛЖ-6А) в количестве 1 мг/л. Степень извлечения достигла
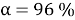
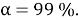
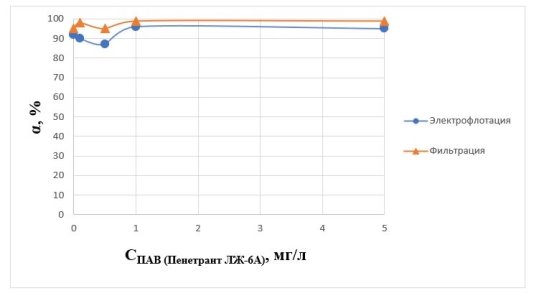
Рис. 2. Влияние концентрации ПАВ Пенетрат ЛЖ-6А (0,1–5 мг/л) на степень извлечения ионов Fe 3+ в водном растворе
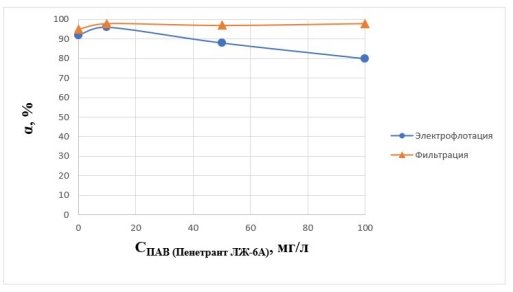
Рис. 3. Влияние концентрации ПАВ Пенетрат ЛЖ-6А (10–100 мг/л) на степень извлечения ионов Fe 3+ в водном растворе
Литература:
- Ильин, В. И. Технология очистки сточных вод предприятий машиностроения и металлообработки с использованием электрофлотофильтрационных процессов / В. И. Ильин, В. А. Колесников, С. О. Вараксин, С. А. Герасимов // Оборонный комплекс — научно-техническому прогрессу России. — 2007. — № 1. — С.68–70.
- Колесников В. А., Ильин В. И., Капустин Ю. И. Электрофлотационная технология очистки сточных вод промышленных предприятий / — М.: Химия. 2007. — 307 с.
- Колесников В. А., Ильин В. И., Бродский В. А., Колесников А. В. Электрофлотация в процессах водоочистки и извлечения ценных компонентов из жидких техногенных отходов. Обзор // Теоретические основы химической технологии. — 2017. — Т. 51, № 4. — С. 361–375.







