В статье приведены результаты выделения и идентификации биологически активных веществ фенольной природы этилацетатного экстракта Bassia hyssopifolia (Pall.) Kuntze, произрастающего на территории Северного Казахстана методами адсорбционного распределительной хроматографии, бумажной хроматографии и ТСХ, УФ- и ЯМР-спектроскопии.
Ключевые слова : Bassia hyssopifolia (Pall.) Kuntze, бассия иссополистная, качественный состав Bassia hyssopifolia (Pall.) Kuntze, фенольные соединения Bassia hyssopifolia (Pall.) Kuntze.
Род Bassia семейства Amaranthaceae включает 25 видов однолетних травянистых растений или многолетних полукустарников. Bassia hyssopifolia (Pall.) Kuntze это однолетнее цветущее растение, растущее на солончаках, песках, пустырях. Растет растение в Европе, на Кавказе, Средней и Центральной Азии, в Северной Америке. В Казахстане растение произрастает в поймах рек Тобол, Ишим, Иртыш, Эмба, на Тургайском плато, в Прибалхашье, в Джунгарском и Заилийском Алатау, Карат и т. д. [1–3].
Род Bassia — обитатели аридных и сильно засоленных территорий. Действительно, за исключением сорных и рудеральных растений, это преимущественно ярко выраженные ксерофиты и классические галофиты, живущие часто в условиях крайней сухости и чрезвычайного засоления почвы, которых уже не выносят никакие другие растения. Галофиты часто содержат большое количество алкалоидов, сапонинов, кумаринов.
По химическому составу Bassia hyssopifolia плохо изученное растение. Известно о содержании алкалоидов сальсолин и сальсолидин, а также сапонинов [4].
Бассия иссополистная ядовита для сельскохозяйственных животных вследствие содержания алкалоидов и сапонинов. Некоторые источники указывают в качестве причины токсичности растения накопление значительных количеств оксолатов [5]. Установлено, что бассия иссополистная накапливает значительные количества аминокислот и жирных кислот [6]. Растение содержит фенольные соединения, такие как флавоноиды (халконы, ауроны). В составе бассии иссополистной обнаружены терпены, сапонины (аралозиды) [7].
Бассия иссополистная проявляет антиоксидантную активность за счет восстановления ионов тяжелых металлов, т. е. ингибируют процессы окисления, связанные с каталитической активностью тяжелых металлов [8]. Установлено, антиоксидантная активность экстрактов бассии иссополистной по модели окисления липосомфосфатидилхолина по тесту с тиобарбитуровой кислотой, разработанному Пивоваренко В. Г. применительно к изофлавонам [9].
Цель нашего исследования: выделение и идентификация индивидуальных веществ этилацетатного и хлороформного извлечений Bassia hyssopifolia (Pall.) Kuntze.
Объект исследования — надземные части и корни растения рода Бассия ( Bassia ) вид бассия иссполистная или кохия иссополистная (лат. Bassia hyssopifolia (Pall.) Kuntze ), заготовленных в местах их естественного произрастания в фазе покоя в Северном Казахстане.
Материалы и методы исследования
2 кг мелко измельченного воздушно сухого растительного сырья трижды экстрагировали по 24 часа 70 % ацетоном при температуре от 20 до 25 0 С. Объединенный экстракт концентрировали в мягких условиях в вакууме водоструйного насоса до полного удаления ацетона. Полученный густой экстракт последовательно обрабатывали бензолом, хлороформом, этилацетатом, н-бутанолом, для предварительного разделения БАВ в зависимости от их растворимости. Из полученных экстрактов удалили растворители на ротационном испарителе. Получили 5 рабочих густых экстрактов: бензольный, хлороформный, этилацетатный, н-бутанольный и водный остаток.
Разделение веществ этилацетатной и хлороформной вытяжек осуществили методом адсорбционно-распределительной колоночной хроматографии [10]. Для этого 10 г этилацетатной вытяжки водно-ацетонового экстракта разделили сухим способом на полиамиде. В качестве элюентов были использованы вода-этанол в соотношениях 2:8, 3:7, 4:6, 1:1, 7:3, 6:4. Хлороформный экстракт разделили на сорбенте Silicagel марки КСК 100/160 м, элюируя смесью хлороформ-ацетон с последующим увеличением соотношения ацетона и смесью гексан-этилацетат с увеличением доли этилацетата. Разделение веществ контролировали методом ТСХ.
Результаты и обсуждение
В результате хроматографического разделения этилацетатной вытяжки Bassia hyssopifolia (Pall.) Kuntze были выделены феруловая кислота, кумаровая кислота, галловая кислота, п-гидроксибензойная кислота, ванилиновая кислота, которые были идентифицированы методом одномерной бумажной хроматографии (БХ) в сравнении с достоверными образцами и методами спектроскопии УФ, ЯМР [11]. Из хлороформного извлечения выделена эллаговая кислота и вещество предположительно терпенового характера.
Феруловая кислота
Кристаллическое вещество белого цвета. С 10 Н 10 О 4 . Т. пл. 168–170 °C (водный спирт).
УФ-спектр, λ max , EtOH: 217, 242, 290 (пл), 322 нм.
Спектр ЯМР 1 Н (300 МГц, ДМСО-d6, δ, м. д.): 9,18 (1Н, с, 4-ОН-группа), 7,45 (д, J 16 Гц, Н-7), 7,08 (1Н, дд, J 2.5 и 9 Гц, Н-6), 7,03 (д, J 2,5 Гц, Н-2), 6,93 (д, J 9 Гц, Н-5), 6,24 (1Н, д, J 16 Гц, Н-8), 3,80 (3Н, с, СН 3 О-группа) (рис. 1).
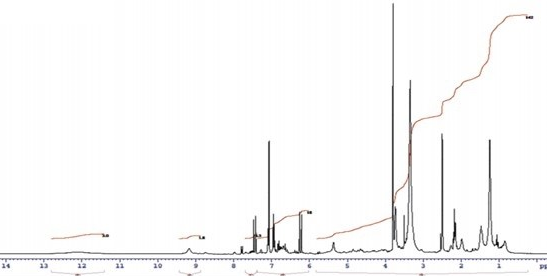
Рис. 1. ПМР-спектр феруловой кислоты
Кумаровая кислота
Белые кристаллы. C 9 H 8 O 3 , т.пл. 210–213 °C. R f 0,86
Ванилиновая кислота (4-гидрокси-3-метоксибензойная кислота) — 3-монометиловый эфир протокатеховой кислоты
Светло желтые кристаллы. С 8 Н 8 О 4 , т.пл. 209–213 о С. R f 0,63
Галловая кислота — 3,4,5-триоксибензойная кислота или 3,4,5-тригидроксибензойная кислота
Бесцветные кристаллы, темнеющие на свету. C 7 H 6 O 5 , т.пл. 240 о С с разложением. R f 0,75
п-гидроксибензойная кислота
Белые кристаллы. HO-C 6 H 4 -COOH, т.пл. 213–215 °C. R f 0,89
Эллаговая кислота — 2,3,7,8-тетрагидрокси [1]бензопирано [5,4,3-cde] [1]бензопиран-5,10-дион
Желтые кристаллы. С 14 Н 6 О 8 , т.пл. 448–450°C с разложением. Rf 0,73
Масс-спектр (ESI-MS, 180 °С, m/z): М+ 303 (302 + Н).
Выводы
По результатам проведенных исследований из этилацетатной фракции Bassia hyssopifolia (Pall.) Kuntze адсорбционно-распределительной хроматографии выделены пять соединений фенольного характера: 2 оксикоричные кислоты и 3 фенолокислоты, которые идентифицировали методами тонкослойной и бумажной хроматографии непосредственным сравнением с достоверными образцами, а также методами спектроскопии. Из хлороформной вытяжки выделили эллаговую кислоту и вещество предположительно терпенового характера.
Литература:
- Онегов А. С. Занимательная ботаническая энциклопедия: Цветущие травы. — М.: Педагогика-Пресс, 2000.
- The families and genera of vascular plants. Edited by Kubitzki. Volume II. Springer 1993. р 269.
- Флора Сибири. т. 5. Новосибирск: Наука. 1992. с 163.
- Растительные ресурсы СССР. Цветковые растения, их химический состав, семейства Magnoliaceae − Limoniaceae. Л.: Наука, 1984 с 227.
- James LF, Williams MC, Bleak AT, 1976. Toxicity of Bassia hyssopifolia to sheep. Journal of Range Management. 5. Государственная
- Токарев А. В., Дрюк О. В. Амино — и жирнокислотный состав Bassia hissopifolia //Материалы IV Международной Научно-практической конференции «Методология, теория и практика современной биологии», Костанай, 15 марта 2019г., С. 115–119
- Токарев А. В., Дрюк О. В. Качественный анализ некоторых групп биологически активных веществ растения Bassia hyssopifolia // Труды VІІ Международной научно-практической конференции молодых ученых, студентов и школьников «Жас ғалым — 2019» посвященной «Году молодежи», Тараз, 22 февраля, 2019 г., с. 292–294
- Дрюк О. В., Букенова А. Определение антиоксидантной активности некоторых растений Северного Казахстана // материалы VIII Всероссийской конференции. 5–9 октября 2020 г. / под ред. Н. Г. Базарновой, В. И. Маркина. — Барнаул: Изд-во Алт. ун-та, 2020. — С. 151–153.
- Букенова А. Определение антиоксидантной активности некоторых растительных экстрактов in vitro // Материалы VI Международной научно-практической конференции «Global science and innovations 2019: Central Asia», Нур-Султан, 9–13 мая 2019 г., т. 1, с. 213–214
- Бердимуратова Г. Д., Музычкина Р. А., Корулькин Д. Ю., Абилов Ж. А., Тулегенова А. У.. Биологически активные вещества растений. Выделение, разделение, анализ. — Алматы: Атамура, 2006. — 438 с.
- Хроматография на бумаге // под ред. Хайса И. М., Мацека М. — М.: Национальная литература», 1962. — 852 с.







