В статье авторы изучают вопрос использования тепловизионной диагностики в сфере медицины и в частности стоматологии.
Ключевые слова: инфракрасная термография, слизистая оболочка полости рта, ботулинический токсин.
Идея использования тепловидения насчитывает десятки веков. Еще врачи Древней Греции определяли локализацию глубоко расположенной опухоли по местам, где наиболее быстро высыхал ил, который тонким слоем наносили на кожу больного. Первые работы по измерению температуры тела человека относятся к 1974 г. (Б. Энандер, К. Ларсон, 1974), когда была предпринята попытка применить радиоастрономический метод измерения слабых тепловых сигналов астрономических объектов в медицине с учетом особенностей измерения биологических тканей.
Наше внимание привлекли сведения об инфракрасной термографии — методе регистрации собственного инфракрасного излучения исследуемой поверхности тела человека с помощью специального прибора (Голованова М В с соавт. 2010: Дехтярев Ю.П) На данный момент современная медицина достигла того уровня, когда термография применяется для определения болезней, так как между температурой человека и заболеваниями есть прямая связь: поверхностные эффекты и изменения напрямую связаны с процессами, происходящими в организме любого человека.
Следует заметить, что в наше время термография относится к разделу пассивной диагностики. Довольно давно тепловизоры с успехом вошли в раздел медицинского оборудования и стали использоваться повсеместно, в том числе в гностических и клинических целях. Тепловизионная диагностика абсолютно безопасна и безвредна как для пациентов, так и для медицинского персонала, являясь современным и чрезвычайно эффективным методом мониторинга лечебно-реабилитационного процесса. (Марусина М. Я., 2007)
В основе термографии лежит измерение теплового излучения, так как известно, что все физические тела, имеющие температуру выше абсолютного нуля (-273° C). согласно закону M. Планка (1900). излучают электромагнитные волны. это излучение является тепловым. Процесс происходит за счет заряженных частиц (электроны, ионы), которые находятся в хаотическом движении и обладают свойствами электрической или магнитной полярности. (Голованова М. В 2011). Интенсивность этих процессов пропорциональна температуре тела и его излучательной способности. Поскольку движение частиц хаотическое, они создают радиоволны различной длины. Глубина эффективного измерения температуры равна толщине излучающего слоя (скинн-слой) и определяется как расстояние, на которое распространяется электромагнитная волна от поверхности объекта до того слоя, в котором ее интенсивность уменьшается в 2,73 раза. При прочих равных условиях, чем больше длина волны, тем больше глубина, с которой можно регистрировать температурные возмущения.
К неоспоримым преимуществам этого метода можно отнести его способность выявлять болезнь задолго до ее клинического воплощения, а также при отсутствии симптомов заболевания. Инфракрасная термография позволяет измерять температуру в труднодоступных областях: ретромолярная область, корень языка, подъязычная область, слизистая оболочка альвеолярного отростка и альвеолярной части. B области жевательной группы зубов, дистальные отделы щечной области. Это обуславливает простоту проведения инфракрасной термографии. Конечно, как и в других случаях, возникают трудности расшифровке полученных результатов из-за анатомических особенностей полости рта, а также невозможностью ее полной изоляции от слюны, поэтому всегда существует возможность некоторой погрешности данных.
Таким образом, при определении температурных показателей слизистой оболочки полости рта и кожных покровов в проекции жевательных мышц у пациентов с гипертонусом жевательных мышц было установлено статистически достоверное их изменение: температурные показатели в области околоушно-жевательной (проекции жевательной мышцы) и передней порции височной мышцы выше у женщин, чем у мужчин в среднем на 1,19 С. и по сравнению со здоровой группой у женщин в области околоушно-жевательной (проекции жевательной мышцы) показатели выше на 1,5° С и у мужчин — на 1,1ºС, а в области проекции передней порции височной мышцы — выше у женщин мужчин в среднем на 1,1ºС. (p<0,05).
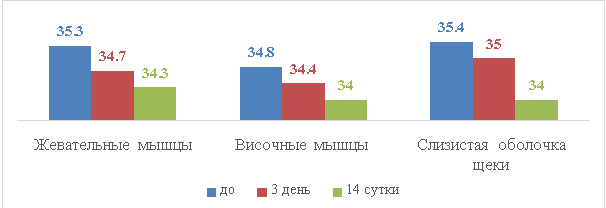
Рис. 1 Динамика изменения температурных данных после инъекций ботулинического токсина типа А Лантокс у мужчин 2 группы
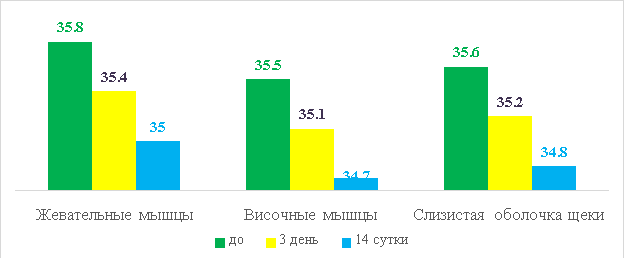
Рис. 2 Динамика изменения температурных данных после инъекций ботулинического токсина типа А Лантокс у женщин 2 группы
Анализ динамики температурных данных инфракрасной термографии через 3 дня и на 14 сутки дня после внутримышечной инъекции раствора ботулинического тип А «Лантокс» температура кожи в области жевательных и височных мыши и со стороны проекции данных мышц на слизистую оболочку щеки у мужчин и женщин 2 группы уменьшилась в среднем на 0.44 + 0,03° C (p<0,05). Метод инфракрасной термометрии слизистой оболочки полости рта и кожных покровов в проекции жевательных мышц у пациентов с гипертонусом жевательных мышц является высокоинформативным методом функциональной оценки уровня метаболизма жевательных мышц.
Инъекции препарата ботулинического токсина типа А «Лантокс» выполнялись в жевательные, височные мышцы симметрично с двух сторон. Инъекции производились в жевательные мышцы со стороны кожных покровов щеки по нижнему краю нижней челюсти в до 30 ЕД на одну сторону, а височные мышцы в дозе 20 ЕД на одну сторону. Средняя общая доза составила 100 ЕД Основой для выбора мышц-мишеней для инъекций являлась клиническая картина и данные с поверхностной электромиографии в соответствии со стандартными рекомендациями.
В конечном итоге мы можем заключить, что мониторинг динамики локальной температуры кожи лица, проводимый с помощью инфракрасной термографии, и динамики биоэлектрической активности поверхности лица, проводимый с помощью поверхностно ЭМГ, может оптимизировать диагностику и лечение гипертонуса желательных мышц. В частности, инфракрасная термография и поверхностная ЭМГ могут быть использованы для диагностики гипертонуса мышц и для оценки эффективности и безопасности и инъекций в эти мышцы локальных миорелаксантов.
Литература:
- Заяц Г. А., Коваль В. Т. Медицинское тепловидение современный метод функциональной диагностики // Здоровье, Медицинская экология и наука. — 2010, № 3-С 27–33
- Голованова М. В., Потехина Ю. П. Возможности термодиагностики в медицине — Нижний Новгород, 2011, 164 c.
- Турбина Л. Г., Гришина Н. В. Диагностика патогенетическое лечение миофасциального болевого синдрома лица. // Рос стоматологический журнал -2001, № 5
- Рабухина Н. А., Голубева Т. И., Перфильев С. А. Спиральная компьютерная томография при заболеваниях челюстно-лицевой области.- М. Медпресс-информ, 2006, 127 с.







