В статье рассматривается процесс получения сероуглерода из метана и серы. Проведен анализ влияния технологических параметров на удельную производительность и селективность реакции синтеза сероуглерода на основе результатов моделирования в программе COMSOL Reaction Engineering Lab.
Ключевые слова: сероуглерод, сера, удельная производительность РИВ, COMSOL, конверсия метана.
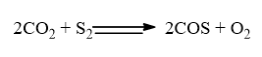
Сероуглерод получают из метана, входящего в состав природного газа и серы. Синтез сероуглерода проходит в парогазовой среде со стехиометрическим избытком серы на катализаторах различного состава по следующей схеме [1]:

При этом также протекает побочная реакция процесса синтеза сероуглерода:
Сероуглерод — это бесцветная жидкость с приятным «эфирным» запахом. Молекула сероуглерода имеет линейное строение. Данное соединение токсично, огнеопасно, имеет самый широкий диапазон концентрационных пределов взрываемости.
Хорошо растворяет жиры, масла, смолы, каучук, используется в качестве экстрагента; растворяет серу, фосфор, иод, нитрат серебра. Сероуглерод применяют для получения ксантогенатов, четыреххлористого углерода, роданидов, поэтому потребность в производстве данного продукта является актуальной. [2]
Для формализации процесса рассмотрим реакцию синтеза сероуглерода:
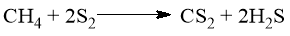
A + 2Y → B + 2Z
При температуре 550–700°С скорость реакции описывается уравнением второго порядка [1]:
k = [P A ]* [P Y ]
Константа скорости реакции описывается следующим уравнением:
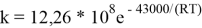
Для моделирования процесса в программе «COMSOL Reaction Engineering Lab» зададимся начальными параметрами процесса. В настоящее время процесс синтеза сероуглерода проводят при следующих параметрах:
Таблица 1
Параметры процесса синтеза сероуглерода
|
Мольное соотношение реагентов |
СН 4 : S 2 = 1: 2,1 |
|
Температура реакции Т, °C |
575 до 680 С |
|
Давление P, бар |
От 2,8 до 7,1 |
|
Степень превращения, % (по метану) |
98,10 |
|
Селективность основной реакции, % |
95,10 |
|
Тип реактора |
Реактор идеального вытеснения (РИВ) |
Для реактора РИВ удельную производительность вычисляют по уравнению [3]:
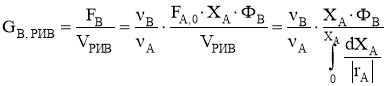
где F B — мольный поток целевого продукта (В);
V РИВ — реакционный объем;
F A ,0 — начальный мольный поток реагента Y;
X A — конверсия реагента Y;
Ф В — селективность основной реакции по целевому продукту (В).
Кинетические кривые построим с помощью программы «COMSOL Reaction Engineering Lab», выглядят они следующим образом [4]:

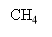
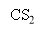
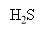

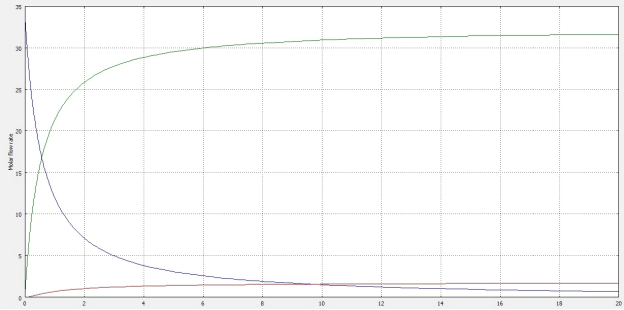
Рис. 1. Кинетические кривые процесса получения сероуглерода (B) в реакторе идеального вытеснения (РИВ)
Влияние конверсии метана на удельную производительность РИВ:
По заданным значениям построим график зависимости удельной производительности реактора от конверсии метана:
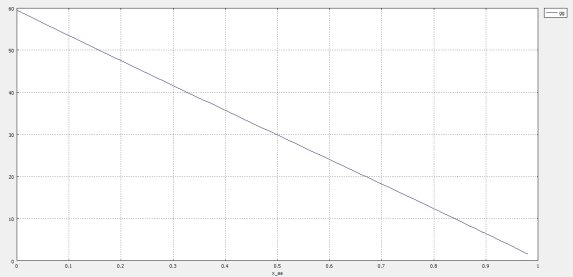
Рис. 2. График зависимости удельной производительности РИВ от конверсии метана (x_aa)
Падающий характер кривой G B = f(x_aa) объясняется тем, что скорость реакции синтеза сероуглерода уменьшается с повышением степени конверсии.
Влияние избытка второго реагента на удельную производительность РИВ:
Для определения зависимости удельной производительности РИВ от избытка серы выберем значение, при котором будем определять значение производительности: (А:Y = 1: 2,1):



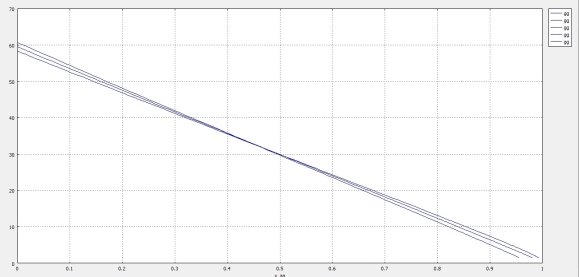
Рис. 3. График зависимости удельной производительности РИВ от конверсии метана, при избытке серы
1 — избыток серы 73,37 + 4,0 mol/s; 2 — базовое значение серы 73,37 mol/s; 3 –значение серы 73,37–4,0 mol/s
Повышение удельной производительности объясняется тем, что с увеличением избытка серы по отношению к метану скорость реакции возрастает, а, следовательно, возрастает и удельная производительность реактора.
Влияние температуры на удельную производительность РИВ:
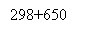
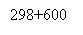
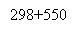


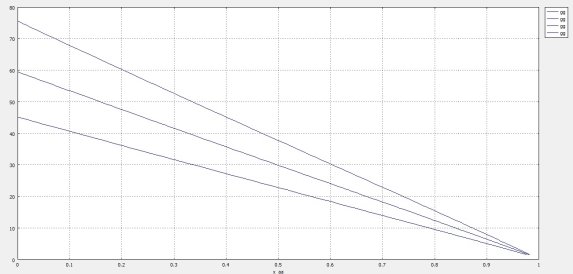
Рис. 4. Зависимость удельной производительности от конверсии метана для РИВ при температуре 298 + 600 (550, 650) K
Из графика видно, что значения удельной производительности РИВ повышаются при росте температуры. Это связано с тем, что рост температуры приводит к росту скорости, так как реакция получения сероуглерода является необратимой с положительной величиной энергии активации.
Далее рассмотрим влияние конверсии сероуглерода на селективность для РИВ:
Зависимость селективности от степени превращения:
Построим графики зависимости селективности реакции по продукту В для типа реактора РИВ:
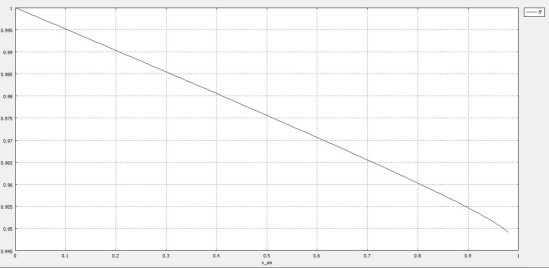
Рис. 5. График зависимости селективности реакции по целевому продукту от конверсии для РИВ
Падающий вид кривой Ф А В = f(Х Y ) объясняется тем, константа скорости реакции синтеза сероуглерода k 1, много больше константы скорости побочной реакции реакции k 2 , поэтому селективность с увеличением конверсии значительно падает.
Влияние избытка второго реагента на селективность для РИВ:
Изменяя значение избытка второго реагента, построим графики зависимости селективности от конверсии метана.



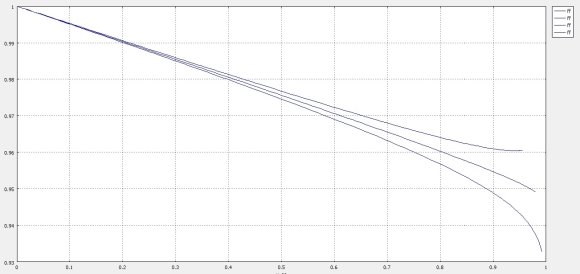
Рис. 6. График зависимости селективности РИВ от конверсии метана при различных значениях избытках серы
1 — избыток серы 73,37 + 4,0 mol/s; 2 — базовое значение серы 73,37 mol/s; 3 –значение серы 73,37 -4,0 mol/s
При увеличении избытка второго реаегнта селективность процесса возрастает.
Влияние температуры на селективность РИВ:
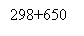
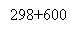
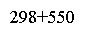
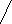


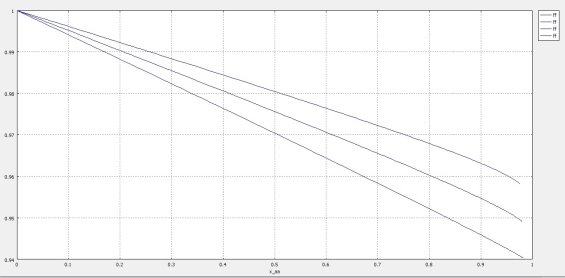
Рис. 7. График зависимости селективности РИВ от температуры
Селективность РИВ возрастает с повышением температуры процесса, что связано с большим (по модулю) значением энергии активации основной реакции, чем побочной.
Из графика зависимости удельной производительности РИВ от конверсии метана видно, что высокая удельная производительность при данной степени превращения может быть достигнута при использовании реактора РИВ, что соответствует тому, что для всех реакций с кинетическими уравнениями простого типа, имеющих суммарный порядок больше нуля, реакторы вытеснения наиболее производительны.
Реакция, протекающая в данном процессе — это необратимая реакция. Для данного процесса, чтобы получить высокую удельную производительность и селективность, выгодно проводить процесс в реакторе РИВ.
В ходе анализа были построены первичные кинетические кривые, был проведен анализ зависимостей удельной производительности и селективности реакции синтеза сероуглерода от параметров процесса.
В ходе анализа, увеличение температуры процесса свыше 650°С слабо влияет на удельную производительность реактора, поэтому повышение температуры не рекомендуемо, также повышение температуры ведет к понижению селективности процесса, что нежелательно. А также ведет к износу технологического оборудования
Было определено, что оптимальными условиями для проведения процесса являются — температура 600 о С в реакторе РИВ. Это позволит обеспечить высокую производительность и селективность процесса.
При оценке моделирования синтеза сероуглерода, можно сделать вывод, что наиболее выгодным будет использование реактора типа РИВ при высоких степенях конверсии.
Литература:
1 Пеликс, А. А. Химия и технология сероуглерода. / А. А. Пеликс, Б. С. Аранович, Е. А. Петров, Р. В. Котомкина. — Ленинград: Химия, 1986. — 224 с
2 Смуров, В. С. Производство сероуглерода. / В. С. Смуров, А. А. Аранович. — Ленинград: Химия, 1966. — 267 с.
3 Лебедев, Н. Н. Теория химических процессов основного органического и нефтехимического синтеза / Н. Н. Лебедев, М. Н. Манаков, В. Ф. Швец; под ред. Н. Н. Лебедева. — 2-е изд. перераб. — Москва: Химия, 1984. — 376 с.
4 Огородников, А. С. Моделирование в среде MatLab COMSOL 3.5a. Часть 1 / А. С. Огородников. — Томск: Изд-во ТПУ, 2012. — 104 с.







