Показана возможность потенциометрического определения ряда лекарственных средств с применением жидкостных ионоселективных электродов на основе алкалоидов. Изучено влияние состава мембраны, природы внутреннего раствора сравнения, селективности на функционирование жидкостных ионоселективных электродов, определены основные аналитические характеристики, приведены конкретные методики для анализа реальных объектов с различным сроком хранения.
Введение.
Определение фармпрепаратов в плане оценки содержания основного компонента очень важная аналитическая задача. Хорошо известно насколько серьезно стоит эта проблема в настоящее время, так как на рынок фармпрепаратов, к сожалению, попадают целые партии фальсифицированных, просроченных, некондиционных препаратов, далеких от требований Государственной Фармакопеи, что часто приводит к весьма плачевным результатам в лечебной практике. Среди лекарственных средств очень весомую (если несказать большую) часть составляют алкалоидсодержащие препараты. Поэтому исследования в области создания новых способов и методов определения содержания алкалоидов в различных лекарственных формах весьма актуальны, особенно, с привлечением современных инструментальных методов, обеспечивающих точность и объективность анализа [1]. В литературе имеются сведения о применении для этих целей потенциометрии. В основном работы касаются описания пленочных и твердоконтактных электродов различной конструкции. В настоящее время весьма перспективным, с нашей точки зрения, является метод потенциометрии с применением жидкостных ионоселективных электродов (ЖИСЭ), и, в частности, потенциометрическое титрование [2]. Возможности этого метода существенно расширяются с применением в качестве ионообменников ионных ассоциатов на основе алкалоидов.
Целью работы стало создание и исследование ЖИСЭ для определения ряда фармацевтических препаратов на основе алкалоидов, оптимизация методик определения и выработка рекомендаций для оценки содержания основного компонента в различных лекарственных формах.
Экспериментальная часть.
Все исследования основаны на потенциометрических измерениях (прямая потенциометрия и потенциометрическое титрование) в ячейке с использованием жидкостного ионоселективного электрода в качестве индикаторного. Установка для титрования представляла собой иономер универсальный марки «ЭВ-74» с магнитной мешалкой. В качестве вспомогательного электрода применен хлоридсеребряный электрод марки ЭВЛ-1М3, заполненный насыщенным раствором хлорида натрия. Использование хлорида натрия вместо хлорида калия связано с тем, что тетрафенилборат натрия (ТФБNa), используемый в качестве титранта и противоиона в мембране, является эффективным осадителем ионов К+, что может внести погрешности в анализе.
Жидкостные ионоселективные электроды (ЖИСЭ) изготавливали по известной методике [3]. Корпусом ЖИСЭ служили полиэтиленовые конусообразные капилляры, основание которых плотно заполнено порошкообразным фторопластом, пропитанным раствором электродноактивного вещества (ЭАВ) в нитробензоле. В электрод помещали 0,1–0,2 мл ЭАВ и внутренний водный раствор сравнения, в качестве которого использовался водный раствор ТФБNa с концентрацией 1·10–3 М. Электродноактивным веществом служил нитробензольный экстракт ионного ассоциата тетрафенилбоата натрия с фармпрепаратами. Были изготовлены и исследованы серии из 3–5 электродов каждого вида с мембранами на основе комплексов: 1 — тетрафенилборат тетрабетиламония (ТФБ-ТБА+), 2 — тетрафенилборат с папаверином, 3 — тетрафенилборат с дибазолом, 4 — тетрафенилборат с но-шпой. Титрантом при потенциометрическом определении содержания фармацевтического препарата служил водный раствор ТФБNa [4].
Используемые реактивы.
Тетрафенилборат натрия ((С6Н5)4ВNа) водный 0,01 М раствор (ТФБNa). Для приготовления 0,01 М раствора 3,4228 г ТФБNa марки “хч” растворяли в 1 л дистиллированной воды. Точную концентрацию полученного раствора устанавливали потенциометрическим титрованием стандартным раствором АgNO3 с использованием в качестве индикаторного аргентитового электрода.
Тетрабутиламмония бромистый ((С4H9)4NBr) водный 0,01 М раствор (ТБАBr). Для приготовления 0,01 М раствора 3,2223 г ТБФBr марки “хч” растворяли в 1 л дистиллированной воды.
Электродноактивные вещества — растворы тетрафенилбората тетрабутиламмония, тетрафенилбората с папаверином, тетрафенилбората с дибазолом, тетрафенилбората с но-шпой в нитробензоле с концентрацией 1·10–3 моль/л.
Водные растворы фармацевтических препаратов: но-шпа, дибазол, папаверин, димедрол, — готовили из субстрата, содержащего, согласно ГФ, 96–98 % основного вещества. Исходные растворы готовились с концентрацией порядка 1·10–2–1·10–3 моль/л. Растворы меньших концентрацией (1·10–3–1·10–6 М) готовили последовательным разбавлением.
Результаты и обсуждения.
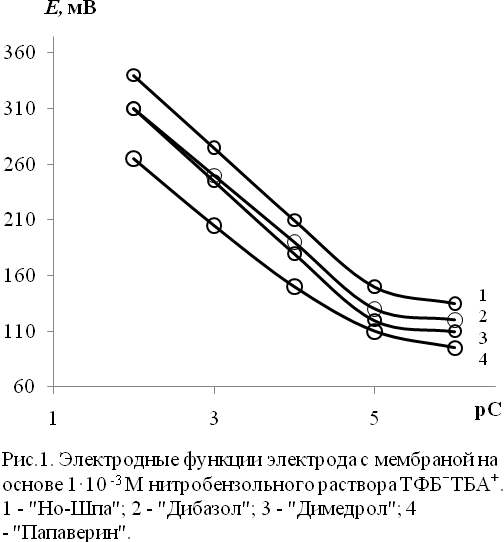
Исследовались следующие характеристики электродов: крутизна электродной функции (S мВ/рС), интервал концентраций, в котором функция Е = f(pC) линейна, и предел обнаружения (Сmin, M). Основные функции исследуемого электрода на основе нитробензольного комплекса тетрафенилбората тетрабутиламмония по отношению к ряду фармацевтических препаратов (папаверин, дибазол, но-шпа, димедрол) приведены на рис.1.
Аналогично были исследованы функции электродов на основе 1·10–3 мольных растворов на основе терафенилботата папаверина, тетрафенилбората дибазола, тетрафенилбората но-шпы. Предел обнаружения (Сmin) оценивали по градуировочной зависимости, как отклонение от линейности на величину Slg2 [5].
Градуировочные зависимости потенциала Е от рС для электродов с другими мембранами не приводим, так как они очень близки к вышеприведенным, а конкретные величины сведены в таблицу 1.
Таблица 1
Характеристики ЖИСЭ с мембранами на основе тетрафенилборатных комплексов (n = 3, р = 0,95)
|
Характеристика |
Тип мембраны* |
Определяемое вещество |
|||
|
Но-Шпа |
Дибазол |
Димедрол |
Папаверин |
||
|
S, мВ/рС |
1 2 3 4 |
57,9±2,8 59,0±3,0 57,2±1,9 60,1±2,5 |
61,3±1,8 58,2±2,6 57,9±1,3 61,6±3,1 |
61,3±1,5 60,1±2,8 61,0±2,1 58,5±3,2 |
59,1±2,3 59,1±2,1 59,9±2,8 60,2±1,9 |
|
Сmin, моль/л |
1 2 3 4 |
5·10¯⁶ 5·10¯⁶ 5·10¯⁶ 1·10¯⁶ |
5·10¯6 5·10¯⁶ 1·10¯⁶ 5·10¯⁶ |
1·10¯⁶ 1·10¯⁶ 1·10¯⁶ 5·10¯⁶ |
1·10¯⁶ 1·10¯⁶ 5·10¯⁶ 1·10¯⁶ |
|
E = f (pC) (ЛГГ) |
1 2 3 4 |
2–4,5 2–5 2–4 2–5 |
2–5 2–5 2–4,5 2–4 |
2–5 2–5 2–4,5 2–4 |
2–5 2–5,5 2–4 2–5 |
* 1 — ТФБ-ТБА+; 2 — ТФБ с папаверином; 3 — ТФБ с дибазолом; 4 — ТФБ с но-шпой.
Как видим из данных, приведенных на рис.1 и табл.1, крутизна электродных функций (S, мВ/рС) близка к теоретической нернстовской величине и составляет 59, 5 мВ/рС. Для этих же систем диапазон линейности электродной функции лежит в пределах от 2 до 5 рС и не отличается более, чем на 0,5 рС.
Тем самым показано, что как ионособственные, так и «классический» (на основе тетрафенилбората тетрабутиламмония) электроды могут успешно применяться для оценки содержания папаверина, дибазола, но-шпы и димедрола в водных растворах. С другой стороны, к сожалению, стоит констатировать, что мембраны равноселективны ко всем алкалоидам и при титровании смесей дадут лишь суммарную оценку.
Все электроды обладают схожими характеристиками, поэтому в дальнейшем исследовании использовали классический электрод на основе нитробензольного раствора ТФБ⁻ ТБА⁺.
Одним из основных результатов нашей работы стало определение папаверина, но-шпы, дибазола, димедрола в различных лекарственных формах, в том числе различного срока хранения. Так установлено, что для нескольких таблеток, взятых из одной упаковки, практически никогда не получается одинаковых результатов. Очевидно, что активный компонент в них распределен не равномерно. Кроме того, для одного и того же препарата, впущенного разными фирмами, также наблюдается разброс по содержанию основного вещества. Эти колебания тем больше, чем старше фармпрепарат, причем содержание действующего вещества уменьшается с увеличением срока хранения лекарственной формы (табл.2)
На рисунке 2 приведены кривые титрования но-шпы. Кривые титрования папаверина, дибазола и димедрола не приводим, так как они очень близки к вышеприведенным, а конкретные величины сведены в таблице 2.
Показано, что содержание основного вещества в фармпрепарате как правило уменьшается с увеличением срока хранения. Это хорошо оценивается по уменьшению величины эквивалентного объема при титровании, хотя погрешность определения при этом не увеличивается и находится в границах определенных требованиями ГФ и даже существенно меньше. Изменения в составе препарата при хранении также отчетливо видны при анализе кривых титрования: скачок титрования (или общее изменение потенциала) уменьшается с увеличением срока хранения препарата. Проводя несложные расчеты по оценке содержания основного вещества в фармпрепарате, можно сделать вывод, что за 8 лет хранения «Но-Шпы» содержание основного вещества уменьшилось на 5 %, а за 13 лет хранения на 37 %. То есть вряд ли такой препарат можно рекомендовать к продаже и применению в лечебных целях.
Данные по другим фармпрепаратам приведены в таблице 2.
Таблица 2
Результаты потенциометрического определения некоторых фармпрепаратов в таблетках с различным сроком хранения (Vпробы = 20 мл; Ст = 10 Сф.п.; п=3; р=0,95)
|
Фармпрепарат |
Допустимо по ГФ, мг |
Срок хранения |
Определено, мг |
Sr |
|
Но-шпа |
40,0±4,0 |
меньше 1 года 8 лет 13 лет |
40,1±0,5 38,1±1,0 25,1±1,5 |
0,01 0,01 0,06 |
|
Папаверин |
40,0±4,0 |
меньше 1 года 7 лет 13 лет |
39,8±0,5 34,4±1,9 29,7±2,3 |
0,01 0,02 0,07 |
|
Дибазол |
20,0±2,0 |
меньше 1 года 6 лет 20 лет |
19,6±1,1 17,1±1,2 7,4±0,5 |
0,05 0,03 0,05 |
|
Димедрол |
50,0±5,0 |
меньше 1 года 2 года 5 лет |
50,6±2,4 49,7±1,2 45,9±1,4 |
0,03 0,03 0,03 |
Выводы
Итак, нами изготовлены и исследованы электроды на основе тетрафенилбората тетрабутиламмония, тетрафенилбората папаверина, тетрафенилбората дибазола, тетрафенилбората но-шпы. Показано, что они имеют вполне удовлетворительные характеристики (крутизна электродной функции близка к нернстовской, линейность электродной функции составляет не менее трех единиц рС, минимально определяемая концентрация 1·10–6 моль/л).
Показана возможность определения ряда алкалоидов (папаверина, дибазола, но-шпы, димедрола) как в водных растворах, так и в конкретных лекарственных формах (инъекции, таблетки), в том числе с различным сроком хранения. Методики не требуют предварительного разделения или других подготовительных операций при анализе. Кроме того, методика достаточно проста, экспрессна (на одно определение требуется не более 10 минут), погрешность определения не более 10 % (Sr).
Литература:
Харитонов С. В. Ионоселективные электроды для определения лекарственных веществ // Успехи химии. 2007. Т.76, № 4. С.398–432
Головнев Н. Н., Новиков Г. В., Головнева И. И. Ионоселективные электроды в анализе лекарственных препаратов //Нано- и микросистемная техника. 2001. № 10. С.4
Гурьев И. А., Калугин А. А., Гущина Е. А.//Заводская лаборатория.1980. Т.46. № 6. С.497.
Гурьев И. А., Лизунова Г. М., Коренман И. М., Медведева О. Н.// Журнал аналитической химии. 1981. Т.36. № 1. С.130.
Камман К. Работа с ионоселективными электродами. — М.: — 1980. — 280 с.