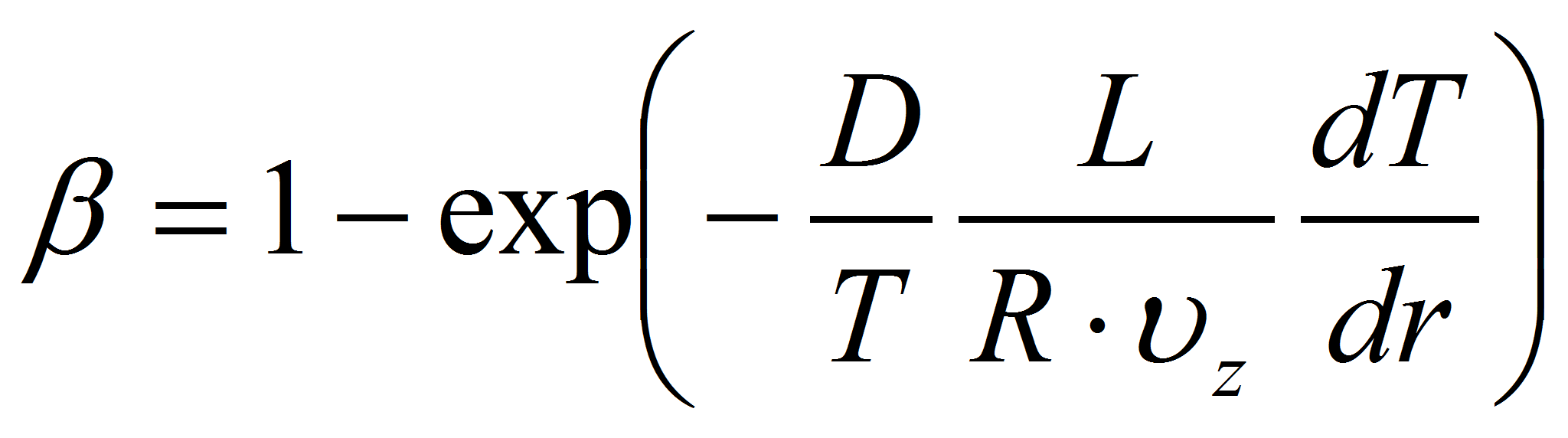В значительной части месторождений природного газа и нефти содержится сероводород, переработка которого сопряжена со значительными трудностями. Вместе с тем, сероводород является одним из наиболее перспективных источников производства серы и водорода. Это обусловлено большими природными запасами сероводорода и тем, что термодинамически водород в молекуле сероводорода сравнительно слабо связан:
H2S
→ H2
+ Sтв;
ΔН![]() =
0,25 кВт·ч/м3.
=
0,25 кВт·ч/м3.
Традиционные процессы получения серы из сероводорода, в том числе наиболее распространенный процесс Клауса, представляют собой различные исполнения процесса неполного окисления, описываемого реакцией:
Принципиальным недостатком этих методов является то, что в качестве целевого продукта получается только элементарная сера, а водород превращается в воду, где он связан гораздо сильнее.
В настоящее время возрастает потребность в целевом производстве водорода как в связи с существенным углублением переработки нефти, так и в связи с расширением ее добычи. Потребность НПЗ в водороде удовлетворяется за счет производства его как побочного продукта в процессах каталитического риформинга бензина на 50–55 % [1].
Процесс полного разложения сероводорода на водород и серу является эндотермическим (энтальпия реакции при комнатной температуре составляет 0,25 кВт ч/м3 H2S) и для эффективного разложения H2S требуются температуры 1500 ÷ 2000 K. Такой нагрев возможен лишь в плазменных реакторах. Важнейшей характерной чертой и одновременно преимуществом плазмохимических систем является их высокая энергонапряженность и удельная производительность, т. е. мощность и производительность на единицу реакционного объема.
Мощность современных генераторов плазмы — плазмотронов при сравнительно небольших габаритах достигает 10 МВт. При этом удельная производительность газофазных плазмохимических процессов может составлять до 10 м3/ч газа — продукта на 1 см3 активного объема плазмы, что значительно превышает соответствующий показатель традиционных химико-технологических процессов. Так для процесса аминовой очистки на 1 см3 объема абсорбера расход газа составляет 0,3–0,5 м3/ч.
При практической реализации плазмохимических методов на первый план выступает проблема минимизации энергозатрат на получение полезного продукта, т. е. оптимизация процесса в целях достижения высокой энергетической эффективности.
Под энергетической эффективностью (КПД) понимают отношение термодинамически минимальных энергозатрат процесса к реальным затратам энергии, вкладываемой в разряд для получения продукта. Эта задача является, в настоящее время, одной из важнейших и наиболее общих задач плазмохимии [2].
На базе плазмохимического разложения сероводорода возможно создание безотходной экологически чистой технологии его переработки. Твердые и жидкие отходы в процессе переработки не образуются. После разложения в продуктах присутствуют сера в жидком или газообразном состоянии, водород и остатки неразложившегося сероводорода. Сера отделяется конденсацией. Водород легко может быть выделен из газообразных продуктов как традиционными методами, например, аминовым, так и с применением полимерных мембран, а оставшийся сероводород возвращают на вход установки.
Исследование диссоциации сероводорода проводилось при давлении 100 ГПа. Мощность Wn, поглощаемая плазмой равнялось 1,2 кВт. Полученные результаты показали, что минимальные энергозатраты на образование молекулы водорода составляют 0,85 кВт·ч/м3 Н2 при степени диссоциации сероводорода α = 45 %. Эксперименты с СВЧ — разрядом проводились на частоте 2,45 ГГц при мощности генератора до 2 кВт. Тангенциальная составляющая скорости газа, поступающего в разрядную зону, υφ ~ 3·104 см/с. Средняя мощность, поглощаемая разрядом 1,2 кВт, давление в плазмотроне — 50–1 00 ГПа, расход сероводорода 0,15–0,5 л/с. Степень диссоциации сероводорода определялась с помощью газоанализатора. При минимальных энергозатратах 0,7 эВ/мол степень диссоциации составила 45 %. Максимально достигнутая степень диссоциации сероводорода составила 80 %. Мощность генератора составляла 4 кВт, частота — 40 МГц, расход плазмообразующего газа был 0, 1 5–0,4 л/с при давлении 100 ГПа. Сероводород подавался в разряд тангенциально со скоростью вращения, близкой к скорости звука. Достигнутая максимальная величина энергозатрат составляла 1 эВ/мол, максимальная степень конверсии близка к 100 %.
Механизм процесса: если процесс квазиравновесный, т. е. имеет место установление химического равновесия при данной температуре на первой стадии и стабилизация продуктов при охлаждении — на второй, то энергетические параметры процесса можно охарактеризовать с помощью понятий абсолютной и идеальной закалки. Абсолютная закалка предполагает сохранение количества продукта при охлаждении. Идеальная закалка предполагает сохранение степени разложения. Идеальная закалка лучше, чем абсолютная отражает особенности процесса. Однако различие степени конверсии и энергозатрат, рассчитанных для случаев абсолютной и идеальной закалки, невелико, так как мала концентрация радикалов (Н, S, HS).
Основные потери энергии в квазиравновесном процессе с последующей абсолютной или идеальной закалкой заключаются в нагреве газа и в энергии, выделяющейся при рекомбинации молекул S2 до S8 и конденсации в твердую серу.
Был предложен механизм неравновесности, обусловленный быстрым выносом тяжелых молекул и зародышей конденсированной фазы (кластеров) из активной зоны на периферию. Такой вынос эффективно происходит в поле центробежных сил благодаря тангенциальной подаче газа при условии
где m — масса S2; υφ — тангенциальная составляющая скорость потока H2S по радиусу реактора; T — средняя температура высокотемпературной зоны; R и L — радиус и длина активной зоны; Mz — число Маха для продольного движения газа; λ — длина свободного пробега молекулы.
Доля серы, выносимая к стенке за время пребывания газа в высокотемпературной зоне, равна
где D — коэффициент температуропроводности; υz — продольная скорость газа, снижается по мере увеличения расхода газа.
Таким образом, центробежный эффект повышает устойчивость продуктов по отношению к обратным реакциям и снижает затраты энергии на получение продукта [3, 4]. Важным фактором, влияющим на степень разложения сероводорода, является время охлаждения газовой смеси.
Экспериментально исследовано термическое разложение сероводорода в проточном реакторе при температурах от 600 до 1300 °С. Результаты опытов показали, что разложение сероводорода начинается при температуре 600 °С, однако, заметно сероводород разлагается при температуре свыше 800 °С. Вследствие обратимости реакции разложения сероводорода степень разложения представляет собой суммарный результат двух противоположно направленных процессов. В целях уменьшения протекания обратной реакции была увеличена скорость охлаждения газовой смеси, что позволило увеличить степень разложения сероводорода.
Таким образом, наиболее важным фактором основании полученных экспериментальных данных, определяющим степень разложения сероводорода, является время охлаждения газовой смеси после реакционной зоны. Кинетика разложения сероводорода при высоких температурах охлаждения (закалки), необходимая для стабилизации продуктов диссоциации.
Численно исследована диссоциация сероводорода в термической плазме на основе полного детального механизма этого процесса, включающего в себя как прямые, так и обратные реакции. Определены скорости охлаждения (закалки), необходимые для стабилизации продуктов диссоциации, и энергозатраты на получение водорода в термических плазмохимических системах. Были получены кинетические кривые, описывающие изменение концентраций реагентов в процессе разогрева со скоростью V=108·K·c-1 и установления термодинамического равновесия при конечной температуре Т=1700 K. Найдено, что характерное время диссоциации при 1700 K равно 5–10–3 с. Причем, указанное время значительно меньше характерного времени пребывания газа в плазмохимическом реакторе.
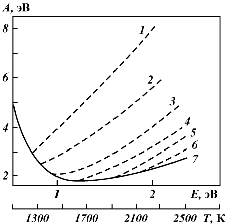
Получена зависимость удельных энергозатрат А на получение водорода от удельного энерговклада Е (и температуры разогрева) на основе термодинамического расчета [5].
Рис. 1.
Из графика на рис. 1 видно, что при скоростях охлаждения 107 K·с-1 во всем рассматриваемом диапазоне температур действительно наблюдается идеальная закалка, т. е. радикалы, полученные в процессе разогрева, рекомбинируют в продукты, повышая при этом выход водорода. Причем, при температурах, соответствующих минимальной величине энергозатрат (А = 1,8 эВ, Т = 1 700 K), охлаждение со сравнительно невысокими скоростями V= 104–105 K·с-1 достаточно для полной стабилизации продуктов диссоциации. Характерное отличие процесса разложения сероводорода от других процессов разложения, например, воды или углекислого газа, так как значительно облегчается эффективность организации этого процесса в плазме.
Рис. 1. Зависимость удельных энергозатрат на получение водорода от удельного энерговклада (температуры разогрева) при скорости охлаждения:1 — υ = 101 K·c-1; 2–102; 3–103; 4–104; 5–105; 6–106; 7–107 K·c-1
Кинетическая схема процесса дисоциации сероводорода представлена следующим образом:
H2S → H + HS — 4 эВ; (1)
H + H2S → H2 + HS + 0, 55 эВ; (2)
HS + HS →H2S + S + 0,39 эВ; (3)
S + H2S →H2 + S2 + 1,83 эВ. (4)
Вторичные реакции (2) — (4) являются быстрыми экзотермическими процессами с малыми энергиями активации, поэтому скорость процесса определяется лимитирующей стадией (1) с константой KI = 1025,9 Т-2 ехр (-46000/Т) см3·моль-1 с.
Обратные эндотермические реакции имеют высокие активационные барьеры, а скорость рекомбинации мала из-за малой концентрации радикалов. Для того, чтобы компенсировать затраты энергии на эндотермическую реакцию (1) надо проводить процесс с малыми добавками кислорода. При введении добавок кислорода в системе будут идти реакции наработки радикалов и продуктов. Суммарный процесс диссоциации сероводорода с малыми добавками кислорода представлен в виде
H2S + xO2 → (1–2x) H2 + 2xH2O + Sm;
ΔH298 К = 0,21–5,01x, эВ,
где x — количество молей кислорода, приходящихся на 1 моль H2S.
Литература:
Сорокин Я. Г. Особенности переработки сернистых нефтей и охрана окружающей среды. — М.: Химия, 1975. — 296 с.
Русанов В. Д., Фридман А. А. Физика химически активной плазмы. — М.: Наука, 1984.-415 с.
Потапкин Б. В. и др. // Тезисы докл. IV Всесоюзн. симпозиума по плазмохимии. — Днепропетровск, 1984. — Т. 214. — С. 320
Балебанов А. В., Бутылкин Б. А., Животов В. К. и др. Диссоциация сероводорода в плазме // ДАН СССР. — 1985. — Т. 283, N3. — С. 657– 660.