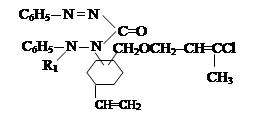
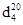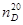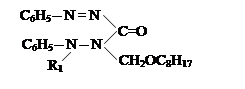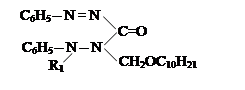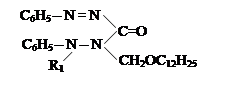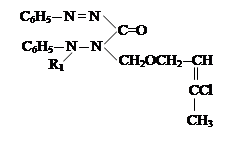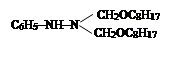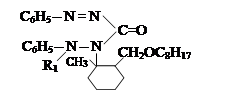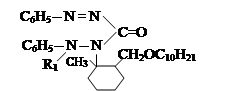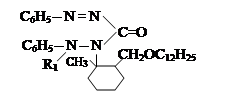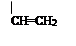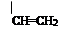На основе α-хлор-метил-алкил и -алкенил эфиров и хлоразона были синтезированы, ранее неизвестные в литературе, 12 новых производных дифенилкарбазона. На основании проведенного исследования было уста-новлено, что эти новые соединения даже при концентрации 2.5; 5; 10 мг/л обладают высокоэффективными свойствами ингибиторов.
Ранее нами на основе α- и γ-хлор-алкенил и алкилоксиметил эфиров были получены производные дифенилкарбазона и дифенилкарбазида, содержащие 4 атома азота и приведено их исследование в качестве ингибиторов защиты от коррозии металлов.
В связи с этим на основании продуктов реакции дифенилкарбазона с α-хлор-алкил и алкенилоксиметил эфирами, а так же на основе реакции этих эфиров с алкоксиметил-хлорированными 1-метил и 4-винилциклогексеном была проведена реакция с хлоразоном и были получены ранее неизвестные в литературе новые производные дифенилкарбазона, содержащие 7 атомов азота (условно названные нами новыми соединениями I – XII).
Во время исследовательских работ по определению ингибиторной активности новых соединений было установлено, что каждое из них по своей ингибиторной активности превосходит как взятый в качестве сырья для синтеза дифенилкарбазон, так и многие известные в литературе ингибиторные вещества.
Как видно из ранее проведенных исследований [1-3], замещение находящегося в составе аминового соединения атома водорода какой – либо функциональной группой, а так же с увеличением атомов азота, эти соединения даже при малой концентрации 2.5; 5; 10 мг/л увеличивают степень адсорбции на поверхности металла и тем самым делают коррозию пассивной.
Именно поэтому, проведение синтеза такого типа в различных направлениях и исследование его с целью дальнейшего применения считается очень актуальным в синтезе органической химии и нефтехимии.
Синтез новых соединений был проведен в несколько этапов.
I. На первом этапе на основе известных методов в литературе [4-7] был проведен синтез α-хлор-метил-алкил и алкенил эфиров.
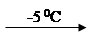
CH2O + ROH + HCl ROCH2Cl
где, R= –C8H17; –C10H21; –C12H25; –CH2–CH=CCl–CH3.
Состав и строение синтезированных эфиров были определены известными методами. Полученные результаты идентичны известным данным в литературе [1–7].
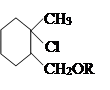
II. На втором этапе по известным способом в литературе [7] на основе α-хлор-метил-алкил и алкенил эфиров была проведена реакция алкоксиме-тилхлорирования 1-метилциклогексена:
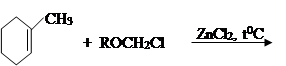 |
 |
||
где, R= –C8H17; –C10H21; –C12H25; –CH2–CH=CCl–CH3.
Структуры и составы синтезированных 1-метил-1-хлор-алкил и алкенило-ксиметилциклогексан эфиров были определены известными методами. Полученные результаты идентичны известным данным в литературе [7].
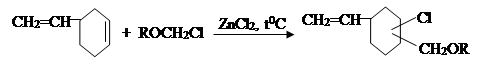 III. На третьем этапе на основе известных способов в литературе [7] была проведена реакция алкил и-алкенилоксиметилхлорирование 4-винилци-клогексена.
III. На третьем этапе на основе известных способов в литературе [7] была проведена реакция алкил и-алкенилоксиметилхлорирование 4-винилци-клогексена.
где, R= –C8H17; –C10H21; –C12H25; –CH2–CH=CCl–CH3.
Строение и структура синтезированных 1-винил-3,4(хлор, алкилокси-метил)циклогексанов и 1-винил-3,4[хлор,(2-хлор-5-оксогексен-2)] циклогек-сан эфиров были определены известными методами. Полученные резуль-таты идентичны известным данным в литературе [7].
IV. На четвертом этапе на основе известных способов в литературе [8] была проведена реакция α-хлор алкил и алкенилоксиметил эфиров с дифенилкарбазоном:
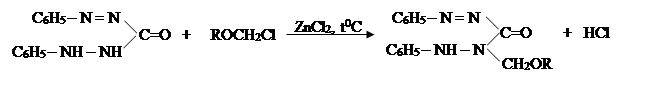 |
где, R= –C8H17; –C10H21; –C12H25; –CH2–CH=CCl–CH3.
Структуры и составы синтезированных соединений N1N5-дифенил-N4-ал-коксиметилкарбазоны и N1N5-дифенил-N4-(2-хлор-5-оксогексен-2)карбазон были определены известными методами. Полученные результаты идентичны известным данным в литературе [8].
V. На пятом этапе на основе известных способов в литературе [9-10] была проведена реакция дифенилкарбазона с соединениями алкоксиметилхлорированых 1-метилциклогексенами.
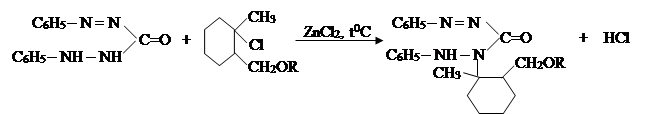
где, R= –C8H17; –C10H21; –C12H25; –CH2–CH=CCl–CH3.
Строение и составы синтезированных соединений 1-метил-1-дифенил-карбазон-2-алкоксиметил-1-циклогексана были определены известными методами.
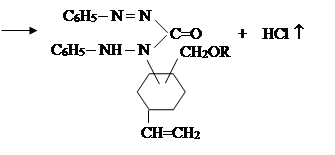
VI. На шестом этапе на основе известных способов в литературе [11] была проведена реакция 1-винил-3,4(хлор, алкилоксиметил)циклогексанов с дифенилкарбазоном:
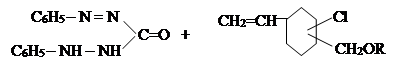 |
|||||
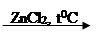 |
|||||
 |
|||||
где, R= –C8H17; –C10H21; –C12H25; –CH2–CH=CCl–CH3.
Строение и составы синтезированных соединений 1-винил-3,4(дифе-нилкарбазон, алкоксиметил)циклогексанов были определены известными методами.
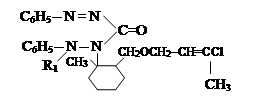
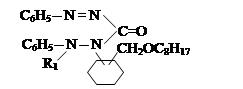
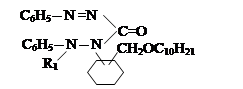
VII. На седьмом этапе была проведена реакция соединений алкил и алкенилоксиметил-дифенилкарбазона с хлоразоном:
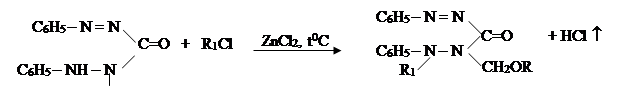 |
CH2OR
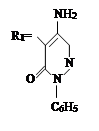 |
где, ; R= –C8H17(I); –C10H21(II); –C12H25 (III), –CH2–CH=CCl–CH3 (IV).
VIII. На восьмом этапе была проведена нижеследующая реакция соединений 1-метил-2-алкил и 2-алкенилоксиметилциклогексанов с хлоразоном:
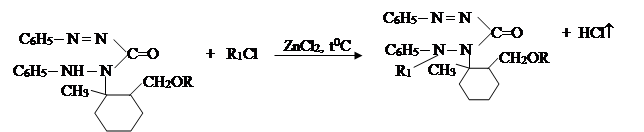 |
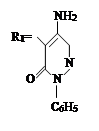 где, ; R= –C8H17(V); –C10H21(VI); –C12H25 (VII),
где, ; R= –C8H17(V); –C10H21(VI); –C12H25 (VII),
–CH2–CH=CCl–CH3 (VIII).
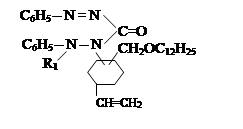
IX. На девятом этапе была проведена реакция соединений 1-винил-3,4-алкоксиметилциклогексанов-дифенилкарбазона с хлоразоном:
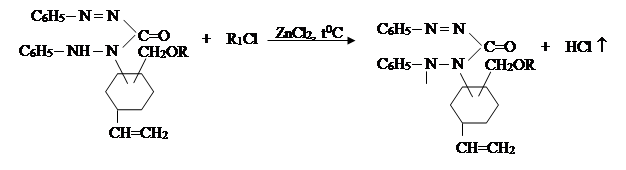
R1
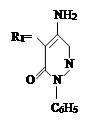 |
где, ; R= –C8H17(IX); –C10H21(X); –C12H25 (XI),
–CH2–CH=CCl–CH3 (XII).
Процентный выход, физико-химические константы и элементный анализ неизвестных в литературе новых 12 производных дифенилкарбазона (соединения I-XII) приведены в табл. 1.
В целях определения степени ингибиторной эффективности новых синтезированных соединений I–XII в лабораторных условиях были созданы сильно коррозионные среды и при различной концентрации соединений испытание проводилось на стали марки 3. Испытание проводилось в течение 3-х часов при температуре 40–45 0С. Определение ингибиторной эффективности проводилось известным в литературе [12] «гравиметрическим» методом по потере массы металла.
Результаты определения ингибиторной эффективности соединений I–XII приведены в табл. 2.
Как видно из табл. 2, каждое из новых соединений I–XI даже при малой концентрации 2.5; 5; 10 мг/л по своей ингибиторной эффективности в значительной степени превышает известное в литературе [13] ингибиторное вещество, условно обозначенное нами А, даже при концентрации последнего 100; 200 мг/л.
Вероятнее всего, что высокая ингибиторная эффективность синтезированных новых соединений I–XII зависит от наличия и природы функциональных групп и кратной связи и от повышения плотности электронов в их составе. Новые синтезированные соединения способствуют образованию на поверхности стали комплекса между молекулой ингибитора и металлами создавая этим высокую адсорбцию и поверхность стали становится пассивной к коррозии.
И так, на основании проведенного исследования еще раз было установлено, что известные в литературе [14] органические соединения с функциональными группами и много атомами азота являются высокоэффективными ингибиторами коррозии.
Как видно из табл. 2 каждое из ранее неизвестных в литературе новых производных дифенилкарбазона (соединения I–XII) может использоваться в нефте-газодобывающей и перерабатывающей промышленности, в нефтехи-мии, а так же и в других направлениях и гарантировать высокую эффектив-ность защиты стального оборудования от коррозии.
Как видно из состава и строения новых неизвестных в литературе производных дифенилкарбазона (соединения I–XII) можно вести исследования для использования их в различных направлениях, поэтому синтез соединений такого типа, их исследование с целью дальнейшего применения считают очень актуальным в нефтехимии и химии органического синтеза.
Экспериментальная часть
Синтез N4-октоксиметил-N5-азон-N1,N5-дифенилкарбазона. В колбу для синтеза помещают 2 г ZnCl2, 22,25 г (0,1 г-моль) хлоразона, прибавляют 100 мл метилового спирта. При температуре 600С смесь перемешивается 1 час. Затем в смесь из капельной воронки периодически добавляется 38,2 г (0,2 г-моль) N4-октоксиметил-N1,N5-дифенилкарбазона. Перемешивание ведется 6 часов при температуре 650С. Затем при комнатной температуре смесь нейтрализуют 100 мл 10%-ного раствора NaOH и промывают несколько раз 200 мл дистиллированной воды. Органический слой извлекается диэтиловым эфиром. Отгоняют эфир, реакционный продукт сушат над СаСl2. Затем на вакуумой установке выделяют синтезированный N4-октоксиметил-N5-азон-N1,N5-дифенилкарбазона (I).
Синтез соединений N4-десоктоксиметил-N5-азон-N1N5-дифенилкарбазон (II), N4-ундоксиметил-N5-азон-N1N5-дифенилкарбазон (III) и N4-(2-хлор-5-оксогексен-2)-N5-азон-N1N5-дифенилкарбазон (IV) был проведен аналогично синтезу соединения I.
Составы и структуры синтезированных новых соединений I–IV установ-лены на основании данных элементного анализа, ИК и масс спектров.
В ИК спектре соединений I–IV проявляются полосы, характеризующие С-О-С простую эфирную группу 1050, 1080 см-1; СН2 группу 2950 см-1; СН3 группу 1380, 1460, 2960,3030 см-1; С-N связь 1310, 1350 см-1; N-N группу 900, 1580 см-1; в бензольном кольце С=С связь 1440, 1465, 1500, 1510, 1590-1600 см-1; С6Н5 группу 700–780 см-1; в группе азона С=С связь 1680 см-1; NH2 группу 550, 1570, 3300 см-1.
Наряду с указанными выше полосами в ИК спектре соединения IV проявляются интенсивные полосы в группе 2-хлор-5-оксогексен-2 С-Сl связь 680 см-1; С=С связь 1640 см-1.
В масс спектрах соединений I-IV было определено, что их молекулярным массам соответствуют молекулярные ионы 567 m/е, 595 m/е, 623 m/е и 543 m/е.
Синтез 1-N4-(1-метил-2-октоксиметил)циклогексан-N5-азон-N1,N5-дифенилкарбазона (IV). В колбу для синтеза помещают 2 г ZnCl2, 11,125 г (0,05 г-моль) хлоразона и 100 мл спирта СН3ОН. Смесь перемешивается при температуре 600С в течение 0,5 час до полного растворения хлоразона. Затем в смесь из капельной воронки периодически добавляется 23,85 г (0,05 г-моль) 1-N4-(1-метил-2-октоксиметил)циклогексан-N1N5-дифенилкарбазона и при температуре 650С перемешивание продолжается еще в течение 6 часов. Затем при комнатной температуре смесь нейтрализуют 100 мл 10 %-ного раствора NaOH и несколько раз промывают 200 мл дистиллированной воды. Органический слой извлекают диэтиловым эфиром. Затем отгоняют эфир, реакционный продукт сушат над СаСl2 и на вакуумой установке выделяют синтезированный 1–N4-(1-метил-2-октоксиметил)циклогексан-N4-азон-N1N5-дифе-нилкарбазона (IV).
Синтез соединений 1-N4-(1-метил-2-десоксиметил)циклогексан-N5-азон- -N1N5-дифенилкарбазона (VI), 1-N4-(1-метил-2-ундесоксиметил)циклогексан--N5-азон-N1N5-дифенилкарбазона (VII) и 1-N4-[1-метил-2(2-хлор-5-оксогек-сен-2)]циклогексан-N5-азон-N1,N5-дифенилкарбазона (VIII) был проведен аналогично синтезу соединения V.
Составы и структуры синтезированных новых соединений V–VIII были установлены на основании данных элементного анализа, ИК и масс спектров.
В ИК спектре соединений V-VIII проявляются полосы, характеризующие С–О–С простую эфирную группу 1050, 1080 см-1; СН2 группу 2950 см-1; СН3 группу 1380, 1460, 2960,3030 см-1; С-N связь 1310-1350 см-1; в группе азона NH2 группу 550, 1570, 3300 см-1; С=С связь 1680 см-1; в бензольном кольце С=С связь 1440, 1465, 1500, 1510, 1590-1600 см-1; С6Н5 группу 700- 780 см-1.
Наряду с указанными выше полосами в ИК спектре соединения VIII проявляются интенсивные полосы в группе 2-хлор-5-оксогексен-2 С-Сl связь 680 см-1; С=С связь 1640 см-1.
В масс спектрах соединений V-VIII было определено, что их молекулярным массам соответствуют молекулярные ионы 663 m/е, 691 m/е, 719 m/е и 639,5 m/е.
Синтез 3,4-N4-(1-винил-3,4-октоксиметил)циклогексан-N5-азон-N1,N5--дифенилкарбазона (IX). В колбу для синтеза помещают 2 г ZnCl2, 11,125 г (0,05 г-моль) хлоразона и 100 мл спирта СН3ОН. Смесь перемешивается при температуре 600С в течение 0,5 час до полного растворения хлоразона, затем в смесь из капельной воронки периодически подается 24,5 г (0,05 г-моль) 3,4-N4-(1-винил-3,4-октоксиметил)циклогексан-N1,N5-дифенилкарба-зона и при температуре 650С в течение 6 часов продолжается перемешивание. Затем при комнатной температуре смесь нейтрализуют 100 мл 10 %-ного раствора NaOH и несколько раз промывают 200 мл дистиллированной воды. Органический слой извлекают диэтиловым эфиром. Затем отгоняют эфир, реакционный продукт сушат над СаСl2 и на вакуумой получают синтезированный продукт 3,4-N4-(1-винил-3,4-октоксиметил)циклогексан-N5-азон-N1N5-дифе-нилкарбазона (IX).
Синтез соединений 3,4-N4-(1-винил-3,4-десоксиметил)циклогексан-N5-азон-N1N5-дифенилкарбазона (X), 3,4-N4-(1-винил-3,4-ундесоксиметил)цик-логексан-N5-азон-N1N5-дифенилкарбазона (XI) и 3,4-N4-[1-винил-3,4-(2-хлор-5-оксогексен-2)]циклогексан-N5-азон-N1N5-дифенилкарбазона (XII) был про-веден аналогично синтезу соединения IX.
Составы и структуры синтезированных соединений IX-XII были установлены на основании данных элементного анализа, ИК и масс спектров.
В ИК спектре соединений IX-XII проявляются полосы, характеризующие функциональную группу: СН2=СН винильную группу 910,990 см-1; С-О-С простую эфирную группу 1050, 1080 см-1; СН2 группу 2950 см-1; СН3 группу 1380, 1460, 2960, 3030 см-1; С-N связь 1310, 1350 см-1; N-N группу 900, 1580 см-1; в бензольном кольце С=С связь 1440, 1465, 1500, 1510, 1590-1600 см-1; С6Н5 группу 700-780 см-1; в группе азона С=С связь 1680 см-1; NH2 группу 550, 1570, 3300 см-1.
Наряду с указанными выше полосами в ИК спектре соединения XII проявляются интенсивные полосы в группе 2-хлор-5-оксогексен-2 С=С связь 1640 см-1; С-Сl связь 650 см-1.
В масс спектрах соединений IX–XII было определено, что их молекулярным массам соответствуют молекулярные ионы 675 m/е, 703 m/е, 731 m/е и 651,5 m/е.
СПИСОК ЛИТЕРАТУРЫ
1. Байрамов Г.И. Синтез новых азотсодержащих органических соединений на основе 2,6-дихлор-5оксогексен-2 эфира и их исследование. НАН Азербайджана. Азерб. хим. журн. №3. 2008. с.174
2. Байрамов Г.И. Синтез серо-, а также азот и серосодержащих новых органических соединений на основе 1-метил-1-хлор-2-октоксиметил-циклогексана. // Жур. Химические проблемы. НАН Азербайджана. №1. 2008. с.96
3. Байрамов Г.И. Синтез и исследование азотсодержащих новых органи-ческих соединений на основе 1,3-дихлорбутена-2. НАН Азербайджана. Азерб. хим. журн. №2. 2008. с.102
4. Исагулянц В.И. и др.1,3-дихлорбутен-2 и новые препараты на его основе. Жур. Успехи химии. Москва. 1964. m XXXIII. №1. С.55
5. Поконова Ю.В. химия и технология галоген эфиров – Л.: ЛГУ, 1982. с.243
6. Поконова Ю.В. Галлоиды эфиров. М.: Химия. 1966. С.57.
7. Байрамов Г.И. Дисс. …канд.хим.наук. Баку, ИНХП АН Азерб. ССР. 1988. с.80, 82, 90
8. Байрамов Г.И. Синтез новых соединений на основе α-хлор-алкоксиметила. НАН Азербайджана. Жур. Химические проблемы №4. 2008. с.625-630
9. Байрамов Г.И. Синтез и исследование новых дифенилкарбазидов на основе эфиров α-хлор-алкоксиметила, 2,6-дихлор-5-оксогексена-2 и 1-метилциклогексена и их исследование. НАН Азербайджана. Азерб. хим. журн. №4. 2008. с.114
10. Байрамов Г.И. Синтез новых азот - и серосодержащих органических соединений на основе эфиров 1-винил-3,4-(хлор, алкоксиметил)цик-логексанов и 2,6-дихлор-5-оксогексена-2 и проведение их исследований. Журнал научных публикаций аспирантов и докторантов №1. январь 2009 г. С.116
11. Байрамов Г.И. Синтез новых гуанидиновых органических соединений на основе эфиров α-хлор-алкоксиметила, 2,6-дихлор-5-оксогексена-2, 1-метил и 4-винилциклогексенов и их исследований. Вестник СамГУ – Естественнонаучная серия. 2008. №8/2/(67)
12. Жук Н.П. Курс коррозии и защита металлов. М.: Изд.Металлургия, 1968. С.361
13. Шихмамедбекова А.З., мамедьярова И.Ф., Байрамов Г.И., и др. N, N' – дифенил – N' октокситметил-гуанидина в качестве ингибитора коррозии стали в двухфазной системе. Автор. Свид. СССР, №1031141, 1983 г., А С07 С129/12; С23 F 11/14.
14. рачев Х., Стефанова С. Справочник по коррозии. М.: Мир, 1982. С.62
Таблица 1. Процентный выход, физико-химические константы и элементный анализ синтезированных новых производных дифенилкарбазона на основе α-хлор-метил-алкил и алкенил эфиров и хлоразона
|
Химическая формула соединения и условный номер |
Выход, % |
Ткип, 0С (мм рт.ст) |
|
|
MRD найдено вычислено |
Брутто формула, мол. вес |
Элементный анализ, % Вычислено/ Найдено |
|||
|
C |
H |
N |
Cl |
|||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
I |
97.56 |
187–188 (2) |
1.0436 |
1.5295 |
167.69 167.5 |
C32H37O3N7 567 |
67,72 67,56 |
6,52 6,34 |
17,28 17,11 |
– |
|
II |
97.54 |
192–193 (2) |
1.0485 |
1.5361 |
176.97 176.79 |
C34H41O3N7 595 |
68,57 68,38 |
6,89 6,72 |
14,12 13,94 |
– |
|
III |
97.57 |
198–199 (2) |
1.0521 |
1.5417 |
186.27 186.09 |
C36H45O3N7 623 |
69,34 69,16 |
7,22 7,04 |
13,48 13,31 |
– |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|||
|
IV |
96.48 |
214-215 (2) |
1.1927 |
1.5884 |
153.43 153.25 |
C28H26O3N7Cl 543,5 |
61,82 61,65 |
4,78 4,61 |
15,46 15,30 |
6,53 6,34 |
|||
|
V |
98.64 |
208–209 (2) |
1.0638 |
1.5487 |
198.15 197.97 |
C39H49O3N7 663 |
70,59 70,41 |
7,39 7,22 |
12,67 12,50 |
– |
|||
|
VI |
98.59 |
216–217 (2) |
1.0679 |
1.5543 |
207.46 207.27 |
C41H53O3N7 691 |
71,20 71,01 |
7,67 7,48 |
12,16 11,98 |
– |
|||
|
VII |
98.67 |
225–226 (2) |
1.0725 |
1.5599 |
216.74 216.56 |
C43H57O3N7 719 |
71,77 71,59 |
7,93 7,75 |
11,68 11,46 |
– |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|||
|
VIII |
97.89 |
232–233 (2) |
1.2125 |
1.6147 |
183.99 183.72 |
C35H38O3N7Cl 639.5 |
65,68 65,52 |
5,94 5,75 |
13,14 12,95 |
5,55 5,32 |
|||
|
IX |
98.58 |
214–215 (2) |
1.0646 |
1.5512 |
202.32 202.14 |
C40H49O3N7 675 |
71,11 70,92 |
7,26 7,05 |
12,44 12,22 |
– |
|||
|
X |
98.72 |
222–223 (2) |
1.0692 |
1.5569 |
211.62 211.43 |
C42H53O3N7 703 |
71,69 71,52 |
7,54 7,36 |
11,95 11,78 |
– |
|||
|
XI |
|
231–232 (2) |
1.0737 |
1.5623 |
220.88 220.69 |
C44H57O3N7 731 |
72,23 72,04 |
7,80 7,64 |
11,49 11,27 |
– |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
XII |
96.96 |
237–238 (2) |
1.2135 |
1.6179 |
188.07 187.89 |
C36H38O3N7Cl 651,5 |
66,31 66,14 |
5,83 5,65 |
12,89 12,72 |
5,45 5,22 |
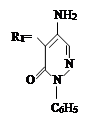
где,
Таблица 2. Показатели результатов исследования ингибиторной эффективности синтезированных новых производных дифенилкарбазона
|
Условный номер соединения |
Концентрация ингибитора, мг/л |
3% NaCl+нефт (10:1) H2S 500 мг/л |
0.3 N HCl +бензин (1:7) H2S 1000 мг/л |
||
|
Скорость коррозии, г/см2 ·час |
Эффек-тивность ингиби-тора, % |
Скорость коррозии, г/см2 ·час |
Эффективность ингибитора, % |
||
|
Без ингибитора |
– |
2.56 |
– |
3.65 |
– |
|
I |
2.5 5 10 |
0.0018 0.0006 – |
99.92 99.97 100 |
0.0007 0.0002 – |
99.98 99.99 100 |
|
II |
2.5 5 10 |
0.0012 0.0004 – |
99.95 99.98 100 |
0.0002 0.0001 – |
99.99 100 |
|
III |
2.5 5 10 |
0.0009 0.0002 – |
99.96 99.99 100 |
0.0002 – |
99.99 100 |
|
IV |
2.5 5 10 |
0.0004 – |
99.98 100 |
0.0001 – |
100 |
|
V |
2.5 5 10 |
0.0011 0.0003 – |
99.96 99.98 100 |
0.0005 0.0001 – |
99.98 100 |
|
VI |
2.5 5 10 |
0.0008 0.0002 – |
99.96 99.99 100 |
0.0002 – |
99.99 100 |
|
VII |
2.5 5 10 |
0.0006 0,0001 – |
99.97 100 |
0.0001 – |
100 |
|
VIII |
2.5 5 10 |
0,0002 – |
99,99 100 |
– |
100 |
|
IX |
2.5 5 10 |
0,0008 0,0001 – |
99,96 100 |
0.0002 0.0001 – |
99.99 100 |
|
X |
2.5 5 10 |
0,0004 – |
99,98 100 |
0.0001 – |
100 |
|
XI |
2.5 5 10 |
0,0001 – |
100 |
– |
100 |
|
XII |
2.5 5 10 |
– |
100 |
– |
100 |
|
А [13] |
200
|
|
98.5 |
|
98 |