Введение
Наночастицы меди, обладающие такими свойствами, как дешевизна, низкая токсичность, стабильность и проводимость, применяются в различных областях, таких как катализ, биомедицина и в качестве антибиотика, грибков... Однако недостатком традиционных физико-химических методов синтеза наночастиц меди является склонность к ее окислению с образованием Cu 2 O и CuO [1]. Исследования показали, что использование растительных экстрактов в качестве восстановителей Cu 2+ при диспергировании наночастиц на наноматериалах Fe 3 O 4 может предотвратить окисление Cu в соответствующие оксиды. Кроме того, использование Fe 3 O 4 в качестве носителя также облегчает извлечение материала благодаря его магнитным свойствам. Показано, что материалы Cu/Fe 3 O 4 , синтезированные методами зеленой химии, обладают хорошей каталитической активностью, антиоксидантным и противораковым действием... [1–3].
Текстильная промышленность играет крайне важную роль в развитии глобальной экономики. Однако это также отрасль с высоким риском загрязнения окружающей среды, особенно сточные воды текстильных производств, в которых содержится большое количество остаток волокон, грязевых частиц, реагентов, поверхностно-активных веществ, красителей. На сегодняшний день существует множество методов очистки водных ресурсов, таких как биохимического окисления, адсорбции, ионного обмена, фоторазложения... Из всех специальных методов очистки воды, метод восстановления пигментов до нейтральной, бесцветной и нетоксичной формы привлекает внимание многих исследователей во всем мире [4].
Цель настоящей работы — синтез наноматериалов Cu/Fe 3 O 4 из экстракта листьев зеленого чая и применение в качестве катализатора восстановления метиленового синего.
Экспериментальная часть
Синтез материалов Fe 3 O 4 : Добавили 0,02 моль Fe 3+ и 0,01 моль Fe 2+ в стакан, содержащий 100 мл дистиллированной воды. Смесь перемешивали магнитной мешалкой при 70 °C, затем к ней медленно добавили 400 мл раствора NaOH 2 M. Полученный осадок извлекали с помощью магнитов, промывали и сушили при 60 °С в течение 4 часов, для получения Fe 3 O 4 .
Синтез материалов Cu/Fe 3 O 4 : Экстракт получили при нагревании 10 г листьев зеленого чая в 200 мл дистиллированной воды при 100 °C в течение 40 мин. Поместили 0,01 г Fe 3 O 4 в стеклянный стакан, содержащий 10 мл дистиллированной воды, и обрабатывали ультразвуком в течение 15 мин, чтобы создать суспензию Fe 3 O 4 в воде. Добавили в суспензии 50 мл раствора CuSO 5 4 ммоль/л, затем 6 мл экстракта, помешали смесь магнитной мешалкой при 40 o С в течение 20 мин. Полученный осадок извлекали с помощью магнитов, промывали и сушили при 60 °С в течение 4 часов, для получения Cu/Fe 3 O 4 .
Структуры, морфология, химический состав Fe 3 O 4 и Cu/Fe 3 O 4 были исследованы методами XRD, SEM, EDX.
Адсорбция метиленового синего (MB) : добавили 4 мг адсорбента в коническую колбу с 50 мл раствора MB 20 мг/л. Перемешали смесь магнитной мешалкой в течение 10–60 мин. Через каждые 10 мин отсасывали примерно 3 мл раствора и измерили оставшуюся концентрацию MB в растворе с помощью фотометрического метода. После завершения фотометрических измерений раствор сливали обратно в колбу.
Катализ восстановления метиленового синего NaBH 4 : К смешанному раствору МB и катализатора, достигшему адсорбционного равновесия, добавили 1 мл раствора 0,2 M NaBH 4 и 1,5 M NaOH. Перемешали смесь магнитной мешалкой в течение 20 мин. Через каждые 4 мин отсасывали примерно 3 мл раствора и измерили оставшуюся концентрацию MB в растворе. После завершения фотометрических измерений раствор сливали обратно в реакционную колбу.
Обсуждение результатов
1. Синтез Cu/Fe 3 O 4
Рентгеновские дифрактограммы (XRD) образцов Fe 3 O 4 и Cu/Fe 3 O 4 представлены на рис. 1.
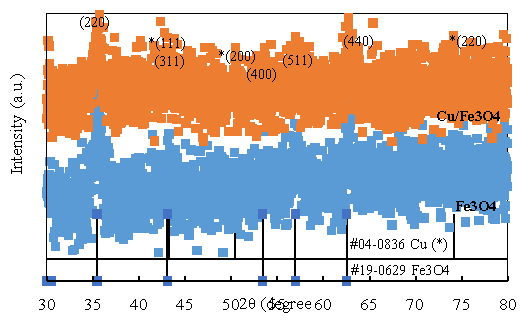
Рис. 1. Дифрактограммы образцов Fe 3 O 4 и Cu/Fe 3 O 4
Из рис. 1 видно, что на дифрактограммах образцов появляются характерные пики для Fe 3 O 4 в положениях 35,4 o ; 43,1 о ; 53,4 о ; 56,9 о ; 63,1 o , соответствующие граням кристалла (220), (311), (400), (511) и (440), в соответствии с базой данных JCPDS 19–0629. На дифрактограмме образца Cu/Fe 3 O 4 помимо типичных пиков для Fe 3 O 4 присутствуют также характерные пики для Cu в положениях 43,3 o ; 50,4 о и 74,1 о , соответствующие граням кристалла (111), (200) и (220), в соответствии с базой данных JCPDS 04–0836. Образование Cu можно объяснить тем, что экстракт листьев зеленого чая содержит полифенолы, способные восстанавливать Cu 2+ до Cu [1].
EDX-спектр образца Cu/Fe 3 O 4 , синтезированного методом восстановления Cu 2+ в суспензионном растворе Fe 3 O 4 с экстрактом листьев зеленого чая, представленный на рис. 2, показывает наличие элементов Fe, Cu, O и C.
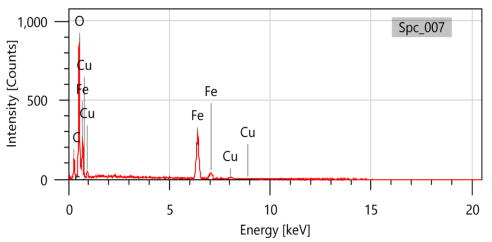
Рис. 2. EDX-спектр материала Cu/Fe 3 O 4
Результаты определения элементного состава показывают, что помимо основных компонентов Fe и O в образце присутствует также небольшое количество Cu (около 2 %). В частности, образец также содержит элемент С в относительно большой концентрации (21,83 %). Это означает, что полученный материал окружен органическими веществами, содержащимися в экстракте.


Рис. 3. Изображения SEM материалов Fe 3 O 4 и Cu/Fe 3 O 4
Из рис. 3 видно, что гранулы материалов имеют достаточно малые размеры и неопределенную форму. Эти гранулы слипались вместе, образуя комки. Материал Cu/Fe 3 O 4 более пористый, чем материал Fe 3 O 4 .
Таким образом, по результатам измерений XRD, EDX, SEM можно сделать вывод: успешно синтезированы наноматериалы Cu/Fe 3 O 4 . В частности, Fe 3 O 4 действует как магнитный носитель, экстракт листьев зеленого чая действует как восстановитель, восстанавливая Cu 2+ до Cu, а органические вещества в экстракте действуют как природные стабилизаторы. Процесс синтеза материалов Cu/Fe 3 O 4 методом зеленой химии с использованием экстракта листьев зеленого чая можно описать схемой [1]:
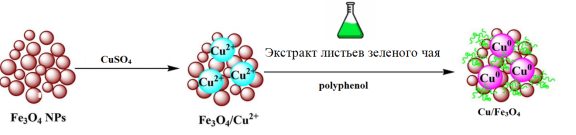
2. Катализ восстановления метиленового синего боргидридом натрия . Для оценки способности синтезированного материала Cu/Fe 3 O 4 обрабатывать красители было проведено три параллельных эксперимента в растворе метиленового синего. Реакционные системы оставляли в темноте для оценки адсорбционной способности, затем выносили на свет для оценки фотокаталитической способности материала. Наконец, добавили к смеси восстановитель NaBH 4 в щелочную среду, чтобы оценить каталитическую способность материала.
,
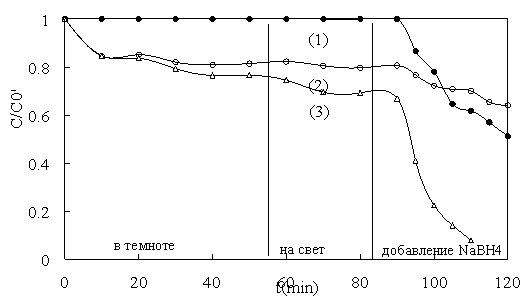
Рис. 4. Зависимость концентрации МB от времени в отсутствие катализатора (1); и в присутствии Fe 3 O 4 (2) и Cu/Fe 3 O 4 (3)
Из рис. 4 видно, что материалы как Fe 3 O 4 , так и Cu/Fe 3 O 4 обладают адсорбционной способностью метиленового синего. Процесс адсорбции протекает довольно быстро, достигая равновесия примерно через 60 мин. Эффективность адсорбции метиленового синего в растворе MB 20 ppm материалами Fe 3 O 4 и Cu/Fe 3 O 4 через 60 мин достигла 17,7 % и 25,5 % соответственно. Под воздействием света в лаборатории концентрация MB существенно не изменилась. Это доказывает, что MB достаточно прочен и не разлагается в условиях видимого света даже в присутствии Fe 3 O 4 и Cu/Fe 3 O 4 .
При добавлении к раствору 1 мл раствора 0,2 М NaBH 4 + 1,5 М NaOH концентрация метиленового синего с течением времени резко уменьшалась. Концентрация МB в растворе, содержащем Cu/Fe 3 O 4 , снижалась значительно быстрее, чем в растворе, содержащем Fe 3 O 4 , и в отсутствие катализатора. Через 20 мин остаточная концентрация МB в растворе, содержащем Cu/Fe 3 O 4 , составляла около 8 %.
График зависимости ln(C 0 /C) (где C 0 — концентрация МB после достижения адсорбционного равновесия, C — концентрация МB в момент времени t) от времени после добавления NaBH 4 показан на рис. 5.
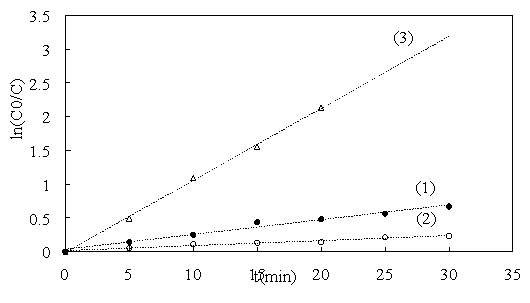
Рис. 5. Зависимость ln(C 0 /C) МB от времени после добавления NaBH 4 в отсутствие катализатора (1); и в присутствии Fe 3 O 4 (2) и Cu/Fe 3 O 4 (3)
График зависимости ln(C 0 /C) от времени имеет линейный характер с R 2 = 0,97–0,99. Это доказывает, что метиленовый синий реагирует с NaBH 4 по кинетическому закону реакции первого порядка по МB. Под действием восстановителя NaBH 4 метиленовый синий восстанавливается до нейтральной, бесцветной и нетоксичной формы (лейкометиленового синего) [5]. Поскольку концентрация NaBH 4 значительно превышает концентрацию метиленового синего, эту реакцию можно считать реакцией псевдопервого порядка по MB.
Таблица 1
Результаты линейной регрессии ln(C 0 /C) МB с течением времени
|
Уравнение |
k ( мин -1 ) |
R 2 |
|
|
Отсутствие катализатора |
y = 0,022x + 0,033 |
0,022 |
0,9881 |
|
Fe 3 O 4 |
y = 0,0074x + 0,0129 |
0,0074 |
0,9778 |
|
Cu/Fe 3 O 4 |
y = 0,1068x — 0,0138 |
0,1068 |
0,9987 |
По коэффициенту наклона уравнения регрессии определили константу скорости реакции восстановления метиленового синего NaBH 4 (k = a). Присутствие Fe 3 O 4 и Cu/Fe 3 O 4 сильно влияет на скорость реакции восстановления МB в двух противоположных направлениях (табл. 1). В то время, материал Cu/Fe 3 O 4 действует как катализатор, увеличивая скорость реакции, материал Fe 3 O 4 действует как ингибитор, снижая скорость реакции. Присутствие Fe 3 O 4 в количестве 0,16 г/л снижает скорость реакции восстановления MB почти в 3 раза (с 0,022 мин -1 до 0,0074 мин -1 ). А присутствие Cu/Fe 3 O 4 в количестве 0,16 г/л увеличивает скорость реакции почти в 5 раз (с 0,022 мин -1 до 0,1068 мин -1 ). Это показывает, что каталитическая способность материала Cu/Fe 3 O 4 определяется фазой Cu, а фаза Fe 3 O 4 действует только как магнитный носитель, помогая восстановить материалы.
Заключение
Успешно синтезирован материал Cu/Fe 3 O 4 методом соосаждения и методом зеленой химии с использованием экстракта листьев зеленого чая. Результаты физико-химического анализа показали, что полученный материал является наноразмерным и состоит из двух фаз: Fe 3 O 4 и Cu.
Наноматериалы Cu/Fe 3 O 4 обладают хорошей каталитической способностью в реакции восстановления метиленового синего боргидридом натрия в щелочной среде. При добавлении Cu/Fe 3 O 4 с содержанием 0,16 г/л к раствору МB 20 ppm скорость восстановления МB увеличилась в 5 раз по сравнению с без катализатора. Фаза Fe 3 O 4 действует как носитель, определяя магнетизм, а фаза Cu выступает как каталитический центр, определяя каталитическую активность материала.
Литература:
- Green synthesis of Cu/Fe 3 O 4 nanoparticles using green tea extract: Evaluation of its catalytic activity, antioxidant and anti-colon cancer effects / L. Xu, L. Zhang, D. Ren [и др.]. — Текст: непосредственный // Inorganic Chemistry Communications. — 2022. — V. 144 — P. 109927. DOI: 10.1016/j.inoche.2022.109927
- Nasrollahzadeh M. Green synthesis of the Cu/Fe 3 O 4 nanoparticles using Morinda morindoides leaf aqueous extract: A highly efficient magnetically separable catalyst for the reduction of organic dyes in aqueous medium at room temperature / M. Nasrollahzadeh, M. Atarod, S. M. Sajadi. — Текст: непосредственный // Applied Surface Science. — 2016. — V. 364(28). — P. 636–644. DOI: 10.1016/j.apsusc.2015.12.209
- Green Nanoarchitectonics of Cu/Fe 3 O 4 Nanoparticles Using Helleborus niger Extract Towards an Efficient Nanocatalyst, Antioxidant and Anti-lung Cancer Agent / Y. Xue, B. Karmakar. — Текст: непосредственный // Journal of Inorganic and Organometallic Polymers and Materials. — 2022. — № 32(9). — P. 3585–3594. DOI: 10.1007/s10904–022–02430-w
- Synthesis of silver decorated silica nanoparticles with rough surfaces as adsorbent and catalyst for methylene blue removal / M. Hu, X. Yan, X. Hu, R. Feng, M. Zhou. — Текст: непосредственный // Journal of Sol-Gel Science and Technology. — 2018. — V. 89. — № 3 — P. 754–763. DOI:10.1007/s10971–018–4871-z
- Isa N. Methylene blue dye removal on silver nanoparticles reduced by Kyllinga brevifolia / N. Isa, Z. Lockman. — Текст: непосредственный // Environmental Science and Pollution Research. — 2019. — № 26(32). P — 11482–11495. DOI: 10.1007/s11356–019–04583–7







