Введение
С развитием фармацевтической науки и производства ежегодно появляются 30–40 новых лекарственных препаратов. В настоящее время в мире зарегистрировано более 10 000 лекарственных веществ [1,2]. В связи с этим все более актуальна проблема их идентификации и определения в различных лекарственных формах, так как на рынок фармпрепаратов, к сожалению, попадают целые партии фальсифицированных, просроченных, некондиционных препаратов, далеких от требований Государственной Фармакопеи (ГФ) [3].
Одним из важных показателей качества лекарственного средства является соответствие требованиям ГФ по содержанию основного компонента. Для идентификации и количественного анализа фармпрепаратов привлекаются самые разнообразные методы, как классические, так и современные. Это физические, химических, физико-химических и биологические методы. Так как наша работа связана в основном с алкалоидсодержащими препаратами, необходимо было оценить современное состояние аналитической химии в области их определения. С этой целью рассмотрены и критически оценены литературные данные по вопросу нашего исследования.
Методы определения
Среди методов количественного определения лекарственных средств в фармацевтическом анализе используют химические методы, в основном это классические, основанные на гравиметрии и титриметрии [4], однако, как правило, им предшествуют трудоемкие операции пробоподготовки. Часто они требуют разделения, концентрирования, высушивания и т. д. Более чувствительны и специфичны физико-химические методы. Методики, используемые в фармацевтическом анализе, должны быть чувствительными, специфическими, избирательными, быстрыми и пригодными для экспресс-анализа. Остановимся на некоторых из них.
Гравиметрический метод основан на взвешивании осажденного вещества в виде малорастворимого соединения или отгонки органических растворителей после извлечения лекарственного вещества. Этот метод чаще всего рекомендуется ГФ, например, при определении солей хинина [5]. Метод точен, но длителен, так как предусматривает такие операции, как фильтрование, промывание, высушивание (или прокаливание) до постоянной массы.
Широкое распространение получили титриметрические методы анализа, они позволяют использовать разнообразные химические реакции и определять вещества, учитывая их свойства и строение. Метод достаточно экспрессен и позволяет оценивать содержание с большой степенью точности, как правило не нуждается в сложном оснащении и может использоваться как в лабораториях, так и, при необходимости, в аптеках. Так в учебной литературе приводятся сведения по определению солей алкалоидов. Например, папаверин гидрохлорид количественно определяют методом неводного титрования или методом нейтрализации в спиртовой среде (индикатор фенолфталеин). В методе неводного титрования для увеличения степени ионизации используют уксусную кислоту, применяя в качестве титранта 0,1н HClO4 в присутствии индикатора кристаллического фиолетового [4].
Применение инструментальных методов значительно расширяет возможности определения фармпрепаратов.
Очень интересно было рассмотреть и оценить вклад отдельных методов в фармацевтическом анализе. По данным оригинальных статей журналов, специализирующихся в области анализа и контроля лекарственных веществ (ЛВ), можно с уверенностью сказать, что «лидирующую» позицию в определении занимают хроматографические методы анализа (более 1500 публикаций за 10 лет). Они составляют более 50 % от всех методик определения лекарственных веществ, описанных в литературе, причем 45 % из них приходится на ВЭЖХ, 23 % — на жидкостную хроматографию, 14 % — на жидкостную хроматографию с масс-спектрометрическим детектированием, 7 % — на газовую хроматографию и 11 % на остальные хроматографические методы. Это хорошо видно на диаграмме [6].
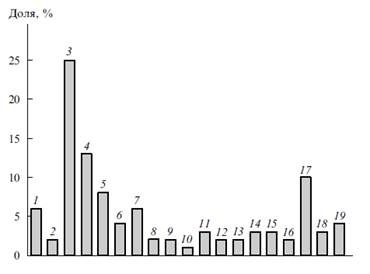
Рис. 1 Распространенность (в %) различных инструментальных методов количественного определения лекарственных веществ (по публикациям 2003–2013гг.). 1 — капилярный электрофорез (6 %); 2 — биоанализ (2 %); 3 — ВЭЖХ (25 %); 4 — жидкостная хроматография (13 %); 5 — жидкостная хроматография с масс-спектрометрическим детектированием (8 %); 6 — газовая хроматография (4 %); 7 — другие хроматографические методы (6 %); 8 — масс-спектрометрия (2 %); 9 — имуноанализ и радиоимуноанализ (2 %); 10 — ИК-спектроскопия и спектроскопия КР (1 %); 11 — вольтамперометрия (3 %); 12 — инверсионная вольтамперометрия (2 %); 13 — ионометрия (2 %); 14 — другие электрохимические методы (3 %); 15 — флуориметрия (3 %); 16 — ЯМР (2 %); 17 — спектрофотометрия и фотоколориметрия (10 %); 18 — проточно-инжекторный анализ (3 %); 19 — другие методы количественного анализа (4 %).
Остановимся подробнее на отдельных хроматографических методах.
Авторами Костенниковой З. П. и Темаковой Л.Ф предложен метод ТСХ для обнаружения алкалоидсодержащих препаратов. В основе метода заложена способность азотсодержащих соединений образовывать комплексы с ионами металлов (используют йодоплатинат калия) и органическими акцепторами (применяют смеси растворителей: бензол — ацетон — эфир — водный аммиак; хлороформ — диэтиламин и др.). ТСХ позволяет идентифицировать алкалоиды, как в чистом виде, так и в смесях [7].
Газовая хроматография дает возможность одновременного определения компонентов лекарственной смеси. Например, в работе Завражной Т. Л. и Кулешовой М. И. показана возможность определение папаверина и этилморфина в смеси. Относительные ошибки определений при этом составляют для папаверина 0,45–0,7 %, а для этилморфина около 1 % при определении миллиграммовых количеств [8].
Второе место по количеству публикаций занимают фотометрические и спектрофотометрические методы анализа
Спектрофотометрический метод в анализе ЛВ это одновременно один из самых простых и достаточно точных методов. Метод предполагает использование органических реагентов, дающих контрастные цветные реакции с различными веществами, что позволяет определять некоторые фармацевтические препараты по их реакции с органическими красителями. Известно достаточно большое количество методик определения лекарственных средств на основе алкалоидов с применением различных реагентов, как органических, так и неорганических [9–13].
Для определения дибазола, димедрола, папаверина широко описано экстракционно-фотометрическое определение, основанное на образовании ионных ассоциатов алкалоидов с азокрасителями. Разработаны методики определения этих фармпрепаратов как в простых, так и сложных лекарственных формах. Например, в работе Карибьянц М. А., Мажитова М. В., Рыжковой А. В. и Бисеновой А. Б. показана возможность определения дротаверина по реакции с феноловым красным в диапазоне концентраций дротаверина от 0,5 мг/мл до 2,5 мг/мл методом градуировочного графика. Наиболее оптимальной кислотностью среды является рН=9 [9]. Илларионовой Е. А. с соавторами описана методика определения дротаверина в субстанции с использованием дихромата калия в качестве образца сравнения. Оптимальная длина волны 353 нм, при относительной погрешноти определения 0,28 %, Sr=0,004. К достоинствам данной методики можно отнести ее экологичность и хорошую воспроизводимость [10].
В работе Мирзаевой Х. А. и сотрудников показана перспективность использования поверхностно активного вещества ОП-7 в качестве стабилизатора малорастворимого ассоциата димедрола {(MoO 2(H 2R) 2) 2-•2ДM +} для его безэкстракционного спектрофотометрического определения в лекарственных препаратах. Разработанная методика определения димедрола, отличается чувствительностью, простотой техники выполнения эксперимента и нетоксичностью используемых реагентов [14].
Кроме того, в другой работе Мирзаевой Х. А. описан экстракционно-фотометрический метод, основанный на взаимодействии димедрола и папаверина с сульфоназо. Способ включает их экстракцию из анализируемой пробы в присутствии цветореагента в виде комплекса с кислотным азокрасителем и фотометрирование полученного ионного ассоциата. Экстракцию осуществляют при объемном соотношении бутанол: проба, равном 1:1, а фотометрирование осуществляют при рН 5 для димедрола и при рН 4 для папаверина в области поглощения с максимумом при 580 нм. Способ позволяет определять исследуемые алкалоиды без их выделения из смеси ингредиентов, входящих в состав лекарственных форм. Метод отличается достаточной точностью (Sr=0,004), чувствительностью, воспроизводимостью и быстротой выполнения анализа [15].
В работах Тираспольской С. Г. с сотрудниками и Щерябякова А. А. с сотрудниками достаточно подробно исследованы условия образования ассоциатов димедрола с такими азокрасителями, как кислотный хром темно-синий, люмогаллион, метиловый оранжевый, сульфонафтолазорезорцин, хромоген черный ЕТ-ОО. Изучены спектральные характеристики и состав образующихся ассоциатов Подобраны оптимальные значения рН и необходимые для экстракции расворители. [12,13]. В работе Сидоровой Е. Ф. показано, что ионные ассоциаты формируются с анионными красителями и лучше экстрагируются в кислой среде. В качестве экстрагента чаще всего используется хлороформ. Для определения димедрола в сложных лекарственных смесях предложена методика, основанная на образовании ионного ассоциата с кислотным хром тено-синим. Как следует из результатов эксперимента, определению не мешают присутствие гидрохлорида эфедрина, теофиллина, борной кислоты, анальгина, фенобарбитала и веществ, применяемых в качестве наполнителей таблеток: глюкозы, фосфата и карбоната кальция, крахмала, желатина, лимонной и винной кислоты, гидрокарбоната натрия и др. [11].
Стоит более подробно остановиться на электрохимических методах анализа лекарственных веществ. По количеству публикаций они занимают третье место, после хроматографических и оптических методов, причем около 20 % работ посвящено потенциометрическому определению ЛВ. Равновесные электрохимические методы анализа ЛВ, в том числе прямая потенциометрия (ионометрия) и потенциометрическое титрование, чрезвычайно удобны, просты и доступны для определения тех ЛВ, которые можно перевести в соответствующую ионную форму. Они, как правило, сочетают в себе достаточную селективность и точность определения, которую можно значительно повысить даже при прямом определении. Электрохимические методы отличаются простотой, экспрессностью, а так же возможностью автоматизизации, что особенно важно на производстве. Кроме того, потенциометрические датчики способны функционировать в режиме проточного анализа и их достаточно легко миниатюризировать для использования в качестве микроэлектродов [6]. Авторами Бобрешовой О. В., Паршиной А. В. и Пожидаевой Ю. В. разработана потенциометрическая мультисенсорная система для экспрессного совместного определения пиридоксина гидрохлорида и никотиновой кислоты в водных растворах. Сенсоры, аналитическим сигналом которых является потенциал Доннана, использованы в мультисенсорной системе в качестве перекрестно чувствительных. В растворах, содержащих оба компонента с концентрациями от 1·10–4 до 1·10–2 М, относительная погрешность определения не превышала 10 % [16]. В работе Назарова С. В., Андрончика К. А. и Егорова В. В. исследована возможность потенциометрического определения баклофена в форме аниона и в форме катиона. Получены основные аналитические характеристики катион-селективного электрода, обратимого к баклофену. Предложена потенциометрическая методика определения баклофена в таблетках, отличающаяся экспрессностью и не требующая трудоемкой пробоподготовки [17].
В плане усовершенствования способов определения лекарственных веществ среди электрохимических методов весьма перспективна потенциометрия с ионоселективными электродами (ИСЭ). За последнее десятилетие опубликовано довольно много статей по созданию и применению ИСЭ в фармацевтическом анализе для определения различных фармпрепаратов: папаверин, дибазол, фенкарол, амброксол, бромгексин, дротаверин, метоклопрамид, мидантан и др. [6, 18, 19] В работах продемонстрированы возможности определения перечисленных физиологически активных аминов в лекарственных формах в вариантах прямой потенциометрии и потенциометрического титрования водными растворами тетрафенилборатом натрия.
Описан также и опробован на модельных растворах и лекарственных формах метод потенциометрического осадительного титрования с использованием ИСЭ. Титрантом для определения катионов ЛВ служит тетрафенилборат натрия, пригодный как для определения индивидуальных ЛВ [20], так и многокомпонентных смесей [21]. Разработан мембранный электрод для определения дротаверина гидрохлорида и предложены в вариантах методы прямой потенциометрии и потенциометрического осадительного титрования. Разработанный ИСЭ обратимо реагирует на изменение концентрации потенциалопределяющего иона в интервале 5·10–2–7,9·10–6 М, имеет предел обнаружения (4,3 ± 0,2) · 10–6 М и наклон электродной функции 58 ± 2 мВ/рС. Харитоновым С. В. и Зарембо В. И. предложена методика потенциометрического определения дротаверина гидрохлорида в таблетках и растворах для инъекций Сmin = (4,3 ± 0,2) · 10–6 М, Sr = 0,003. [22]. Кроме того, описаны ИСЭ для количественного определения антигистаминных препаратов супрастина и фенкарола методами прямой потенциометрии и потенциометрического осадительного титрования. Сmin = 1×10–5 M [18].
Представляет интерес осадительное потенциометрического титрование с применением проточно-инжекционного варианта. Предложена проточно-инжекционная ячейка для определения эфедрина методом потенциометрического титрования с использованием в качестве индикаторного ионоселективного электрода с тетрафенилборатом тетрапентиламмония, растворенным в о-нитрофенилпентиловом эфире. Определение эфедрина проводят в отдельном канале ячейки, в котором располагается ИСЭ. Электрод можно использовать для определения при рН от 2,5 до 11,5; наклон электродной функции составляет 56,4 мВ/рС, предел обнаружения — 3,8·10¯? моль/л [23].
Для количественного определения ЛВ также успешно используют вольтамперометрические методы анализа. Они являются наиболее удбными для анализа сложных систем, ибо дают возможность определять интересующий нас компонент, не выделяя его из смеси других ингридиентов, если они не восстанавливаются и не окисляются при том же потенциале. Окраска растворов или осадок не мешают определению исследуемого компонента, что выгодно отличает вольтамперометрический метод от оптических. Так авторами Зиятдиновой Г. К., Самигуллиным А.И, Будниковым Г. К. предложена методика прямого определения папаверина и дротаверина в лекарственных формах. Показано, что производные изохинолина (папаверин и дротаверин) окисляются на графитовом электроде на фоне 0.1 М серной кислоты, образуя на вольтамперограммах волны при 1.1 В для папаверина и 1.05, и 1.28 В для дротаверина. Оценены нижние границы определяемых содержаний и диапазоны линейной зависимости тока от концентрации папаверина и дротаверина. Проведено определение микрограммовых количеств папаверина и дротаверина в модельных растворах (Sr 0.01–0.04). [24] Однако, при всех достоинствах, недостатком метода является работа с дорогостоящим оборудованием, что подчас делает труднодоступным их использование.
Многие лекарственные препараты используют в виде гидрохлоридов или гидробромидов, причем во многих случаях соотношение основа:гидрохлорид имеет строго определенную стехиометрию. Поэтому возможно косвенное их определение по содержанию галогенидов различными методами. Так Зиятдиновой Г. К., Самигулинным А. И., Абдуллиной С.Г и Будниковым Г. К. описаны способы определения папаверина гидрохлорида и дротаверина гидрохлорида методом кулонометрического титрования с биамперометрической индикацией конечной точки. Установлены стехиометрические коэффициенты реакций папаверина и дротаверина с электрогенерированным хлором. Предполагается возможным определение микрограммовых количеств препаратов в субстанции и лекарственных формах с величиной Sr 0,01–0,03 [25].
Выводы
Итак, нами рассмотрены многочисленные публикации по методам определения алкалоидсодержащих фармпрепаратов, как в «чистом виде» или модельных растворах, так и в конкретных лекарственных формах, в том числе и в сложных смесях, содержащих многие сопутствующие компоненты (наполнители, красители, стабилизаторы и др.).
Критически оценивая эти литературные данные можно сделать вывод, что наиболее широко в настоящее время представлены работы по хроматографическим методам во всех разнообразных проявлениях (газовая, жидкостная, тонкослойная, ВЭЖХ, хромато-масспектрометрия). Методы достаточно чувствительны, точны и селективны. Однако, безусловно требуется дорогостоящая аппаратура, пробоподготовка и дефицитные реагенты или сорбенты.
Достаточно большое место занимают оптические методы. Это и колориметрия, фотометрия, спектрофотометтрия и экстракционно-фотометрические методы. Как правило, они основаны на уже ранее известных реакциях и реактивах. Методики чувствительны, достаточно точны, однако, как и оптические методы в целом недостаточно селективны. Кроме того они мало применимы для анализа сложных многокомпонентных фармацевтических средств.
Из электрохимических методов наиболее широко описана потенциометрия. Особое внимание уделяется работе с ионоселективными электродами. Здесь имеют место и прямые методы (ионометрия) и потенциометрическое титрование. Причем последнее в большинстве своем основано на реакциях осаждения или образования ионных ассоциатов. Эти методы достаточно чувствительны, селективны и точны, как правило, не требуют предварительного разделения, концентрирования или выделения основного компонента.
С нашей точки зрения, методы потенциометрического титрования очень перспективны. Их стоит изучать и развивать. Этой проблеме и посвящено наше исследование.
Литература:
1. Лекарственные препараты в России. Справочник Видаль. АстраФармСервис, Москва, 2012.
2. Фармацевтический вестник, (22), 2012.
3. Чупраева Н. В., Максимкина Е. А. Управление качеством процессов выявления фальсифицированных лекарственных средств//Фармация. — 2010. — № 7. — с. 20–23.
4. Беликов В. Г. Фармацевтическая химия: Учебник для фармацевтических институтов и фармацевтических факультетов. — М.: Высшая школа. — 768 с.
5. Государственная Фармокопея, 2005.
6. Харитонов С. В. Ионоселективные электроды для определения лекарственных веществ.// Успехи химии. — 2007. Т.76, № 4, с. 398–432.
7. Костенникова З. П. Темакова Л. Ф. Использование комплексообразования в ТСХ при анализе настоек, содержащих алкалоиды. РЖ. Химия. — 1981. — № 40298.
8. Завражная Т. Л., Кулешова М. И. Газохроматометрическое определение лекарственной смеси, содержащей папаверина гидрохлориди этилморфина гидрохлорид // Фармация. — 1982. — № 4, с.32.
9. Карибьнц М. А., Мажитова М. В., Рыжкова А. В., Бисенова А. Б. Определение дротаверина по реакции с феноловым красным// Естественные науки. — 2010. — № 3(32), с.161–166.
10. Илларионова Е. А., Сыроватский И. П., Иноземцев П. П. Новый вариант спектрофотометрического определения дротаверина // Сибирский медицинский журнал. — 2011. — № 5, с.75–77.
11. Сидорова Е. Ф., Курымов Г. И. Применение кислотного хром темно-синего для экстракционно-фотометрического определения папаверина гидрохлорида и димедрола.// Фармация. — 1975. — № 1, с.46–50.
12. Тираспольская С. Г., Назарова Л,Е., Скибина В. В. Экстракционно-фотометрическое определение димедрола в присутствии норсульфазола и сульфадимезина. // Фармация. — 1984. — № 1, с.67–69.
13. Щерябякова А. А., Жебентяев А. И. Сравнительное экстракционно-фотометрическое исследование ассоциатов димедрола с азокрасителями. // Фармация. — 1997. — № 3. С.46–50.
14. Мирзаева Х. А., Бюрниева У. Г., Рамазанов А. Ш., Кимпаева М. М. Спектрофотометрическое определение димедрола с использованием его ионного ассоциата. //Фармация. — 2012. — № 4. С.18–20.
15. Мирзаева Х. А., Ахмедова М. С., Рамазанов А. Ш., Ахмедов С. А. Экстракционно-фотометрическое определение димедрола и папаверина в лекарственных формах.// ЖАХ. — 2004. — Т.4, № 3, с.245–249.
16. Бобрешова О. В., Паршина А. В., Пожидаева Ю. В. Потенциометрическое перекрестно-чувствительные Пд-сенсоры для совместного определения никотиновой кислоты и пиридоксина гидрохлорида в водных растворах. // ЖАХ. — 2013. — Т.68, № 4, с.348.
17. Назаров В. А., Андрончик К. А., Егоров В. В., Беляев С. А., Юркштович Т. П. Количественное определение баклофена в таблетках с помощью ионоселективных электродов. // Химико-фармацевтический журнал. — 2011. — Т.45, № 6, с.50–52.
18. Харитонов С. В., Зарембо В. И. Мембранные ионоселективные электроды для количественного определения супрастина и фенкарола. // Известия высших учебных заведений. Серия: Химия и химическая технология. — 2006. — Т. 49, № 1, С. 28–31.
19. Астапович Р. И., Егоров В. В., Высоцкий Д. Л., Тельманова М. О., Назаров М. А. Ионоселективные электроды для определения некоторых физиологических активных аминов и их применение в анализе. // Заводская лаборатория. — 2010. — Т.76, № 1, с.22–27.
20. M. N. Abbas, G. A. Mostafa, A. M. A.Homoda. Talanta, 53, 425 (2000).
21. Егоров В. В., Репин В. А. ЖАХ, 50 463 (1995).
22. Харитонов С. В., Зарембо В. И. Ионоселективные электроды для количественного анализа лекарственных форм препарата но-шпа. // Химико-фармацевтический журнал. — 2008. — Т. 42, № 5, С. 46–49.
23. M. N. M.P.Alcada, J. L. F.C.Lima, M. C. B.S. M. Montenegro. J.Pharm.Biomed.Anal.,13? 459 (1995).
24. Зиятдинова Г. К., Самигуллин А.И, Будников Г. К. Вольтамперометрическое определение папаверина и дротаверина. // ЖАХ. — 2007. — Т.62, № 8, с.858–861.
25. Зиятдинова Г. К., Самигуллин А.И, Абдуллина С. Г., Будников Г. К. Количественное определение производных бензихинолина методом кулонометрического титрования. // Химико-фармацевтический журнал. — 2008. — Т.42, № 2, с.47–50.







