Ключевые слова : бромирование, α-бромэтаноны, α-аминокетоны, антибактериальная активность, периферическая н-холинолитическая активность.
Благодаря структурному сходству с одним из важнейших природных соединений — адреналином — α-аминокетоны представляют большой интерес в аспекте создания новых биологически активных средств. В настоящее время в медицинской практике широко используются препараты этой группы [1–5]: адреналон (аналог адреналина); бутилсимпатон (адреноблокатор, применяется для лечения паркинсонизма); лофепрамин (антидепрессант); метиндион (психотропный, противоэпилептический, противосудорожный); мифадол (анальгетик, противокашлевый); МНН, тилорон (противовирусный). α-аминoкетоны продолжают привлекать внимание ученых как с целью применения их больших возможностей в качестве исходных соединений в органическом синтезе, так и при поиске биологически активных соединений широкого спектра действия.
Синтезу и биологической активности новых α-аминoкетонов посвящено большое число публикаций [6–36]. Одним из наиболее часто применяемых методов синтеза α-аминoкетонов является алкилирование аминов α-бромкетонами [6–29]. Реакцию проводят в присутствии органического (неорганического) основания или избытка амина в качестве связывающего агента. Так, взаимодействием производных 2-гидрокси(алкокси)-5-(2-бромацетил)бензойной кислоты 1 с 4-(2-оксо-1-бензимидазолинил)пиперидином ( 2 ) в среде сухого растворителя в присутствии сухого поташа синтезированы производные 2-гидрокси(алкокси)-5-[4-(2-оксо-1-бензимидазолинил)пиперидиноацетил]бензойной кислоты 3 [9, 10].

X = HO, CH 3 O, C 2 H 5 O, NH 2 , замещенные амины; R 1 = H, CH 3 , C 2 H 5 ;
R 2 и R 3 = H или двойная связь в пиперидиновом кольце
Аналогично указанному примеру взаимодействием производных 2-(1,4-бензодиоксан-2-ил)-2-бромацетила 4 с 4-(2-оксо-1-бензимидазолинил)пиперидином в среде диметилформамида получены производные 2-(1,4-бензодиоксан-2-ил)-2-[4-(2-оксо-1-бензимидазолинил)пиперидиноацетил]-1,4-бензодиоксана 5 [10].
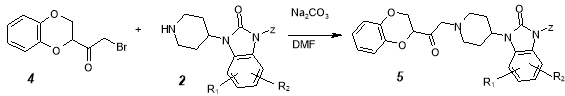
Z = H, алкил, алкенил, алкилоксиалкил, феноксиалкил, цианоалкил;
R 1 и R 2 = H, галоген, алкил, алкенил
Авторами работ осуществлен синтез ω-аминопроизводных 4-(3’,4’,5’-триметоксибензoиламино)ацетофенонов 6 [12, 13].

Am = NH 2 , N(C 2 H 5 ) 2 , NC 6 H 11 , HNCH 2 C 6 H 5 , HNC 6 H 4 COOH (o-, м-, п-)
Соединения 7 , аминным фрагментом в молекуле которых служат замещенные пиперидины, также получены вышеуказанным методом и обладают гипотензивной активностью; некоторые производные нашли применение в фармацевтических композициях [15].
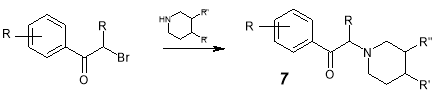
R = НО, Hal, алкил, алкокси, алкенилокси, алкилтио, CO 2 H, CO 2 Аlk и др.
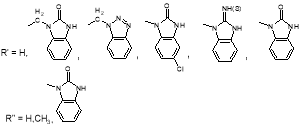
Существуют и другие методы получения α-аминoкетонов. Так, в ряде работ описан синтез α-аминoкетонов из N-замещенных аминoкислот [17–19, 23]. Авторами публикаций [17–19, 23] защищенные α-аминoкислоты посредством реакции Фриделя — Крафтса удалось перевести в α-аминoкетоны; так, из N-(метоксикарбонил)аланина получено соединение 8 с сохранением конфигурации.
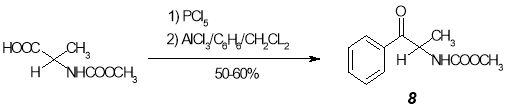
В работе [16] предложен общий путь синтеза α-аминoкетонов из лейцина. Полученный из него N-метоксиметиламид взаимодействием с металлорганическим соединением превращается в соединение 9 .
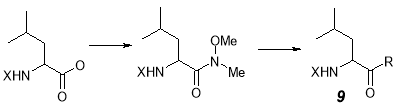
Синтез α-аминогалометилкетонов 10 осуществлен, исходя из эфиров защищенных аминoкислот 11 через промежуточные N-силил-защищенные производные 12 и далее взаимодействием последних с дигалометаном и алкиллитием [18, 23].
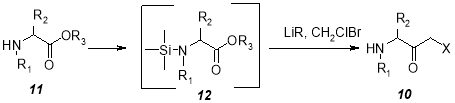
X = Hal; R 1 = защитная группа; R 2 = H, алкил; R 3 = низший алкил
Авторы [23] указывают на преимущества дополнительной защиты аминогруппы силильной группой, что значительно повышает выход аминoкетонов 10 . Синтезированы α-аминогалометилoкетоны 13 , исходя также из эфиров α-аминoкислот [17]. Последние переводят в N-защищенные α-аминогалометилкетоны 14 через промежуточные иминопроизводные 15 .
Способ предложен для промышленного производства соединений 13 .
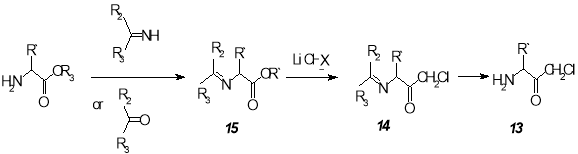
Другие методы получения α-аминoкетонов были успешно использованы авторами работы [24]. Так, соединение 16 синтезировано окислением аналогичного аминоспирта.

R 1 , R 2 — алкил, алкиленовая цепь (C 3 –C 6 ), в т. ч. включающая гетероатом;
R 3 , R 4 — Н, алкил, арилалкил, гетероарилалкил, арил; R 3 , R 4 вместе могут составлять алкиленовую цепь (C 3 –C 6 ), в т. ч. включающую гетероатом
Авторы патента [19] синтезировали соединения 17 из эпоксидного производного.

Интересным путем из производных 3-оксазолидин-5-онов автору работы [20] удалось синтезировать α-аминогалометилкетоны или N-замещенные α-аминогалометилкетоны 18 . Способ предложен для промышленного производства.
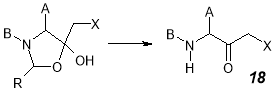
Из кетиминов 19 и 20 по схеме получены соответствующие α-аминoкетоны 21 и 22 [29].
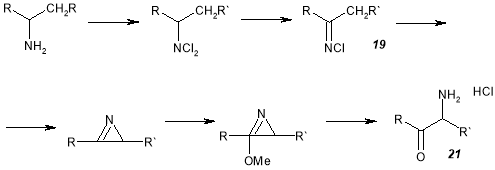

R = H, CH 3 , i-C 3 H 7 , C 6 H 5 ; R' = H, CH 3
α-аминoкетоны 23 , 24 обладают седативной и антигипертензивной активностью и могут найти применение как лекарственные препараты при лечении гипертензии [25, 26].

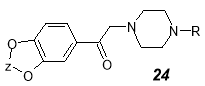
R = H, Cl, F; Z = (СН 2 ) m , m = 1–3, или –СН 2 –(R 2 )C(R 2 )–СН 2 –
R = Ph, замещенный Ph
Высокой активностью отмечены соединения 25 – 27 [30, 33]. Из этой группы отобран 3-хлор-α-трет-бутиламинопропиофенон ( 26 ) (бупропион), который в медицинской практике предложен для лечения психосексуальной дисфункции [4, 8, 33].

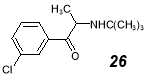
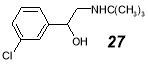
R = H, (СН 2 ) n ОН, (СН 2 ) n О–(СО)–О(СН 2 ) р СО 2 и т. п.; n = 1, 2; p = 1–3
Описан также соответствующий аминоспирт 27 , предложенный как антидепрессант [30].
В ряде патентов приводится синтез аминoкетонов (не только α-, но и β- и др.) с большим разнообразием гетероциклических аминов; некоторые из них, например соединения 28 , проявляют спазмoлитическую и сосудорасширяющую активность, другие предложены в качестве лигандов 5-НТ 4 -рецепторов.
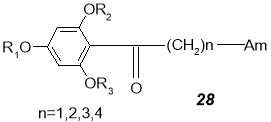
Am = гетероциклические амины, в т. ч. пирролидино, пиразолидино, пиперидино, замещенные пиперидино, пиперазино, морфолино, азепино, имидазолидино;
R 1 = H, п(м)-СН 3 , п-СН 3 О, ОН, Cl; R 2 = H, алкил; R 3 = H, о-СН 3
Производные пирролидина 29 запатентованы как средства, стимулирующие центральную нервную систему [23].

R 1 = H, п(м)-СН 3 , п-СН 3 О, ОН, Cl; R 2 = H, алкил; R 3 = H, о-СН 3
Запатентовано большое число замещенных α-аминoацетофенонов, которые могут быть предложены как противомикробные, гипотензивныe, противовоспалительные, анальгезирующие, психотропные и иммунодепрессантные средства [14, 24, 33–36].
Спектр фармакологической активности α-аминoкетонов в действительности значительно шире; они перспективны также для применения как нейролептические [35], фунгицидные, антимикробные и другие средства [13, 17, 30, 33].
Литература:
- Машковский М. Д. Лекарственные средства / М. Д. Машковский. М.: Новая волна, 2007.
- Авакян О. М. Фармакологическая регуляция функции адренорецепторов / О. М. Авакян. М.: Медицина, 1988.
- Кудрин А. Н. Аминокетоны / А. Н. Кудрин, В. Г. Воробьев. М.: Медицина, 1970.
- Negwer M. Organic-chemical drugs and their synonyms. Akademie-Verlag, Berlin, 1987.
- Геворгян Г. А. О взаимосвязи между химической структурой и биологической активностью в ряду α- и -аминокетонов / Г. А. Геворгян, А. Г. Агабабян, С. А. Габриелян // Взаимосвязь «химическая структура — биологическая активность»: cборник трудов. Ереван: Апага, 1998. С. 187–198.
- Геворгян Г. А. Синтез и некоторые биологические свойства -, -, -аминокетонов и их производных: дисс. … д-ра хим. наук / Г. А. Геворгян. Ереван, 2007.
- Fischer H. E., Huchowski J. M. Synthesis of α-aminoaldehides and α-aminoketones // Org. Prep. proced Int. 1990. № 22 (4). P. 399–484.
- JP 82-91117 (1996). Davidson C. M. R., Grisar M. J., Claxton G. P. 2-Hydroxy-5-[1-hydroxy-2-(4-oxo-1-benzimidazolinyl)piperidinoethyl]benzoesaure derivate sowie Verfahren zu deren Herstellung.
- GB 2053194A (1980). Grisar M. J., Claxton G. P. Benzimidazolines.
- US 3910930 (1975), LP49-95980 (1974), NL 7400132 (1974). Van Wijngaarden I., Sendijn W., Janssen P. A. J. [1-[2-(1,4-Benzodioxan-2-yl)-2-hydroxyethyl]-4-piperidyl]-2-enzimidazolinones.
- Клюшин В. В. ω-Aминокетоны и азотсодержащие гетероциклы, содержащие 3,4,5-триметоксифенильную группу / В. В. Клюшин, В. А. Портнягина, В. Я. Починок // Украинский химический журнал. 1984. № 50 (9). С. 1000–1002.
- Клюшин В. П. ω-Аминопроизводные 4-(3,4,5-триметоксибензоиламино)ацетофенона и их физиологическая активность / В. В. Клюшин, В. А. Портнягина, В. Я. Починок // Украинский химический журнал. 1984. № 50 (9). С. 1291–1296.
- Попов А. Ф. Синтез и противомикробное действие α-аминокетонов / А. Ф. Попов, Ж. Н. Пискунов, В. Л. Матвиенко // Химико-фармацевтический журнал. 1989. № 10. С. 1232–1234.
- EP 0092391 (1983), EP 0092391A2 (1983), EP 0092391 A3 (1983). Teranishi M., Obase H., Namoto Y. Novel piperidine derivatives and pharmaceutical composition containing same.
- Dufour M. N., Jouin P., Poncet J. Synthesis and reduction of α-aminoketones derived from leucine // The Journal of the American Chemical Society. Perkin Trans I. 1986.
- US 6500985B2 (2002). Tomoyuki O., Takashi N., Naoko H. Process for the preparation of α-aminoketones.
- US 5523463 (1996). Hilpert H. Method of producing halogenated α-aminoketones and α-aminoalcohols.
- WO 00/53571 (2000). Inishi T., Hiroze N., Suzuki T. Process for the preparation of α-aminoketones.
- JP 82-91117 (1996). Grisar M. J., Claxton G. P. Production of α-aminoketones.
- JP 63-192742 (1988), JP 63-192744 (1988). Ori Allchiro. Production of α-aminoketones.
- JP 63-192743 (1988). Fukuoka Onori. Selection of α-aminoketones.
- EP 0703209A2 (1994), EP 0703209A3 (1996), EP 0703209B1 (1995). Hilpert H. Verfaren zur Herstellung von halogenierten α-Aminoketonen und α-Aminoalkoholen.
- FR 253693 (1984). Corbiere J. New aminoketones, process for preparing them and therapeutic use.
- US 4684651 (1987). Ryoji Kikumoto, Harucazu Furami, Kenichiro Nakao, Mamoru Sugano. Alkylenedioxybenzene and acid addition salts thereof as hypotensives.
- Bounte J. P., Piancastelli M. C. Aminoketone and aminoalcohol derivatives of benzoxazolinone synthesis, adrenergic and antihypertensive properties // The Journal of Medicinal Chemistry. 1990. № 25 (4). P. 361–368.
- JP 8291117 (1996). Miyata Hiroyuki, Yamamoto Yasuhito, Yakota Naoyuki, Ataka Kikuo. Production of α-aminoketones.
- PCT JP 00/01336 (2000). Onishi T., Hirose N., Suzuki T. Process for the preparation of α-aminoketones.
- Baumgarten H. E., Petersen J. M., Wolf D. C. Reactions of amines. XI. Synthesis of α-aminoketones from ketimines // The Journal of Organic Chemistry. 1963. № 28 (9). P. 2369–2371.
- Rom. 67367 (1979). Mehta N. B. Ketone compounds with biologicai activity. CA. 1981. V. 95: 61775q.
- US4906781 (1990). Drabb T. W., Jr. Preparation of 2,4-diamino-3’,5’-dichloroacetophenones as intermediates for animal growth regulators. CA. 1990. V. 113: 40156.
- EP 0700383 (1998). Clark R. D., Eglen R. Novel 1-phenylalkanone 5-HT4 receptor ligands.
- DE 3343934 (1984). Stern W. C. м-Хлор-α-трет-бутиламинопропиофенон и его применение для понижения уровня холестерина // Бюллетень изобретений. 1984. № 23.
- EP 171227 (1986). Stern W. C. 3-Chloro-α-tetr.-butylaminopropiophenone in treatment of psychosexual dysfunction. CA. 1986, 105:56618 n.
- Schulz E., Frahm C., Kobow M., Sprung W. D. Antiinflammatory and analgesic action of long-chain phenyl substituted — aminoketones // Pharmazie. 1996. № 51 (8). P. 591–593.
- Huang Y., Hall I. H. Antiinflammation activity of α-, β- and γ-aminoketones in CF mice // Res. Commun. Pharmacol. 1996. № 1. P. 17–38.
- N-Адамантилпроизводные ароматических аминов. Сообщение II. Синтез и свойства N-(5-R- или 6-R-адамант-2-ил)ариламинов / Н. В. Климова, Н. И. Авдюнина, Б. М. Пятин [и др.] // Химико-фармацевтический журнал. 2002. Т. 36, № 6. C. 14–16.







