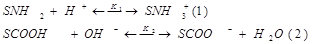В работе проведено потенциометрическое титрование дисперсий альбумина в растворе калия хлорида различной концентрации, определено значение ТНЗ и влияние хлорида калия на это значение.
Ключевые слова: потенциометрическое титрование, альбумин, сорбция.
Все белки в зависимости от строения делятся на простые — протеины, состоящие только из аминокислот, и сложные — протеиды, имеющих небелковую простетическую группу. Протеины представляют собой простые белки, состоящие только из белковой части. Они широко распространены в животном и растительном мире. К ним относятся альбумины и глобулины, встречающиеся практически во всех животных и растительных клетках, биологических жидкостях и выполняющих важные биологические функции. Альбумины участвуют в поддержании осмотического давления крови, транспортируют с кровью различные вещества [1–2].
Протеиды являются сложными белками, состоящими из белковой и небелковой частей. Название протеида определяется названием его протеистической группы. Так, нуклеиновые кислоты являются небелковой частью нуклеопротеидов, фосфорная кислота входит в состав фосфопротеидов, углеводы — гликопротеидов, а липиды — липопротеидов [3].
Яичный альбумин занимает промежуточное место. Обычно яичный альбумин, как и все альбумины, относят к простым белкам. Функция яичного альбумина в живых организмах основана на его способности образовывать отложения — запасная функция, он является одним из важнейших источников белка для человека, содержащий все важные, незаменимые аминокислоты [4–6].
Представленная в статье работа, является частью работ посвященных изучению физико-химических и коллоидных свойств белков [7–11] и порфиринов [12–15]. Актуальность исследований систем содержащих сложные биологически активные соединения, а также устойчивость их дисперсий, не вызывает сомнений [16–18]. Подобные исследования позволят создавать комплексы белков и лекарственных препаратов, включая новые лекарственные формы, разрабатываемые в настоящее время в академии [19–22].
В качестве объекта исследования был взят яичный альбумин производства немецкой фирмы Merck. Для исследования использовался метод потенциометрического титрования [23–24]. В ячейку для потенциометрического титрования помещали 25 мл исследуемой дисперсии, 30 минут пропускали воздух, освобожденный от СО2 и титровали раствором КOH (0,0129 моль/л) или НС1 (0,010 моль/л). Титрант вводили порциями по 0,1 мл с помощью микробюретки с интервалом в 1 минуту. Растворы КOH готовили на дистиллированной воде, предварительно освобожденной от СО2 воздуха кипячением в течение 30 минут. После каждой добавленной порции титранта измеряли значения рН раствора. Регистрация рН осуществляется на рН-метре — милливольтметре рН-673 с точностью измерения рН ±0,05 единиц рН. Растворы KCl готовились из фиксаналов.
По результатам потенциометрического титрования были построены зависимости рН исследуемого раствора от объема добавленного титранта (V, мл) для растворов без адсорбента и с адсорбентом. В кислой области преобладает адсорбция ионов водорода, а в щелочной области ионов ОН-. Значение рН точки пересечения кривых титрования с адсорбентом и без него соответствует условию равенства адсорбированных Н+ и ОН- -ионов — это соответствует точке нулевого заряда (рНТНЗ) [25]. Таким образом, методом потенциометрического титрования определяется разница между адсорбцией ионов Н+ и ОН-. Кривые титрования с адсорбентом и без сравнивают и рассчитывают разницу между количеством адсорбированных ионов Н+ -(ОН-) отнесенное к единице массы или поверхности адсорбента:
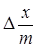 (ОН- — H+) =
(ОН- — H+) = 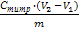
[1]
где (H+-ОН-) — разница между количеством адсорбированных ионов Н+ и ОН- отнесенная к единице массы адсорбента, моль/г;
Ститр — концентрация титранта КOH (HCl), моль/л;
V1 — объем раствора титранта, пошедший на титрования раствора без адсорбента, мл;
V2 — объем раствора титранта, пошедший на титрование раствора с адсорбентом, мл;
m — масса адсорбента, г;
Расчет — (Н+- ОН-) производят для одинаковых значений рН раствора с адсорбентом и без, в нашей работе при значениях рН от 3,0 до 10,0. Через заданное значение рН проводят линию параллельную оси абсцисс и находят V1 и V2.
Погрешность измерения значений рН составила 0,05 единиц рН.
Ранее метод был отработан на полисахаридах и порфиринах [26–27].
Рассмотрим результаты потенциометрического титрования. На рис. 1 представлены результаты титрования дисперсии альбумина в присутсвии хлорида калия. Анализ кривых потенциометрического титрования показывает, что в области рН <рНТНЗ кривая титрования с адсорбентом идет выше, чем без адсорбента, вследствие адсорбции Н+ — ионов на альбумине. Альбумин в этой области рН заряжен положительно. В области рН >рНТНЗ кривая с адсорбентом идет ниже, чем без адсорбента из — за адсорбции ОН- — ионов. Вследствие того, что на альбумине в водных растворах адсорбируются одновременно ионы Н+ и ОН-. В общем виде можно записать две поверхностные реакции:
где S –символ поверхности.
Аналогично выглядят зависимости и для других концентраций КCl.
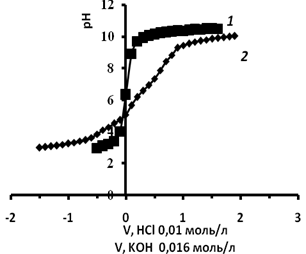
Рис. 1. График потенциометрического титрования.: 1 — кривая титрования раствора КСl (0,01 моль/л); 2 — кривая титрования дисперсии альбумина КСl (0,01 моль/л)
Соответственно в зависимости от того, адсорбция каких ионов преобладает, поверхность приобретает либо положительный, либо отрицательный заряд. При увеличении концентрации протонов в водных растворах увеличивается протонизация аминогрупп, и уменьшается диссоциация карбоксильных групп. К обратному эффекту приводит увеличение концентрации гидроксид-ионов. При этом поверхность белка заряжается отрицательно. При увеличении ионной силы раствора происходит увеличение обмена катионов и анионов на Н+, ОН-, что отражается на увеличении адсорбции Н+, ОН-.
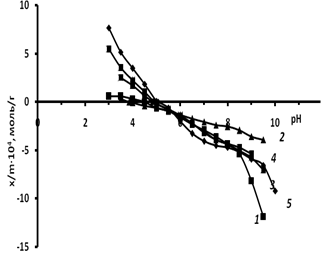
Рис. 2. Зависимость адсорбции ионов Н+, ОН- на альбумине от рН: 1 — водная дисперсия альбумина; 2 — водная дисперсия альбумина с добавлением KCl (0.001 моль/л), 3 — водная дисперсия альбумина с добавлением KCl (0.01 моль/л), 4 — водная дисперсия альбумина с добавлением KCl (0.1 моль/л), 5 — водная дисперсия альбумина с добавлением KCl (1 моль/л).
Из рис 2. видно что, что рНТНЗ с увеличением концентрации хлорида калия сдвигается в основную область и изменяется от 4,1 до 5,0, что свидетельствует о сорбции аниона, в нашем случае Cl-.
Выводы
В работе проведено исследование адсорбции ионов водорода и гидроксид-ионов на альбумине в растворе хлорида калия различных концентраций. Установлено:
1. Адсорбция H+, OH- — ионов на альбумине возрастает с увеличением концентрации хлорида калия.
2. Хлорид калия влияет на рНТНЗ, сдвигая в основную область, что свидетельствует об адсорбции Cl-.
Литература:
1. Грин Н., Стаут У., Тейлор Д. Биология в 3-х томах. — М.: Мир, 1996. Том 1. — 368 с.
2. Измайлова В. Н., Ямпольская Г. П., Сумм Б. Д. Поверхностные явления в белковых системах. — М.: Химия, 1988. — 239 с.
3. Измайлова В. Н., Ребиндер П. А. Структурообразование в белковых системах. — М.:Наука, 1974. — 268 с.
4. Ptitsyn O. B., Finkelstein Theory of Protein Secondary Structure and Algorithm of Its Predicthion. Biopolymers.,1983.Vol. 22. № 1. Р. 15–25.
5. Kuo-Chen Chou. Origin of low-frequency motions in biological macromolecules. A viev of recent progress in the quasi-continuity model. Biophys. Chem., 1986. Vol. 25. № 2. Р. 105–116.
6. Byler D. M., Susi H. Examination of the Secondary Structure of Proteins by Deconvolved FTIR Spectra. Biopolymers., 1986. Vol. 25. № 2. Р. 469–487.
7. Чухно А. С., Дмитриева И. Б., Мартынов Д. В.. Изоэлектрическая точка белков в водных растворах азолов. // Вестник СПбГУ. 2011. Серия 4: Физика. Химия. Вып. 2. С.124–133.
8. Чухно А. С., Дмитриева И. Б., Колодеева С. С., Мартынов Д. В.. Адсорбция ионов Н+ и ОН- на коллагене. // Вестник СПбГУ. 2011. Серия 4: Физика. Химия. Вып. 3. С. 87–95.
9. Чухно А.С., Дмитриева И.Б., Банкина А.Н., Бриллиантова Е.Ю. Изучение взаимодействия белков с биологически активными азотсодержащими гетероциклическими соединениями при различных значениях pH. // Бутлеровские сообщения. 2013. Т.34. № 5. С.91–99.
10. Чухно А. С., Банкина А. Н., Бриллиантова Е. Ю.. Кинетика процесса набухания желатины в водных растворах азолов. // Бутлеровские сообщения.- 2014. — Т.38. № 5. С.84–88.
11. Men'shikova A.Yu., Skurkis Yu.O., Kuchuk V. I., Dmitrieva I. B., Evseeva T. G., Shabsel's B. M. Effect of the surface structure of poly(styrene-co-acrolein) microspheres and its modification by protein on electrosurface properties. // Коллоидный журнал. 2001. Т. 63. № 5. С. 629–636.
12. Родионова Е. Ю., Дмитриева И. Б., Чухно А. С. Электрокинетические свойства гемоглобина в водных растворах НСl и KCl. // Бутлеровские сообщения. 2012. Т.30. № 6. С.103–107.
13. Родионова Е. Ю., Дмитриева И. Б., Чухно А. С. Электрокинетические свойства гемоглобина в водных растворах 1-, 2- и 3-зарядных ионов. // Бутлеровские сообщения. 2013. Т.34. № 6. С.135–140.
14. Родионова Е. Ю., Дмитриева И. Б., Чухно А. С. Электрокинетические свойства хлорофилла в водных растворах 1-, 2- и 3-зарядных катионов. // Бутлеровские сообщения. 2013. Т.34. № 6. С.130–134.
15. Крайник И. И., Родионова Е. Ю., Дмитриева И. Б. Исследование электроповерхностных свойств водных дисперсий гемоглобина. // Молодой ученый. 2014. № 14–1. С. 20–24.
16. Широкова И. Ю., Кучук В. И., Беляев А. П., Шевченко Н. Н., Голикова Е. В. Агрегативная устойчивость дисперсных систем. Часть 1. Исследование электроповерхностных свойств и кинетики коагуляции монодисперсных полимерных частиц с карбоксилированной поверхностью. // Бутлеровские сообщения. 2014. Т.37. № 2. С.29–38.
17. Кучук В. И., Широкова И. Ю., Голикова Е. В. Физико-химические свойства водно-спиртовых смесей гомологического ряда низших алифатических спиртов. // Физика и химия стекла. 2012. Т. 38. № 5. С. 625–633.
18. Родионова Е. Ю., Дмитриева И. Б., Чухно А. С. Влияние состава дисперсионной среды на устойчивость и электрокинетические свойства билирубина. // Бутлеровские сообщения. 2014. Т.37. № 1. С.55–61.
19. Беляев А. П., Рубец В. П., Антипов В. В., Бордей Н. С., Зарембо В. И. Фазовый переход пар — кристалл при синтезе пленок парацетамола методом вакуумного испарения и конденсации. // ЖТФ. 2014. Т.84. Вып. 3. С.141–143.
20. Беляев А. П., Рубец В. П., Антипов В. В., Рыбников А. О., Беляева С. А. Кристаллизация парацетамола ромбической формы. // Бутлеровские сообщения. 2014. Т.37. № 3. С.113–119.
21. Dmitrieva I. B., Chukhno A. S., Rodionova E. Y.,. Novichkov R. V.. Specific Adsorption of Aspartic Acid on Iron (III) and Nickel (II) Oxides.// Eurasian Chemico-Technological Journal. 2012. Т. 14. № 4. С. 299–304.
22. Дмитриева И.Б., Чухно А.С., Новичков Р. В.. Взаимодействие глицина с катионами железа(III) и никеля(II) в водных растворах и на поверхности их оксидов. // Бутлеровские сообщения. 2013. Т.35. № 8. С.133–137.
23. Беляев А. П., Скворцов А. М., Кучук В. И., Дмитриева И. Б., Бахолдина Л. А., Чухно А. С., Гришин В. В., Купина Н. А., Малахова Е. Е.. Физическая и коллоидная химия. Руководство к практическим занятиям: учебное пособие. / Под ред. проф. А. П. Беляева. — М.: ГЭОТАР-Медиа, 2012. — 320 с.
24. Григоров О. Н. Электрокинетические свойства капиллярных систем. / Григоров О. Н., Козьмина З. П., Маркович А. В., Фридрихсберг Д. А. М. — Л.: Изд-во АН СССР. 1956. 336с.
25. Беляев А. П. Физическая и коллоидная химия / Беляев А. П., Кучук В. И. / под.ред. А. П. Беляева. — 2-ое изд., перераб. и доп. — М., 2012.-752с.
26. Чухно А. С., Дмитриева И. Б., Мартынов Д. В.. Влияние солей одно-, двух- и трехзарядных катионов металлов на сорбцию Н+ и ОН- ионов на декстране. // Бутлеровские сообщения. 2011. Т.27. № 14. С. 47–54.
27. Чухно А. С., Дмитриева И. Б., Силаева Д. С., Сенина А. С., Кошевенко А. С., Назипова А. Р. Сорбция ионов Н+ и ОН- на хлорофилле, влияние рН на устойчивость водных дисперсий хлорофилла. Бутлеровские сообщения. 2013. Т.34. № 5. С.124–130.