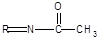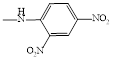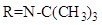В результате проведенных исследований были синтезированы азометиновые производные госсипола с аминосоединениями, и перевод этих азометинов в водорастворимое состояние.
Ключевые слова: госсипол, интерферон, матрица, кристаллическая структура.
Одним из перспективных направлений биоорганической химии, химии природных и физиологически активных веществ является изучение зависимости между химическим строением и биологической активностью. Эти систематические исследования позволяют разрабатывать научные основы направленного синтеза эффективных, специфических биологически-активных веществ [1].
Известно, что первым низкомолекулярным индуктором интерферона является госсипол — желтый пигмент семян хлопчатника. Это уникальный не только по своему строению, но и биологической активности полифенол. На основе самого госсипола и некоторых его производных создан ряд лекарственных препаратов противовирусного действия (3 % линимент госсипола, 3 % мазь мегосина, таблетки гозалидона, рагосина, мебавина). В основе специфической активности этих, разрешенных к широкой медицинской практике препаратов, лежит их способность индуцировать в самом организме a, b и g — интерфероны. Поэтому производные госсипола, влияя на систему интерферона, оказывают опосредовано свое противовирусное действие [2–3].
В связи с вышеизложенным, целью настоящего исследования был синтез новых азометиновых производных госсипола с аминосоединениями, и перевод этих азометинов в водорастворимое состояние.
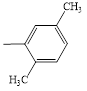
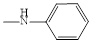
Синтез новых азометиновых производных госсипола осуществляли по следующей схеме:
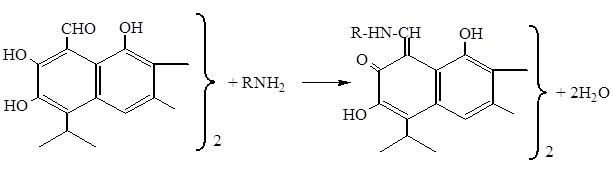
ИК-спектр самого госсипола и некоторых его иминосоединений имеют характерные полосы поглощения в области — 2140–2040, 1630–1605 и 1460–1430 см-1. В этой области дают сигнал ароматические ядра и азометиновые связи во всех изученных веществах. Для всех изученных веществ полоса поглощения изопропильной группы при С5 составляет величину 1180–1170 см-1. Валентные колебания СН3 группы во всех соединениях дают сигнал в области 2970–2860 см-1, а деформационные колебания в области 1430–1380 см-1.
В качестве спектрального критерия прохождения реакции между госсиполом и перечисленными аминами были выбраны спектры их ПМР. Для снятия ПМР спектров синтезированных веществ в качестве растворителя использовали CDC13. Изменение химсдвигов протона и проявления сигнала протона в положении 15 молекулы госсипола (альдегидной группы), лежит в пределах от 11 м.д. до 11,3 м.д., а для протона азометиновой группы (CH=N) в молекулах его производных в пределах от 9,40 до 10,40 м.д.. Поэтому, исчезновение сигнала протона альдегидной группы и появление вместо него сигнала протона азометиновой группы, однозначно свидетельствовало о прохождении реакции между госсиполом и амином. В спектрах ПМР также имеются сигналы соответствующие таким группам как, -ОН, -СООН, -СН, -СН2, -СН3 и др. находящихся как в самой молекуле госсипола так и в молекулах соответствующих аминосоединений.
В качестве R-использовали гомологи анилина и фенилгидразина. Некоторые физико-химические характеристики полученных новых азометинов госсипола приведены в таблице 1.
Таблица 1
Физико-химические характеристики азометиновых производных госсипола
|
№ |
Радикал — R |
Tпл, 0С |
Rf |
Цвет вещест. |
Выход прод. реак. в %-ах |
|
I |
|
251–253 |
0,64* |
Светло желт. |
82,3 |
|
II |
|
259–261 |
0,86** |
Оранж. |
80,1 |
|
III |
|
242–244 |
0.42* |
Желтый |
43.4 |
|
IV |
|
263–265 |
0,87** |
Красный |
92,9 |
|
V |
|
287–289 |
0,37* |
Светло желт. |
78.4 |
Системы: *Гексан-ацетон (2:1); **Бензол-ацетон (5:1)
Ди-2,5-ксилидингоссипол образует с ацетоном стабильный клатрат. Кристаллографические параметры монокристалла следующие: кристаллы моноклинные, пр.гр. Р21/n, C46H48O6N2·C3H6O, a= 13.5738(3) Å, b=12.4839(3) Å, c=26.1622(5) Å, β= 98.277(2)°, V= 4387.11(17) Å3, M= 782.94, Z=4, Dвыч.= 1.185 г/см3. R=0.0666 для 5500 отражений. Молекулы ди-2,5-ксилидингоссипола образуют бесконечные цепочки с помощью Н-связей элементом симметрии плоскостью скользящего отражения. Укладка этих цепочек приводит к хозяйскую матрицу с небольшими полостями. К каждой хозяйской молекулы водородно связана одна молекула ацетона, которая заполняет одну из межклеточную полость [4]. .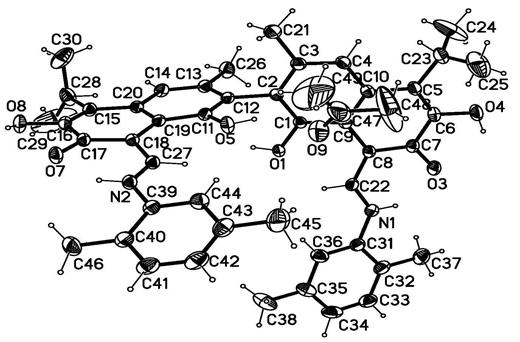
Рис. 1. РСА. Конформация и нумерация атомов молекул ди-2,5-ксилидингоссипола и ацетона в структуре клатрата ди-2,5-ксилидингоссипола с ацетоном
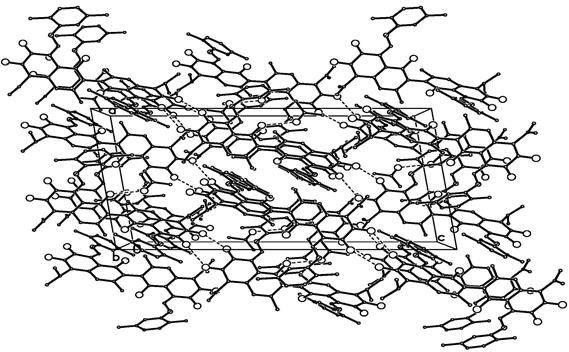
Рис. 2. РСА. Кристаллическая структура клатрата ди-2,5-ксилидингоссипола с ацетоном
Таблица 2
Водородные связи в структуре клатрата ди-2,5-ксилидингоссипола с ацетоном
|
Связь |
D-Н, (Å) |
Н…A, (Å) |
D…A, (Å) |
Угол, D-H<A(о) |
Операция симметрии для атома А |
|
Внутримолекулярные водородные связи |
|||||
|
N1- H1N.. O3 |
0.86 |
1.93 |
2.591(3) |
132.4. |
|
|
N2- H2N.. O7 |
0.86 |
1.92 |
2.593(3) |
133.5 |
|
|
O4- H4O.. O3 |
0.82 |
2.14 |
2.615(3) |
116.7 |
|
|
O8- H8O.. O7 |
0.82 |
2.20 |
2.632(3) |
112.9 |
|
|
Межмолекулярные водородные связи |
|||||
|
O5- H5O.. O9 |
0.82 |
2.06 |
2.751(3) |
142.00 |
|
|
O4- H4.. O7 |
0.82 |
2.25 |
2.978(3) |
147.6 |
x-1/2, 3/2-y, 1/2+z |
|
O8 — H8O.. O3 |
0.82 |
2.08 |
2.794(3) |
145.4 |
1/2+x,3/2-y,z-1/2 |
С целью дальнейшего изучения особенностей структуры полученных производных госсипола и формирования клатратов производных госсипола была предпринята попытка получения клатрата ди-2,5-ксилидингоссипола с ацетоном. При кристаллизации ди-2,5-ксилидингоссипола из раствора в ацетоне был получен клатрат с хозяин-гость соотношением 1:2 и методом РСА установлена его кристаллическая структура. При этом ди-2,5-ксилидингоссипол образует смешанный клатрат с ацетоном. Половина молекул ацетона Н-связана с хозяйскими молекулами, образуя тем самым матрицу, другая часть гостевых молекул размещаются в полостях этой матрицы.
Литература:
1. Садыков А. С., Жданов В. М., Асланов Х. А., Ершов Ф. М., Ауелбеков С. А., Душанбиева С. Баринский И. Ф., Каламкарян А. Г., Исмаилов А. И., Биктимиров Л., Барам Н. И./Антигерпетическое средство–мегосин//- М.:А.С. 1062919 СССР, МКИ А61К 31/00
2. Асланов Х. А., Хаитбаев А. Х., Ауелбеков С. А., Хаитбаев Х. Х., Ахунов А. А. Поиск новых биоактивных производных госсипола // Кимё ва фармация.-Тошкент, 1995.-№ 4–5.-Б.12.
3. Барам Н. И., Исмаилов А. И., Зияев Х. Л., Режепов К. Ж. Биологическая активность госсипола и его производных//Химия природн. соедин.-Ташкент, 2004.-№ 3.-С.171–176.1
4. Sh.M.Hakberdiev, S. A. Talipov, D. N. Dalimov and B. T. Ibragimov 2,2'-Bis{8- [(benzylamino)methylidene]-1,6-dihydroxy-5-isopropyl-3-methylnaphthalen-7(8H)-one} ActaCryst. (2013). E69, o1626-o1627