Методами эмиссионной мессбауэровской спектроскопии 67Cu(67Zn) и измерения скорости радиоактивного распада 64Cuпоказано, что примесные атомы меди занимают катионные узлы в решетке AgClи находятся в состоянии Cu+, если кристаллы AgCl легируются медью методом диффузии в вакууме. Диффузия в атмосфере Cl2 приводит к частичному переходу примеси меди в состояние Cu2+ и образованию ассоциатов Cu2+ с катионными вакансиями. Зависимость зарядового состояния примеси меди от природы атмосферы отжига кристаллов AgCl объясняется влиянием атмосферы на концентрацию катионных вакансий.
Ключевые слова: примесные атомы, электронный обмен, эмиссионная мессбауэровская спектроскопия.
1. Введение
Мессбауэровская спектроскопия является эффективным методом исследования состояния примесных атомов в твердых телах [1–9]. Из-за плохой растворимости примесных атомов такие исследования обычно выполняются в варианте мессбауэровской спектроскопии (EMS) [10]. В EMS, долгоживущий радиоактивный изотоп родителей вводят в образец, где он распадается, чтобы дать мессбауэровских зондов (дочерний изотоп). В частности, в этом исследовании используют 67Cu (с периодом полураспада 59 часов) в качестве материнского изотопа производства 67Zn зонд мессбауэровской при β-распаде (см. рис. 1).
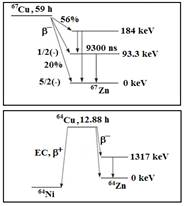
Рис. 1. Схематическое изображение радиоактивного распада 67Cu и 64Cu.
Это означает, что информация, эмиссионной мессбауэровской спектоскопии связана с позицией решетки и окружающей среды симметрии одного из материнского атома и зарядового состояния атома. В некоторых случаях (для 67Cu (67Zn) примесных атомов в AgCl в настоящем исследовании), анализ экспериментальных данных позволяет делать выводы которые могут быть достигнуты, касающиеся не только позиции и локальная симметрия родительских атомов примеси, но и их зарядовых состояниях. Тем не менее, независимые данные, как правило, требуются, о зарядовых состояний атомов родителей. В данном исследовании, предлагается, что можно использовать зависимость скорости радиоактивного распада изотопа 64Cu на медной валентности [11] в качестве источника такой информации.
2. Детали эксперимента
Хлорид серебра — монокристаллы были выращены методом со-Баргер из оптически чистого AgCl (концентрации примесей не превышает 2 × 10–4 моль. %). Диски диаметром 10 мм и толщиной 5 мм с ориентацией (100) были вырезаны из выращенного кристалла. Образцы подвергались травлению в 10 %-ным раствором тиосульфата натрия и отжигались при температуре 350 ° С в течение 4 часов в атмосфере аргона.
Радиоактивные AgCl: 67Cu и AgCl: 64Cu источники были подготовлены путем диффузии 67Cu или 64Cu в AgCl монокристаллов. Для этого часть 67CuCl2 или 64CuCl2 растворенного в воде было помещено на поверхности кристалла, который затем сушат и отжигают в течение 1 часа при 440°С в вакууме (AgCl: Cu (I)-типа образцов) или в атмосфере хлора (AgCl: Cu (II) типа образцов). После отжига кристалла поверхности травились в горячей соляной кислотой, промывались этанолом и затем протравливались раствором тиосульфата натрия. На основе данных Cu диффузии для AgCl, средняя глубина диффузии меди при указанных выше условиях отжига была предсказана, около 0,2 см.
67Cu (67Zn) мессбауэровские спектры были сняты при 4,2 К с использованием электродинамических спектров с ZnS поглотителем имеющие 1000 mg.cm-2 поверхностной плотности в терминах 67Zn.
Скорость распада для 64Cu радиоактивных источников были проведены при комнатной температуре путем обнаружения вторичных 511 кэВ квантов. ФЭУ и 76x76 мм NaI (Tl) кристалл с 40x20 мм также были использованы в детекторе. Источник под следствием был помещен в центр скважины.
3. Экспериментальные результаты и обсуждение
Типичные мессбауэровских спектров AgCl: 67Cu, показаны на рис. 1, а результаты их обработки приведены в таблице I.
Таблица 1
Параметры 67Cu (67Zn) мессбауэровских спектров и Δλ / λ значения для 64Cu (относительно CuCl)
(IS является изомерным сдвигом по отношению к ЦНС, eQUzz является квадрупольной постоянной взаимодействии, Q является квадрупольным моментом 67Zn, Uzz является основным компонентом тензора градиента электрического поля на ядрах 67Zn, и P-доля синглетной компоненты в спектре).
|
|
Spectrum I |
Spectrum II |
|
|||
|
IS (μm.s-1) |
eQUzz (MHz) |
IS (μm.s-1) |
eQUzz (MHz) |
P (%) |
(Δλ/λ).104 |
|
|
AgCl:Cu(I) |
-52.5(5) |
< 0.5 |
|
|
100 |
-0.005(10) |
|
AgCl:Cu(I) |
-52.5(5) |
< 0.5 |
-60.0(5) |
2.0(3) |
15(5) |
-1.5(1) |
|
CuCl2 |
|
|
|
|
|
-2.1(1) |
Спектр AgCl: Cu (I) образец является синглетной линией, соответствующей изолированному 67Cu примесных атомов (верхний спектр на рис 2.). Она будет упоминаться далее как спектр I. Изомерный сдвиг спектра I типичен для Zn2+ соединений, а также отсутствие квадрупольного расщепления указывает на кубическую симметрию локального окружения атомов меди.
Спектры образцов AgCl: Cu (II) представляют собой суперпозицию выше синглета (спектр I) и квадрупольного триплет (спектр II) (нижний спектры на рис. 2). Изомерный сдвиг спектра II соответствует Zn2+ квадрупольное расщепление указывает на понижение локальной симметрии атомов примеси меди. Избыточный заряд ионов Cu2+ компенсируется за счет катионных вакансий формирования ассоциации с Cu2+. Таким образом, спектр II должен быть характерен для 67Zn2+ центров, образующихся в β-распаде 67Cu2+ AgCl на местах катионов, с катионной вакансии в их ближайшем окружении. Это приводит к более низкой локальной симметрии центров в квадрупольного расщепления спектра.
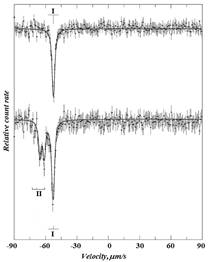
Рис. 2. Мессбауэровские спектры 67Cu (67Zn) примесных атомов в AgCl при 4,2 К. верхний и нижний спектры соответствуют отжига в вакууме и хлора, соответственно. На нижнем спектре показаны позиции синглетного (спектр I) и квадрупольного триплета (спектр II)
По современным представлениям, преобладающим дефектом в AgCl являются катионные вакансии (акцепторы) и интерстициальной ионов Ag+ (доноров). Отжиг в вакууме обеспечивает электрическую нейтральности AgCl решетки и установлению равновесия между катионом вакансий и внедренным ионом Ag+. В результате примесные атомы меди в основном занимают нормальных состояния катиона, а в нейтральным состояние донор Cu+. С другой стороны, отжиг в хлоре делает концентрацию катионных вакансий выше. Электронейтральность решетки требует в этих условиях переход атомов примеси меди в ионизированном состоянии донора Cu2+, и взаимное притяжение ионизированных доноров и акцепторов должна привести к формированию Cu2+ — вакансии ассоциации, которая была открыта в спектры в стадии рассмотрения. Таким образом, приведенные спектры хорошо согласуются с теоретическими предсказаниями о влиянии окружающей атмосферы на генерации дефектов в AgCl подвергают термической обработке.
Тем не менее, интерпретация спектров I и II основана на довольно произвольных предположениях о зарядовых состояний атомов примеси меди и требует некоторой независимой экспериментальной проверке. Это было сделано путем измерения скорости распада радиоактивных ядер 64Cu. Распад радиоактивных ядер, как известно, описывается выражением:
N = N0exp(-λt) (1)
где: N и N0 — число ядер в момент времени T и в начальный момент времени, соответственно, λ = LN2/T1/2 является скоростью распада, а T1/2 — периодом полураспада.
Как установлено экспериментально (для 64Cu, см., например, [2]), электронный захват (ЕС) λ скорость распада зависит от состояния валентных распадающихся атомов. Вариации скорости распада около 0,01 %, и, как правило, описывается выражением:
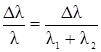 (2)
(2)
где Δλ = λ1 — λ2 и λ1 и λ2 являются скорости распада для изотопов в химических формах 1 и 2.
Там нет надежной теории, описывающей зависимость Δλ/λ на химических параметров радиоактивного соединения. Тем не менее, ключевая роль плотности электронов на распадающегося ядра, | Ψ (0) | 2, является общепринятым:
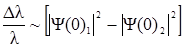 (3)
(3)
где |Ψ(0)1| 2 и |Ψ(0)2|2 — электронные плотности на радиоактивных ядер в соединениях 1 и 2, соответственно.
Экспериментальный метод определения Δλ/ λ состоит в измерении нормированный R отношение скоростей счета в двух источниках 1 и 2, как функция времени (квази-дифференциальным методом). Эта зависимость описывается выражением
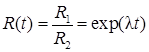 (4)
(4)
где: Rt = C1/C2, где C1(T) = kλ1N01exp(-λ1t) и c2(T) = k λ2N02exp (λ2Т) — скорость счета источников 1 и 2 соответственно; К эффективности детектора; N01 и N02 — числа радиоактивных ядер в источниках 1 и 2, соответственно, в начальный момент времени, и Rt — начальное отношение скоростей счета.
Изотоп 64Cu (T1/2 = 12,88 ч) обеспечивает оптимальные условия для Δλ / λ квазидифференциальным методом. Распад 64Cu происходит по трем каналам: ЕС (43 %), β + (19 %), β-и (38 %), как показано на рисунке 1. большое количество экспериментальных данных о зависимости λ от химического состояния меди в настоящее время доступны для этого изотопа [11].
На рисунке 3 показаны типичные R (т) зависимости записанный для источника пар CuCl, CuCl2, CuCl-AgCl: Cu (I) и CuCl-AgCl: Cu (II). Можно увидеть из таблицы 1 и Рис. 3 что максимальное значение Δλ/λ наблюдается для CuCl, CuCl2. Этот факт имеет очевидное объяснение: чем выше соединения содержат медь в двух различных валентных состояниях, Cu+ и Cu2+, с электронными конфигурациями 3d9 и 3d10. Переход от 3d10 увеличивается до 3d9|Ψ(0)|2 и, как следствие, повышает скорость распада 64Cu.
Сравнение со случаем для CuCl-AgCl: Cu (I) показывает, что источником Δλ/λ значения лежит в пределах погрешности (рис. 3 в), следовательно, с указанием Cu+ состояние примеси меди в легированных AgCl в вакууме. В противоположность этому, Δλ/λ значение для CuCl-AgCl: Cu (II) источник значительно выше (рис. 3 б). Другими словами, отжиг AgCl в хлоре стабилизирует атомы меди в Cu2+ состояние. С Δλ/λ значение считается пропорциональной Cu2+ фракции, AgCl: Cu (II) образцы должны быть около 70 % меди в таком состоянии, что хорошо согласуется с данными мессбауэровской спектроскопии.
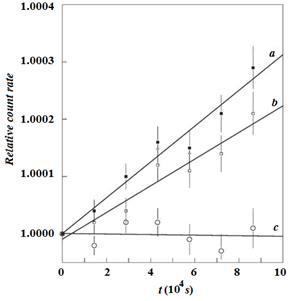
Рис. 3. R (т) зависимостей для источника пар CuCl, CuCl2 (а), CuCl-AgCl: Cu (II), (б) и CuCl-AgCl: Cu (I), (с). На вставке показана схема распада 64Cu
4. Выводы.
Исследования диффузии AgCl, легированных монокристаллов 67Cu (67Zn) эмиссионной мессбауэровской спектроскопии и измерения скорости распада 64Cu показали, что атомы меди заменить серебро. Тем не менее, заряд состояний меди оказалось зависит от допинга часть меди в Cu 2+ состояния. Зависимость состояния зарядки примеси меди от окружающей атмосферы при отжиге кристаллов AgCl объясняется влияние окружающей атмосферы от концентрации катионных вакансий.
Литература:
1. Murin A. N., Lurje B. G., Seregin P. P., Cherezov N. K. Study the state of iron in single crystals AgCl by Mössbauer. Solid State Physics. 1967. v. 8, N 1. pp. 3291–3294.
2. Murin A. N., Lurje B. G., Seregin P. P., Study the state of the iron ions in the silver halides by Mössbauer. Solid State Physics.1967. v. 9. N 5. pp. 1424–1433
3. Murin A. N., Lurje B. G., Seregin P. P., On the state of impurity iron ions in silver halides. Solid State Physics. 1967. v. 9. pp. 2428–2430
4. Murin A. N., Lurje B. G., Seregin P. P., On the state of impurity iron ions in silver halides. Solid State Physics. 1968. v. 10. pp. 923–925
5. Efimov A. A., Bondarevskiy S. I., Seregin P. P.,Shipatov V. T., Mossbauer effect on the impurity atoms of tin in the silver halides. Solid State Physics. 1970. v. 12. pp. 949–950
6. Efimov A. A., Bondarevskiy S. I., Seregin P. P.,Shipatov V. T., Mossbauer effect on the impurity atoms of tin in alkali halides. Solid State Physics. 1970. v. 12. N 4. pp.1244–1248
7. Seregin P. P., Savin E. P., Investigation of impurity atoms 129Te in alkali halides by Mössbauer. Solid State Physics. 1971. v. 13. N 11. pp. 3388–3392
8. Seregin N. P., Nasredinov F. S., Bondarevskii S. I., Ermolaev A. V., Seregin P. P. The charge state of copper impurity atoms in AgCl annealed in vacuum or chlorine. Journal of Physics Condensed Matter. 2001. V. 13. N 11. pp. 2671–2676
9. Murin A. N., Seregin P. P. Investigation of cobalt-, iron- and tin-doped silver and alkali halides by the Mossbauer method. Physica Status Solidi (A) Applied Research. 1970. V.2. N 2. pp.663–677.
10. Bordovsky G., Marchenko A., and Seregin P. Mossbauer of Negative Centers in Semiconductors and Superconductors. Identification, Properties, and Applicaton. Academic Publishing GmbH & Co. 2012. pp.499.
11. Bondarevskiy S. I., Masterov V. F., Nasredinov F. S., Seregin N. P., Seregin P. P., Valence states of copper atoms in the metallic oxides of copper determined from the change in the electron-capture constant of 64Cu. Solid State Physics. 1998. v. 40. N 10. pp. 1793–1794.







