В данной работе освещаются различные аспекты терапии пациентов с ювенильным идиопатическим артритом (далее ЮИА), рациональность использования генно-инженерных биологических препаратов (далее ГИБП), в частности этанерцепта (Энбрела)
Ключевые слова: дети, ювенильный идиопатический артрит, этанерцепт
Актуальность проблемы: Ювенильные артриты — наиболее часто встречающиеся ревматические заболевания у детей. В соответствии с современными представлениями, ЮИА — артрит неизвестной этиологии, который начинается в возрасте до 16 лет и длится по крайней мере в течение 6 нед. Хроническое, неуклонно прогрессирующее течение заболевания приводит к быстрому развитию инвалидизации больных, снижению качества жизни, социальной и психологической дезадаптации.
Современными рекомендациями по лечению ЮИА с целью контроля над течением заболевания предусмотрено назначение базисных противоревматических препаратов, среди которых предпочтение отдают метотрексату. Неэффективность последнего в адекватных дозах (10–15 мг/м2 поверхности тела) является показанием для назначения генно-инженерных биологических препаратов. В настоящее время в Российской Федерации для лечения ЮИА зарегистрированы следующие ГИБП: адалимумаб, этанерцепт, абатацепт, тоцилизумаб, канакинумаб. Проведенные рандомизированные клинические исследования показали их эффективность и безопасность. Опубликованы единичные работы, посвященные анализу эффективности ГИБП в условиях реальной клинической практик. В единичных зарубежных исследованиях было показано влияние терапии отдельных ГИБП (этанерцепт) на «стоимость болезни».
Этанерцепт является конкурентным ингибитором связывания ФНО-α с его рецепторами на поверхности клеток и таким образом ингибирует биологическую активность ФНО-α. Этанерцепт медленно абсорбируется из мест инъекций при подкожном введении, достигая максимума через 48 часов. Биодоступность составляет 76 %. Этанерцепт блокирует не только ФНО-α, но и ФНО-β (лимфотоксин-α). Он полностью состоит из человеческого белка. У взрослых больных препарат вводится подкожно по 25 мг 2 раза в неделю или по 50 мг один раз в неделю. Доза препарата у детей составляет 0,4 мг/кг 2 раза в неделю или 0,8 мг/кг еженедельно.
Цель работы: оценить эффективность и безопасность применения этанерцепта при лечении пациентов с ЮИА.
Материалы и методы: под нашим наблюдением находилось 23 ребенка (6 мальчиков и 17 девочек в возрасте от 4 до 17 лет (средний возраст — 7,8 лет). В большинстве случаев заболевание развилось в раннем и дошкольном возрасте (средний возраст в дебюте болезни — 4,3+2,7 года). Длительность болезни составила 7,5+3,3 года, в том числе до назначения этанерцепта — 4,3+3,12 года. У 15 детей был установлен серонегативный полиартрит, у — 4 персистирующий олигоартрит, у 2 больных — ювенильный артрит с системным началом (течение болезни по типу полиартрита), у 2 больных — артрит, связанный с энтезитом. Этанерцепт вводился подкожно из расчета 0,4 мг/кг (максимально 25 мг) 2 раза в неделю. Средняя разовая доза препарата составила 0,5+0,1 мг/кг. Все больные принимали нестероидные противовоспалительные препараты (преимущественно нимесулид), метотрексат внутримышечно (средняя доза 11,6+3,4 мг/кв.м/нед.), в том числе 8 больных в сочетании с циклоспорином А, 2 — с сульфасалазином. Глюкокортикоиды (метипред) принимали 4 больных. Оценка эффективности проводилась по критериям ACRpedi через 3, 6 и 12 месяцев от начала терапии.
Для оценки индекса функциональной недостаточности (ФН) использовалась русская версия опросника состояния здоровья ребенка the Childhood Health Assessment Questionnaire [3]. В качестве критериев эффективности терапии использовались педиатрические критерии Американской коллегии ревматологов: 1) общая оценка активности болезни врачом по ВАШ, 2) общая оценка тяжести болезни пациентом или родителями по ВАШ, 3) степень функциональной недостаточности по опроснику CHAQ, 4) число суставов с активным артритом, 5) число суставов с ограничением движений, 6) СОЭ или С-реактивный белок. Критериями АКРпед 30, 50 и 70 являлись снижение как минимум 3 из 6 показателей на 30, 50 и 70 % соответственно; при этом один показатель может ухудшиться на 30 % и более.
С целью мониторинга эффективности и безопасности терапии всем больным проводились общие анализы крови и мочи, биохимический анализ крови, иммунограмма (С-РБ, сывороточные иммуноглобулины А, М, G, циркулирующие иммунные комплексы), реакция Манту и/или Диаскин-тест, а также рентгенография ОГК каждые 6 месяцев.
Статистическая обработка результатов проводилась в операционной среде Windows2000 с использованием статистической программы «STATISTICA 6.0». При описании количественных данных в качестве меры центральной тенденции указывается среднее арифметическое (М), в качестве меры рассеяния — среднее квадратическое (стандартное) отклонение (σ).
Результаты. Через 3 месяца от начала лечения улучшение (критерий ACR30) было установлено у 21 больного (91,3 %), из них критериям ACR50 соответствовали 16 больных (69,6 %), ACR70–14 (60,9 %). Через 6 и 12 месяцев критериям ACR30 отвечали 22 ребенка (95,6 %), ACR50–21 ребенок (91,3 %), ACR70–20 (86,9 %). В связи с отсутствием клинически значимого улучшения лечения этанерцептом было прекращено у 1 больного. Через 24 месяца от начала лечения большинства больных, продолживших лечение (20/22) был достигнут статус «неактивной болезни», у 2 больных сохранялась минимальная степень активности болезни. Подавляющие большинство больных (22/23) хорошо переносили лечение препаратом. Однако, у 1 больной с олигоартритом отмечалось развитие увеита, что послужило основание для прекращения лечения этанерцептом. У 1 больного был выявлен вираж туберкулиновой пробы. На период проведения химиопрофилактики лечение препаратом было приостановлено.
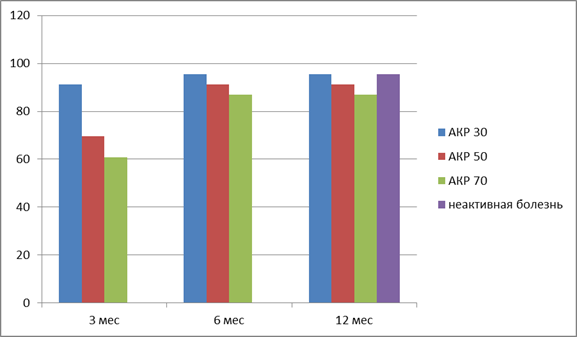
Рис. 1 Оценка эффективности терапии по критериям Американского колледжа ревматологов
Заключение. Назначение этанерцепта позволило добиться улучшения у подавляющего большинства больных (95,6 %), в том числе достичь клинико-лабораторной ремиссии у 20 больных (86,9 %). Отмечено постепенное нарастание эффективности лечения препаратом на протяжении 2 лет наблюдения. Не отмечено случает развития вторичной неэффективности. В целом препарат этанерцепт показал не только высокую эффективность, но хорошую переносимость. Развитие увеита и виража тубпроб соответствует литературным данным. Таким образом, препарат является высокоэффективным препаратом для лечения ювенильных артритов, рефрактерных к базисным противоревматическим препаратам. С целью своевременного выявления нежелательных эффектов больной подлежат регулярному тщательному клинико — лабораторно — инструментальному мониторинг.
Литература:
1. Алексеева Е. И., Бзарова Т. М. Результаты открытого, проводимого в одном центре, нерандомизированного. Без группы сравнения наблюдательного исследования оценки эффективности и безопасности терапии этанерцептом в комбинации с метотрексатом у пациентов с ювенильным идиопатическим артритом // Вопросы современной педиатрию — 2011ю — Том 10, № 5 — С. 24–31.
2. Малиевский В. А. Ювенильные артриты: эпидемиология, медико-социальные и экономические последствия, качество жизни: Автореферат дисс. … докт. мед. наук. — Москва, 2006. — 38 с.
3. Российский адаптированный вариант опросников для оценки качества жизни и состояния здоровья детей с ювенильными хроническими артритами / Н. Н. Кузьмина, И. П. Никишина, А. В. Шайков [и др.] // Научно–практическая ревматология. — 2002. — № 1. — С. 40–47.
4. Cassidy J., Petty R. Textbook of Pediatric Rheumatology. — Elsevier, 2011.
5. Horneff G., Foeldvari I., Kuemmerle-Deschner J. Switching of biologics in juvenile idiopathic arthritis // Ann. Rheum. Dis. — 2011;70 (Suppl3). — Р. 402.
6. Lovell D. Biologic Agents for the Treatment of Juvenile Rheumatoid Arthritis // Pediatr. Drugs. — 2004. — Vol. 6(3). — P. 137–146.
7. Petty R. E., Southwood T. R., Manners P. et al. International League of Associations for Rheumatology classification of juvenile idiopathic rthritis: second revision, Edmonton, 2001. — // J. Rheumatol. — 2004; 31.- Р. 390–392.
8. Population pharmacokinetic analysis and simulation of the time-concentration profile of etanercept in pediatric with juvenile rheumatoid arthritis / D. S. Yim, H.Zhou, M.Buckwalter [et al.] // J.Clin.Pharmacol. — 2005. — Vol. 45(3). — P. 246–256.
9. Safety and efficacy of high dose etanercept in treatment of juvenile rheumatoid arthritis / S.Takei, D.Groh, B.Bernstein [et al.] // J.Rheumatol. — 2001. — Vol. 28(7). — P. 1677–1680.
10. D. Windschall, G. Horneff Safety and efficacy of etanercept in children with theJIAa categories extended oligoarthritis, enthesitis related arthritis and psoriasis arthritis // Ann. Rheum. Dis. — 2013;72 (Suppl3). — Р. 71.







