В статье представлены результаты исследования сорбционной активности свекловичного жома, активированного угля и полифепана по отношению к катионам свинца. Показано, что свекловичный жом связывает значительно сильнее Pb2+, что обусловлено наличием пектина, обладающего гидрофильными и комплексообразующими свойствами по сравнению с гидрофобными исследуемыми энтеросорбентами.
Ключевые слова:сорбция, свекловичный жом, полифепан, активированный уголь, свинец.
Загрязнение окружающей среды химическими элементами приводит к избыточному их поступлению в организм человека, что пагубно влияет на здоровье людей. Поиск соединений с высокой сорбционной активностью по отношению к токсическим соединениям и разработка на их основе новых лекарственных препаратов являются важными задачами современной экспериментальной фармакологии и фармации. Среди веществ, связывающих химические элементы и токсические соединения, вызывают интерес пищевые волокна, в частности пектин. Препараты на его основе применяются в качестве энтеросорбентов (Фитосорбовит, Полисорбовит-50, Полисорбовит-95). Однако, производство пектина дорогой и трудоемкий процесс [1]. Мы предлагаем использовать в качестве энтеросорбента свекловичный жом. Существенным преимуществом использования свекловичного жома в качестве основы для создания энтеросорбента, является доступность сырья, меньшая сложность технологического процесса получения.
Цель работы — изучить металлсвязывающую активность и провести сравнительный анализ сорбционной способности свекловичного жома и лекарственных препаратов из группы энтеросорбентов по отношению к ионам свинца.
Объектом исследования являлись энтеросорбенты: активированный уголь (ОАО «Ирбитский химфарм завод»), полифепан (ЗАО «Сайнтек»), а также свекловичный жом, полученный после переработки плодов и высушенный естественным путем. Ионы свинца брали в виде солей Pb(NO3)2, используя реактив квалификации «х.ч».. Количественный анализ катионов свинца в растворе проводили титриметрическим методом по следующей методике. В колбу для титрования отбирали мерной пипеткой 2 мл анализируемого раствора, добавляли 0,1–0,2 г сухого уротропина до рН = 5,0, три капли индикатора ксиленолового оранжевого и титровали стандартным раствором ЭДТА (0,025 М) до перехода фиолетовой окраски в лимонно-желтую [2].
Важнейшими характеристиками сорбентов являются величина сорбционной емкости и время достижения сорбционного равновесия.
Кинетику сорбции исследовали методом ограниченного объема раствора. Для получения кинетических кривых сорбции в серию пробирок помещали навески (m) адсорбента по 1 г, заливали их 0,05 л (V) водного раствора соли исследуемого металла и выдерживали от 5 мин до 1 ч. Начальная концентрация (C0) ионов металлов составляла 0,025 моль/л. Через определенные промежутки времени раствор отделяли от сорбента и выявляли в нем текущую концентрацию ионов металла (CT) титриметрическим методом. Сорбционную емкость сорбентов (АT) в каждый данный момент времени рассчитывали по формуле:
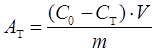 .
.
Степень извлечения (α) определяли следующим образом:
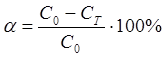 .
.
На рис.1. представлена зависимость сорбционной емкости сорбентов в каждый момент времени в отношении ионов свинца.
По полученным данным была рассчитана связывающая активность сорбентов, т. е. степень извлечения ионов свинца (рис.2). Изучение скорости сорбционных процессов показало, что связывание ионов свинца свекловичным жомом, происходит достоверно быстрее, чем активированным углем и полифепаном.
Через 5 мин 1 г свекловичного жома связывает в среднем 23,88 % свинца, активированный уголь — 4,54 %, а полифепан всего 1,16 %. Таким образом, процент связывания ионов свинца в первые 5 минут свекловичным жомом в 5 раз больше, чем активированным углем и в 20 раза, чем полифепаном. Однако, через 10 мин степень извлечения свинца свекловичным жомов в 2,6 раза больше, чем активированным углем и в 8,7 раз, чем полифепаном, через 15 мин соответственно в 3 и 6 раз, через 20 мин — 3 и 5 раз, через 60 мин — 3 и 5 раз.
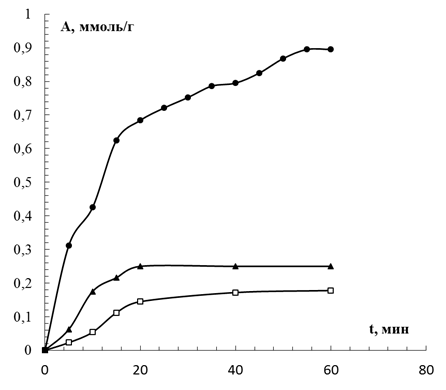
Рис. 1. Кинетика сорбции ионов свинца энтеросорбентами: ● — свекловичный жом; □ — полифепан; ▲ — активированный уголь
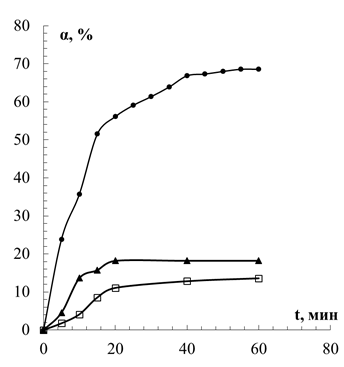
Рис. 2. Степень извлечения ионов свинца энтеросорбентами: ● — свекловичный жом; □ — полифепан; ▲ — активированный уголь
Полученные данные свидетельствуют, что активированный уголь и полифепан, имея гидрофобную поверхность, обладают малым сродством к молекулам воды и гидратированным ионам [3]. Высокая сорбционная активность свекловичного жома, обусловленная наличием пектина, физические свойства которого проявляются как гидрофильный коллоид и поэтому обладающего большим сродством к молекулам воды и гидратированным ионам, а также за счет наличия в составе пектина карбоксильных и гидроксильных групп галактуроновой кислоты способствующих хелатообразованию с ионами d- металлов [3, 4]. Максимальное количество свинца, которое может быть связано 1 г сорбента составляет: полифепан — 36,88 мг/г, активированный уголь — 51,8 мг/г, свекловичный жом — 185,44 мг/г. Таким образом, свекловичный жом, может быть рекомендован в качестве детоксиканта ионов свинца, что предполагает разработку лекарственной формы на его основе.
Литература:
1. Рябинина Е. И. Влияние щавелевой кислоты на выход пектина из яблочных и цитрусовых выжимок / Е. И. Рябинина, Е. Е. Зотова, Н. И. Пономарева, И. П. Чурилова // Перспективы развития науки и образования: сборник научных трудов по материалам Международной научно-практической конференции 28 февраля 2015 г.: в 13 частях. Часть 6; М-во обр. и науки РФ. Тамбов: Изд-во ООО «Консалтинговая компания Юком», 2015. — С. 126–127.
2. Харитонов Ю. Я. Аналитическая химия. Количественный анализ. Физико-химические методы анализа: практикум: учеб. пособие / Ю. Я. Харитонов, Д. Н. Джабаров, В. Ю. Григорьева. — М.: ГЭОТАР — Медиа, 2012. — 368 с.: ил.
3. Рябинина Е. И. Активность энтеросорбента полифепана по отношению к катионам некоторых d — металлов / Е. И. Рябинина, Е. Е. Зотова, Н. И. Пономарева, А. А. Тимашова, Н. А. Андреева // Прикладные информационные аспекты медицины. — 2014. — Т.17, № 2. — С.87–91.
4. Николаев В. Г. Современные энтеросорбенты и механизмы их действия / В. Г. Николаев, С. В. Михаловский, Н. М. Гурина // Эфферентная терапия. — 2005. — Т.11, № 4. — С. 3–17.







