Для экспериментов использовали хлорид калия Тюбегатанского месторождения и нитрат кальция, полученного из промышленных отходов азотно-туковых заводов [1 и 2].
Опыты по конверсии нитрата калия из хлорида калия и нитрата кальция проводили в лабораторной установке, состоящей из стеклянного кварцевого реактора с мешалкой и электрическим подогревом. Температуру конверсии в реакторе поддерживали с помощью контактного термометра ТК-300, с точностью ±1°С. Скорость вращения и температура непрерывно регулировались.
Для исследования использовали кристаллический хлорид калия и нитрат калия. Опыты проводили в круглодонной колбе, на мешалке с подогревом, в которую загружали 20,54 г KCI, 24,59 г Ca(NO3)2 и 54,86 г H2O. Колбу с хлоридом калия и водой растворяли в магнитной мешалке при 660С, потом добавляли нитрат кальция. Конверсию проводили в течение 60 мин. После конверсии раствор охлаждали с целью извлечения из раствора нитрата калия. По полученному нитрату калия проводили анализы химического состава жидкой и твердой фаз. Из результатов анализов следует, что степень конверсии хлорида калия с нитратом кальция зависит от температуры и увеличивается с ее ростом.
Эксперименты по конверсии нитрата калия из хлорида калия и нитрата кальция проводили при больших температурных интервалах. По экспериментальным данным установили оптимальную температуру 660С. Процесс в основном заканчивается в течение 60 минут: при этом степень конверсии при 25, 40, 66 и 1000С составляет соответственно 52,0, 72,6, 96,7 97,1 %. Оптимальная температура 660С и дальнейшее увеличение продолжительности процесса практически не приводит к повышению степени конверсии. При 660С выход по калию достигает 33,45 %.
Таблица 1
Влияние соотношение KCI: Ca(NO3)2 на плотность суспензии при различных температурах
|
|
20 |
40,2 |
60 |
80 |
|
0,9; 1 |
1,557 |
1,540 |
1,527 |
1,506 |
|
1; 1,19 |
1,488 |
1,467 |
1,453 |
1,438 |
|
1; 23 |
1,420 |
1,400 |
1,382 |
1,367 |
|
1; 2 |
1,351 |
1,331 |
1,314 |
1,300 |
|
1; 5 |
1,289 |
1,276 |
1,263 |
1,256 |
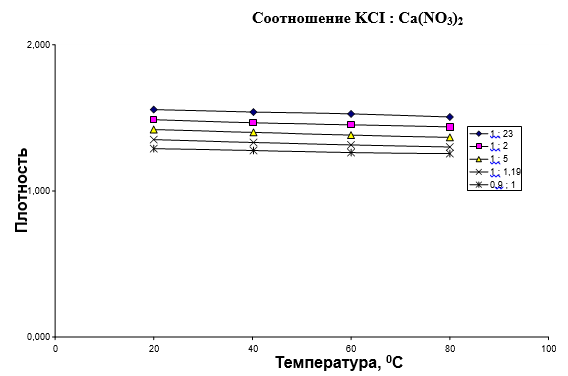
Рис. 1. Влияние температуры конверсии на плотность суспензии при различных соотношениях KCI: Ca(NO3)2
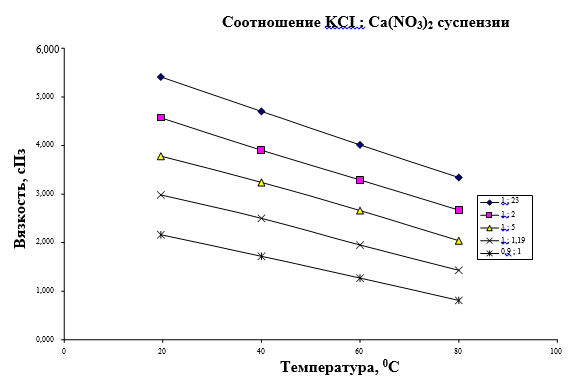
Рис. 2. Влияние температуры конверсии на плотность суспензии при различных соотношениях KCI: Ca(NO3)2.
Соотношение KCI: Ca(NO3)2 играет ключевую роль в конверсии нитрата калия. Нами было проведено детальное изучение, влияние и соотношение в широком интервале. В соотношении KCI: Ca(NO3)2 1: 0,3 в осадок упал до 5,6 г.
Таблица 2
Влияние соотношения KCI: Ca(NO3)2 на плотность суспензии при различных температурах. Влияние соотношения KCI: Ca(NO3)2 на вязкость суспензии
|
|
20 |
40 |
60 |
80 |
|
1; 23 |
5,410 |
4,700 |
4,010 |
3,340 |
|
1; 2 |
4,570 |
3,900 |
3,290 |
2,670 |
|
1; 5 |
3,780 |
3,240 |
2,660 |
2,040 |
|
1; 1,19 |
2,980 |
2,500 |
1,950 |
1,430 |
|
0,9; 1 |
2,160 |
1,720 |
1,270 |
0,810 |
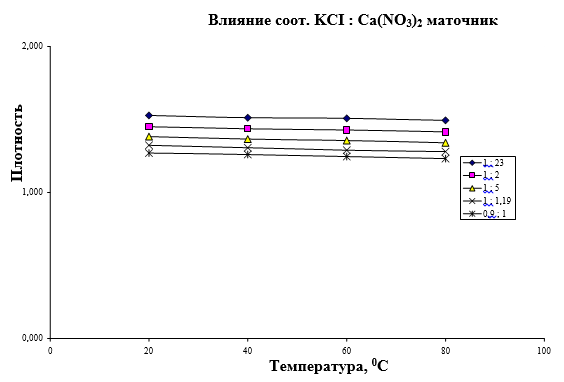
Рис. 3. Влияние температуры конверсии на плотность суспензии при различных соотношениях KCI: Ca(NO3)2
Таблица 3
Влияние соотношения KCI: Ca(NO3)2 на плотность суспензии при различных температурах. Влияние соотношения KCI+Ca(NO3)2 на плотность маточника
|
|
20 |
40 |
60 |
80 |
|
1; 23 |
1,527 |
1,512 |
1,507 |
1,494 |
|
1; 2 |
1,450 |
1,436 |
1,427 |
1,414 |
|
1; 5 |
1,382 |
1,365 |
1,355 |
1,340 |
|
1; 1,19 |
1,323 |
1,306 |
1,289 |
1,279 |
|
0,9; 1 |
1,270 |
1,260 |
1,245 |
1,231 |
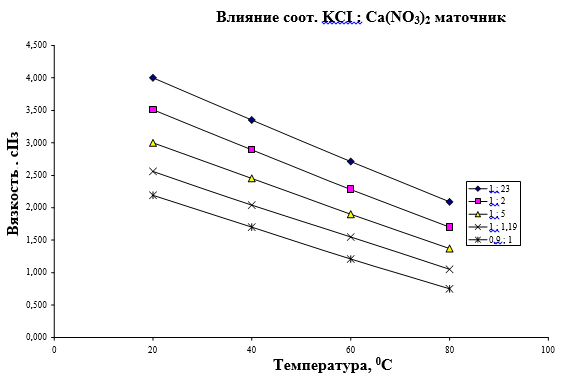
Рис. 4. Влияние температуры конверсии на плотность суспензии при различных соотношениях KCI: Ca(NO3)2
Таблица 4
Влияние соотношения KCI: Ca(NO3)2 на плотность суспензии при различных температурах. Влияние соотношения KCI+Ca(NO3)2 на вязкость маточника
|
|
20 |
40 |
60 |
80 |
|
1; 23 |
4,000 |
3,350 |
2,710 |
2,090 |
|
1; 2 |
3,510 |
2,890 |
2,280 |
1,700 |
|
1; 5 |
3,000 |
2,450 |
1,900 |
1,370 |
|
1; 1,19 |
2,560 |
2,040 |
1,550 |
1,050 |
|
0,9; 1 |
2,190 |
1,700 |
1,210 |
0,750 |
По лабораторным данным была разработана принципиальная блок-схема технологии производства нитрата калия и составлен материальный баланс на производство 1-ой тонны нитрата калия конверсионным методом.
Технологическая схема получения нитрата калия включает следующие операции:
1. Растворение хлористого калия в горячем растворе.
2. Фильтрация полученного раствора с целью отделения нерастворимых примесей.
3. Обменное разложение между KCI и Ca(NO3)2 с получением раствора KNO3.
2KCI + Ca(NO3)2 = 2KNO3 +CaCI2
4. Охлаждение полученного раствора в целях кристаллизации нитрата калия.
5. Отделение кристаллов нитрата калия методом центрифугирования.
6. Сушка полученного нитрата калия.
7. Маточный раствор после отделения нитрата калия подвергается упарке с целью отделения от маточника хлорида аммония.
8. Выделение из маточного раствора выпавших кристаллов CaCI2.
9. Сушка выделенного хлорида кальция.

Рис. 3. Принципиальная блок-схема технологии производства нитрата калия конверсионным методом.
Материальный баланс конверсии нитрата калия с хлоридом калия и нитратом кальция на 1 т. готовой продукции.

Рис. 4. Материальный баланс получения нитрата калия конверсионным методом из хлорида калия и нитрата кальция.
Литература
1. Безотходная технология получения нитрата калия на основе растворов. Дормешкин О. Б., Воробев Н. И., Новек Д. М. Белорусский государственный технологический университет. Хим.пром-сть, 2005. № 8. с375–381.
2. Самадий М., Мирзакулов Х. Ч., Кучаров Б., Хужамкулов С. Разработка технологии получения нитрата калия конверсионным методом на основе местного сырья. // Аналитик киме фанининг долзарб муаммолари- 2010: III-Республиканская научно-техническая конференция. 31–23 апреля 2010. — Термиз, 2010. с.226–227.







