Извлечение скандия, тория и РЗЭ фосфиноксидом разнорадикальным из сернокислых и смешанных растворов
Авторы: Литвинова Галина Николаевна, Мальцева Ирина Евгеньевна, Костикова Галина Валерьевна, Жилов Валерий Иванович
Рубрика: 1. Общие вопросы химии
Опубликовано в
II международная научная конференция «Современная химия: Успехи и достижения» (Чита, апрель 2016)
Дата публикации: 06.04.2016
Статья просмотрена: 638 раз
Библиографическое описание:
Литвинова, Г. Н. Извлечение скандия, тория и РЗЭ фосфиноксидом разнорадикальным из сернокислых и смешанных растворов / Г. Н. Литвинова, И. Е. Мальцева, Г. В. Костикова, В. И. Жилов. — Текст : непосредственный // Современная химия: Успехи и достижения : материалы II Междунар. науч. конф. (г. Чита, апрель 2016 г.). — Чита : Издательство Молодой ученый, 2016. — С. 3-8. — URL: https://moluch.ru/conf/chem/archive/162/10206/ (дата обращения: 26.04.2025).
В последнее время все больший интерес в России проявляется к разработке месторождения «Томтор», являющимся уникальным по запасам редкоземельных элементов (РЗЭ) и скандия. Содержание оксидов промышленно-ценных элементов в руде изменяется в широких пределах (%): Nb-1,63÷16,43; Y– 0,178÷2,94; Sc– 0,0146÷0,098; ∑ РЗЭ — 2,2÷27,79. Также в рудах этого месторождения содержится уран (0,018÷ 0,0892 %) и торий (0,0191÷0,3040 %) [1].
Чаще всего для вскрытия монацитовых концентратов применяют сернокислотный метод, в результате чего образуются растворы, содержащие ценные компоненты, высоко концентрированную серную кислоту, фосфат-анионы. Для переработки полученных растворов может быть использован метод жидкостной экстракции с использованием экстрагентов различных классов и их смесей. Целью настоящей работы являлось изучение возможности извлечения ценных компонентов (РЗЭ, Sc, Th) из сернокислых и смешанных сульфатных растворов фосфиноксидом разнорадикальным (ФОР).
Фосфиноксид разнорадикальный (ФОР) был единственным из класса оксидов третичных фосфинов, который получали в СССР в промышленном масштабе иодидным методом. В настоящее время производство его прекращено. Ведущие фирмы Японии, Канады и США выпускают триоктилфосфиноксид и его аналоги: продукт, включающий разные радикалы нормального строения С6-С8 (Cyanex 923), стерически загруженный оксид, в котором два линейных радикала С8 заменены на разветвленные 2,4,4-триметилпентильные радикалы (Cyanex 925), и др. [2].
Для оценки экстракционной способности ФОР была получена зависимость величин коэффициентов распределения (D) Sc, Th и РЗЭ от концентрации фосфиноксида в органической фазе при экстракции из 3М H2SO4 (рис.1). В качестве экстрагента были использованы растворы ФОР в декане с добавкой 10 % изоамилового спирта, что, как было показано ранее [3], не снижает экстракционную способность и предотвращает образование второй органической фазы.
Полученные данные свидетельствуют о том, что при концентрации ФОР более 25 % (0,64 М), степень извлечения Sc превышает 80 %, однако степень извлечения Th также составляет более 40 %, что не позволяет рассматривать ФОР как экстрагент для селективного извлечения Sc. Степень извлечения РЗЭ не превышает 9 % для всего исследованного интервала концентраций ФОР.
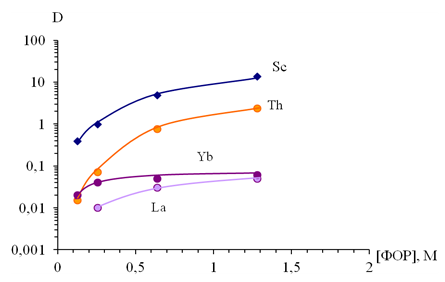
Рис. 1.Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации ФОР в декане с добавкой 10 % изоамилового спирта при экстракции из равновесной водной фазы, содержащей 3М H2SO4. [Sc]исх.~5 г/л, [Th]исх.~5 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л
Далее для 25 % ФОР была получена зависимость величин коэффициентов распределения скандия, тория, лантана (как легкого РЗЭ) и иттербия (как тяжелого РЗЭ) от концентрации серной кислоты в равновесной водной фазе (рис.2).
Во всем интервале концентраций H2SO4 лучше всех рассматриваемых элементов экстрагируется скандий, однако величины коэффициентов его распределения не превышают 4, величины коэффициентов разделения (β) Sc/Th не выше 5, что согласуется с ранее полученными данными (рис.1) и не является достаточным для проведения экстракционного процесса его селективного извлечения.
Одним из основных компонентов экстракционной системы является серная кислота. Во всем рассматриваемом интервале ее концентраций величины D не превышают 0,1, что свидетельствует о слабой экстракционной способности ФОР по отношению к H2SO4.
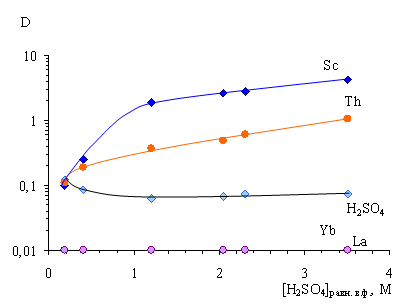
Рис. 2. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb и H2SO4 от концентрации серной кислоты в равновесной водной фазе [Sc]исх.~5 г/л, [Th]исх. ~10 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент — 25 % ФОР в декане с добавкой 10 % изоамилового спирта
Далее, для увеличения коэффициентов распределения рассматриваемых элементов, в систему была добавлена азотная кислота (рис.3). Однако, несмотря на существенно лучшую экстрагируемость нитратов Sc, РЗЭ и Th [4], это привело к падению величин D Sc и Th за счет конкурирующей экстракции азотной кислоты.
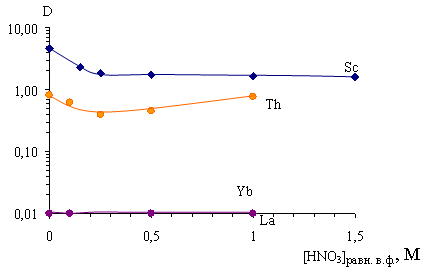
Рис. 3. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации HNO3 в равновесной водной фазе на фоне 3М Н2SO4. [Sc]исх.~5 г/л, [Th]исх. ~10 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент – 25 % ФОР в декане с добавкой 10 % изоамилового спирта
РЗЭ практически не экстрагируются ни из сернокислых (рис.2), ни из смешанных нитратно-сульфатных растворов (рис.3).
Также было рассмотрено введение в экстракционную систему LiNO3. Как и в предыдущем случае (рис. 3), это привело к падению величин коэффициентов распределения Sc и Th за счет перехода в органическую фазу HNO3.
Далее была получена зависимость величин коэффициентов распределения Sc, Th, La и Yb от изменения относительных концентраций LiNO3– H2SO4 в равновесной водной фазе (∑ [LiNO3+ H2SO4]=3M =const) (рис.4, табл.1).
Для всех рассмотренных элементов наблюдается возрастание коэффициентов распределения с увеличением относительного содержания LiNO3, что связано как с высокой высаливающей способностью нитрата лития, так и с лучшей экстрагируемостью нитратов Sc, Th и РЗЭ. Величины D ΣН+ также увеличиваются за счет преимущественного перехода в органическую фазу азотной кислоты. Во всем интервале концентраций H2SO4 и LiNO3 скандий и торий экстрагируются совместно, и оптимальным условием их отделения от тяжелых и легких РЗЭ является интервал соотношений LiNO3:H2SO4 1:2 и 1:1.
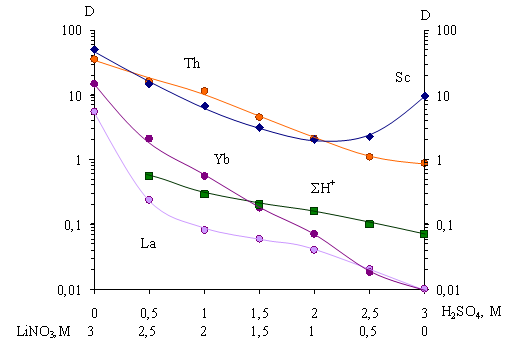
Рис. 4. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от изменения относительных концентраций LiNO3-H2SO4 в равновесной водной фазе ([LiNO3+H2SO4]=3M=const). [Sc]исх.~2 г/л, [Th]исх. ~8 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент – 25 % ФОР в декане с добавкой 10 % изоамилового спирта
Таблица 1
Величины коэффициентов разделения () взависимости от изменения относительных концентраций LiNO3-H2SO4 вравновесной водной фазе ([LiNO3+H2SO4]=3M=const). [Sc]исх.~2 г/л, [Th]исх. ~8 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент— 25% ФОР вдекане сдобавкой 10% изоамилового спирта
|
[H2SO4], М |
[LiNO3], М |
Sc/La |
Th/La |
Sc/Yb |
Th/Yb |
|
0,0 |
3,0 |
9,09 |
6,36 |
3,37 |
2,36 |
|
0,5 |
2,5 |
61,6 |
67,0 |
7,04 |
7,66 |
|
1,0 |
2,0 |
82,0 |
140 |
11,9 |
20,4 |
|
1,5 |
1,5 |
51,6 |
75,1 |
17,2 |
25,0 |
|
2,0 |
1,0 |
51,2 |
52,5 |
29,3 |
30,0 |
|
2,5 |
0,5 |
114 |
55,0 |
152 |
73,3 |
|
3,0 |
0,0 |
970 |
88,0 |
9700 |
880 |
Так как после вскрытия монацита в сернокислых растворах в значительных количествах может содержаться фосфат-анион, что может оказать существенное влияние на свойства экстракционной системы, для выбранных условий разделения были определены величины коэффициентов распределения и разделения Sc, Th, La, Yb в присутствии 0,5М Na3PO4 методом масс-спектроскопии с индуктивно связанной плазмой (МС-ИСП) на приборе Agilent 7500ce (табл. 2). В этом случае коэффициенты распределения скандия и, соответственно, коэффициенты разделения Sc/РЗЭ несколько уменьшаются. Для тория и РЗЭ присутствие в экстракционной системе фосфат-анионов не оказало существенного влияния на величины коэффициентов распределения и разделения.
Таблица 2
Величины коэффициентов распределения (D) Sc, Th, La, Yb иразделения (β) взависимости от изменения относительных концентраций LiNO3-H2SO4 вравновесной водной фазе ([LiNO3+H2SO4]=3M=const) вприсутствии 0,5М Na3PO4. [Sc]исх.~2 г/л, [Th]исх. ~8 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент – 25% ФОР вдекане сдобавкой 10% изоамилового спирта
|
H2SO4, M |
LiNO3, M |
D Sc |
D Th |
D La |
Sc/La |
Th/La |
D Yb |
Sc/Yb |
Th/Yb |
|
1,0 |
2,0 |
2,71 |
10,6 |
0,09 |
30,1 |
117 |
0,51 |
5,31 |
20,8 |
|
1,5 |
1,5 |
1,54 |
3,72 |
0,07 |
22,0 |
53,1 |
0,15 |
10,3 |
24,7 |
Таким образом при соотношении в исходном водном растворе сульфат и нитрат –анионов равном 1:2 и 1:1 для избирательного экстракционного извлечения Sc и Th и их отделения от тяжелых и легких РЗЭ в качестве экстрагента может быть использован фосфиноксид разнорадикальный.
Литература:
- Толстов А. В. Массив Томтор крупнейший из «редких» //Наука и техника в Якутии. — 2011. — № 2(21). — С. 16–23.
- Сокальский М. А., Сокальская Л. И., Татарников А. В., Утилизация отравляющих веществ и полупродуктов их синтеза: получение на их основе ионообменных материалов для гидрометаллургии. // Рос. хим. ж. (Ж. Рос. хим. об-ва им. Д. И. Менделеева). — 2001. — Т. XLV. — № 5–6. — С. 157–162.
- Костикова Г. В., Кутепова О. А., Резник А. М., Цивадзе А. Ю., Крылов Ю. С., Сальникова Е. В. Экстракция минеральных кислот нейтральными фосфорорганическими соединениями из смешанных нитратно-хлоридных сред // Вестник МИТХТ. — 2013. — T. VIII. — № 6. — С. 88–94.
- Костикова Г. В., Данилов Н. А., Крылов Ю. С., Корпусов Г. В., Сальникова Е. В. Исследование экстракции скандия из различных сред. (Сообщение 1). Экстракция скандия из азотнокислых растворов // Радиохимия. — 2005. — Т. 47. — № 2. — С. 162–166.











