На уроках физики мы говорили о разнообразии веществ, существующих в природе. Сейчас их известно несколько миллионов. Многие из веществ находятся в природе в виде кристаллов. Даже вода в твердом состоянии тоже кристаллична, а снежинки — это основа кристалла воды. Я посмотрел фильм, его основой стала работа японского исследователя Массару Эмото, который более двадцати лет изучает кристаллы воды. Оказалось, что вода, к которой до начала кристаллизации «обратились» со словами «доброта», «любовь», «ангел», «благодарю», образует кристаллы с правильной структурой, симметричной формы, украшенные сложным, красивым орнаментом. Но если воде говорили слова «зло», «ненависть», то кристаллы получались мелкими, уродливыми.

Значение кристаллов в жизни человека огромно. С кристаллическими веществами мы встречаемся на каждом шагу — дома, в школе, на улице. Мы едим кристаллы, например, соль или сахар, мы ходим по кристаллам, и они хрустят под ногами, живем под крышей из кристаллов, лечимся кристаллами. Поэтому изучение кристаллов веществ и способов их получения актуально в наше время.
Цель моей работы — вырастить кристаллы искусственным путем и выявить их особенности.
Согласно этой цели были поставлены следующие задачи:
– ознакомиться с научно-популярной литературой по заданной теме;
– изучить методики о способах искусственного выращивания кристаллов;
– вырастить кристаллы поваренной соли, медного купороса, азотнокислого калия и чистой меди;
– описать результаты наблюдений и сделать выводы;
– закрепить навыки в умении аккуратно обращаться с веществами и правильно организовывать план своей работы.
Предметом моего исследования стали кристаллы поваренной соли, медного купороса, азотнокислого калия и чистой меди.
В научной работе были использованы следующие методы исследования: наблюдение, опыты, сравнительный анализ результатов опытов.
Условия проведения опыта, необходимое оборудование, ход эксперимента и его внешние проявления, а также результаты работы были оформлены в виде журнала наблюдений.
В ходе ознакомления с теоретическими материалами были выдвинуты следующие гипотезы:
Кристаллы поваренной соли, медного купороса, азотнокислого калия и чистой меди можно получить искусственным путем.
Кристаллы различных веществ могут быть различны по цвету, форме, размеру.
Основная часть
Теоретическое обоснование проблемы
Интересно происхождение слова «кристалл» (оно звучит почти одинаково на всех европейских языках). Много веков назад среди вечных снегов в Альпах, на территории современной Швейцарии, нашли очень красивые, совершенно бесцветные кристаллы, очень напоминающие чистый лед. Древние натуралисты так их и назвали — «кристаллос», по-гречески — лед. Это слово происходит от греческого «криос» — холод, мороз.
В XIX веке было установлено, что особенности кристаллов связаны с расположением атомов в пространстве. Законы таких расположений были выведены в 1891 году нашим замечательным соотечественником, родоначальником современной кристаллографии Е. С. Федоровым (1853–1919). Как известно, настоящие природные кристаллы образовывались в течение миллионов лет, в глубине земной коры, при высоких температурах (до 2000 ºС) и под колоссальным давлением 1 . Мест, где складывались такие условия, крайне мало. Этим объясняется ограниченность естественных запасов кристаллических веществ.
Современная промышленность не может обойтись без самых разнообразных кристаллов. Они используются в часах, вычислительных машинах, лазерах и многом другом. Великая лаборатория — природа — уже не может удовлетворить спрос развивающейся техники, и вот на специальных фабриках начинают выращивать искусственные кристаллы.
Существуют различные способы выращивания кристаллов. Часто этот процесс требует высоких температур и огромного давления, но некоторые кристаллы можно выращивать и в домашних условиях.
Основой выращивания кристаллов, как пишет любая литература, является насыщенный раствор соли 2 .
Описание методик выращивания кристаллов (из раствора, где растворитель — вода) можно свести к трем пунктам:
– Выращивание больших кристаллов (длина ребер от 1 см и более) соединений, растворимых в воде.
– Получение кристаллов мало- или нерастворимых соединений в воде.
– Получение кристаллов простых веществ (металлов и неметаллов).
Практическая часть
Опыт 1 (20.01.2020).
Приготовление насыщенных растворов медного купороса, азотнокислого калия, поваренной соли.
Оборудование: три стеклянные банки объемом 500 мл, столовая ложка, фильтрованная бумага, водный термометр.
Исходные вещества: порошок медного купороса, поваренная соль, калий азотнокислый (удобрение), кипяченая вода.
Ход опыта: (для каждого вещества проводится отдельно): в чистую стеклянную баночку наливаем 300 мл горячей кипяченой воды (t +50 ºС), засыпаем вещество небольшими порциями (одна порция — это одна столовая ложка), каждый раз перемешивая и добиваясь полного растворения. Когда раствор «насытился» — вещество стало оставаться на дне — добавляем еще две порции и оставляем раствор при комнатной температуре на сутки. Чтобы в раствор не попадала пыль, накрываем его листом фильтровальной бумаги (салфеткой).
Внешние проявления процесса:
Раствор медного купороса приобрел яркий синий цвет. На получение насыщенного раствора ушло 6 порций вещества.
Раствор поваренной соли стал сначала белым, затем — прозрачным. На получение насыщенного раствора ушло 5 порций вещества.
Выращивание кристаллов стало для меня поистине увлекательным и познавательным занятием. Кроме веществ и оборудования, для проведения работы мне потребовалась тщательная подготовка, аккуратность и наблюдательность. Раствор азотнокислого калия (удобрение) стал прозрачным, чистым. А реакция протекала с поглощением тепла (вода в банке сразу стала холодной). На получение раствора затрачено 7 порций вещества.
Выводы: Взятые вещества при одинаковой температуре, в одинаковом объеме воды растворяются в разных количествах. Реакция растворения азотнокислого калия происходила с поглощением тепла.
Опыт 2 (21.01.2020).
Получение кристалла — «затравки».
«Затравка» — это маленький кристаллик правильной формы, который станет основой для дальнейшего роста кристалла.
Оборудование: кастрюля для водяной бани, три стеклянные банки объемом 500 мл, чайная ложка, фильтровальная бумага, воронка.
Исходные вещества: растворы, полученные в опыте 1.
Ход опыта: (для каждого вещества отдельно): осмотрим полученные растворы, аккуратно сливаем с осадка раствор в новые баночки, туда же добавляем одну чайную ложку чистого вещества. Баночки нагреваем на водяной бане до полного растворения соли. После этого ставим их на рабочий стол и оставляем на сутки остывать.
Внешние проявления процесса: Быстрее всего растворился азотнокислый калий. Окраска медного купороса стала еще интенсивнее. Растворы поваренной соли и азотнокислого калия прозрачные.
Выводы: чем больше температура воды, тем больше вещества в ней можно растворить.
Опыт 3 (22.01.2020).
Отбор кристаллов — «затравок».
Оборудование: три стеклянные банки объемом 500 мл, три футляра для фотопленки с крышкой, стержни от ручки, тонкие нити.
Исходные вещества: растворы, полученные в опыте 2.
Ход опыта: осмотрим содержимое баночек с растворами: раствор медного купороса дал большое количество крупных кристаллов, осевших на дне банки. Кристаллы на дне банки с раствором поваренной соли были очень мелкими, соединялись друг с другом, образуя форму снежинок. Калий азотнокислый дал три крупных кристалла, затем появились мелкие кристаллы. Для получения затравок опускаем в них ниточки на стержнях-перемычках. Азотнокислый калий образовал кристалл с гранью 3 мм на второй день, а поваренная соль — на четвертый день опыта. Отобранные кристаллы — «затравки» откладываем в футляры для фотопленки и плотно закрываем крышкой.
Выводы: у медного купороса кристаллы растут быстрее, чем у поваренной соли и азотнокислого калия, т. е. кристаллы разных веществ растут с разной скоростью.
Опыт 4 (27.01.2020).
Закладка «затравки» для выращивания кристаллов.
Оборудование: пять тонкостенных стаканов, стержни-перемычки, тонкие нитки, фильтрованная бумага.
Исходные вещества: кристаллы — «затравки», насыщенные растворы солей.
Ход опыта: два кристалла медного купороса кладем на дно стакана, заливаем насыщенным раствором, а два кристалла укрепляем на нити и опускаем в насыщенный раствор. Три кристалла калия азотнокислого укрепляем на нитях и с помощью стержня — перемычки погружаем в стакан с насыщенным раствором. То же проделываем с поваренной солью. Следует помнить, что температура насыщенного раствора не должна превышать 30 градусов, иначе кристаллы растворятся. Теперь следует следить за ростом кристаллов каждый день, не сотрясая раствор.
Опыт 5 (28.01.2020).
Получение кристаллов меди.
Оборудование: стакан на 200 мл, фильтрованная бумага, железные скрепки.
Исходные вещества: порошок медного купороса, поваренная соль (твердая и насыщенный раствор).
Ход опыта: в чистый стакан насыпаем очень тонкий слой медного купороса (чтобы он покрывал дно), утрамбовываем. Сверху насыпаем в три раза больше поваренной соли, утрамбовываем. Поверх слоев укладываем круг из фильтровальной бумаги так, чтобы он вплотную соприкасался со стенками стакана. На фильтр высыпаем железные скрепки. Медленно, тонкой струйкой заливаем вещества насыщенным раствором поваренной соли.


Внешние проявления: слои солей окрасились в зеленый цвет
Выводы :
– (30.01.2020) начались химические процессы.
Внешние проявления: зеленая окраска дошла до фильтра, в слое поваренной соли появились розовые нити.
– (04.02.2020) началось образование кристаллов меди.
– Достаем кристаллы из растворов.
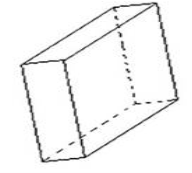
Кристалл медного купороса представляет собой призму, в сечении которой лежит ромб. Кристаллы синего цвета, прозрачные, с длиной грани 1 см.

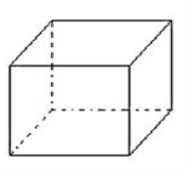
Кристалл поваренной соли и азотнокислого калия — куб. Кристалл прозрачный, бесцветный. Длина грани — 5 мм

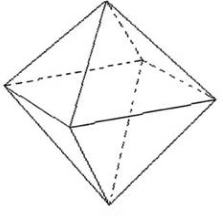
Кристаллы меди имеют форму октаэдров, похожи на острые иголочки, ярко-розового цвета, мелкие, с различной длиной грани.

Литература:
- Я познаю мир: Драгоценные камни и минералы: Дет. Энцикл./Н.Орлова; Худож. А.Разванова. — М.: ООО «Издательство АСТ», 2003. — С. 365
- Опыты без взрывов/ Ольгин О. — М.: «Химия», 1995. — С. 74










