В статье автор представляет результаты сравнения действия ипилимумаба, пембролизумаба и ниволумаба в лечении метастатической меланомы кожи.
Ключевые слова: меланома кожи, моноклональные антитела, иммунотерапия/
Меланома кожи — это злокачественная опухоль, возникающая из меланоцитов. Это один из самых серьезных видов рака, устойчивый к большинству методов лечения, поэтому сообщество ученых и медиков озабочены поиском наиболее эффективного препарата.
В прошлой работе я сравнила 3 основных метода лечения меланомы (хирургический, лучевая терапия, лекарственная терапия) и пришла к выводу, что наиболее перспективным является иммунотерапия. Ее главное преимущество — меньшее количество побочных эффектов, т. к. она активирует иммунитет человека для борьбы с онкологией, за счет иммунной памяти предотвращает частые рецидивы опухоли. [1].
Сегодня перспективное направление в иммунотерапии — применение препаратов на основе моноклональных антител, т. к. они специфичны и имеют высокую активность. Основными препаратами являются ипилимумаб, пембролизумаб и ниволумаб, но в исследованиях сравниваются 2 из них между собой, но не все 3 сразу и выводы о большей эффективности того или иного препарата противоречивы. [2,3,4].
Гипотеза: Сравнив приводимые в различных научных исследованиях действия препаратов по разным показателям (общая выживаемость, выживаемость без прогрессирования, их медиана, частота ответов), можно выявить наиболее эффективные препараты.
Цель работы: Сравнение действия на основе данных современных научных исследований и выявление наиболее эффективных препаратов на основе моноклональных антител в монотерапии меланомы кожи.
Моноклональные антитела в лечении меланомы кожи
Иммунотерапия — лечение онкологического больного с использованием лекарственных препаратов, обладающих способностью корректировать иммунитет.
Одной из наиболее успешных стратегий иммунотерапии является использование моноклональных антител (МКА). Особое место среди них занимают ингибиторы блокаторов иммунного ответа, которые селективно связываются с рецепторами PD-1 и CTLA-4 на поверхности иммунокомпетентных клеток. Эти рецепторы являются представителями системы иммунологических контрольных точек, предотвращающими запуск аутоиммунных процессов. Путь CTLA-4 можно заблокировать с помощью гуманизированного МКА ипилимумаба, путь PD-1–PD-L1 — с помощью пембролизумаба и ниволумаба. [1,4,5].
Мною было изучено и проанализировано более 30 рандомизированных контролируемых исследований применения ипилимумаба, пембролизумаба и ниволумаба зарубежных авторов. На основе данных, представленных в исследованиях, была составлена сравнительная таблица эффективности данных препаратов (см Приложение 1). За основу были взяты следующие критерии эффективности: побочные эффекты, общая выживаемость, медиана общей выживаемости, выживаемость без прогрессирования, медиана выживаемости без прогрессирования, 6-ти, 12-ти, 24-х месячная выживаемость, частота объективного и полного ответа.
Выводы
- Ипилимумаб в дозе 10 мг/кг вызывает больше побочных эффектов, чем ипилимумаб в дозе 3 мг/кг, при этом медиана выживаемости больше на 6,7 месяцев, частота объективного ответа больше на 5 %, 12-ти месячная выживаемость больше на 4,7 %. По остальным показателям (частота полного ответа, медиана выживаемости без прогрессирования) значение отличается меньше, чем на 2 %, нет данных о общей выживаемости, выживаемости без прогрессирования, 6-ти месячной выживаемости и 2-х летней выживаемости при применении ипилимумаба в дозе 10 мг/кг. Из имеющихся данных можно сделать вывод, что при применении ипилимумаба может быть выражен дозозависимый эффект, что требует дальнейшего изучения и подтверждения.
- Ипилимумаб уступает пембролизумабу и ниволумабу по всем показателям (вызывает больше побочных эффектов 3–4 степени тяжести, общая выживаемость и ее медиана, выживаемость без прогрессирования и ее медиана, 6-ти и 12-ти месячная выживаемость частота объективного и полного ответа меньше, чем у ингибиторов сигнала PD1-PDL1 — ниволумаба и пембролизумаба), следовательно, можно сказать, что ингибиторы PD1 являются более эффективны при лечении метастатической меланомы кожи.
- Пембролизумаб превосходит ниволумаб по медиане выживаемости без прогрессирования, частоте объективного ответа, полного ответа, 12-ти месячной выживаемости. Частота 2-х летней выживаемости пембролизумаба и ниволумаба практически одинаковая, медиана выживаемости на 2 месяца больше у ниволумаба, чем у пембролизумаба.
Поскольку нет сведений общей, 6-ти месячной выживаемости и выживаемости без прогрессирования, нельзя сделать однозначный вывод, какой из анти PD1 препаратов эффективнее, но исходя из имеющихся данных — пембролизумаб может быть эффективнее.
- Полноценно сравнить пембролизумаб и ниволумаб не удается из-за отсутствия нужных данных в исследованиях. Из этого можно сделать вывод о необходимости стандартизации критериев оценки эффективности препарата.
- Моя гипотеза частично подтвердилась. Сравнив приводимые в различных научных исследованиях действия по приведенным выше показателям, можно сказать, что ингибиторы PD1 являются более эффективными, чем ингибитор CTLA4. При этом нельзя с точностью выявить наиболее эффективный препарат среди ингибиторов PD1 из-за отсутствия определенных сведений.
Приложение 1
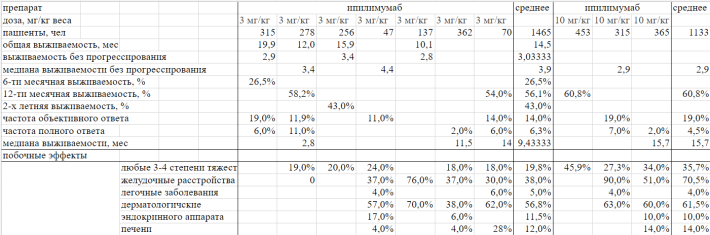
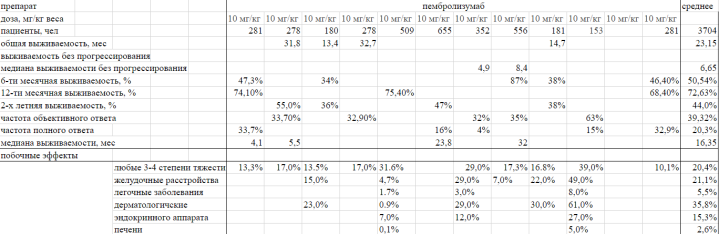
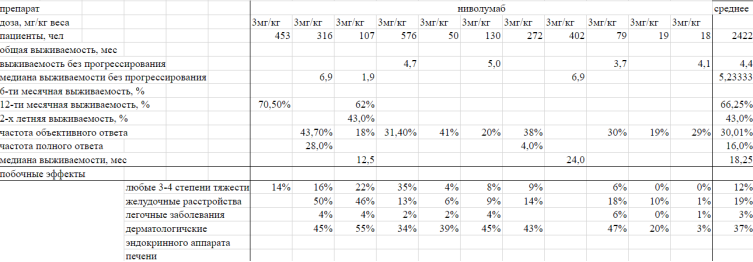
Литература:
- Ивашкина М. Д. Методы лечения меланомы кожи//Юный ученый. — 2020.- № 4 (34) С.90–95
- Adedayo A. Onitilo, Jaimie A. Wittig Principles of Immunotherapy in Melanoma //Surg Clin North Am. — 2020.- № 100(1) С.161–173., англ.
- Franklin C., E. Livingstone, A. Roesch Immunotherapy in melanoma: Recent advances and future directions// EJSO — 2017.-№ 43 С. 604–611., англ.
- Optionen bei Melanomen im Stadium III: Die richtige Entscheidung treffen// AIM at Melanoma Foundation and Terranova Medica — 2019 [Электронный ресурс] — Режим доступа:http://aimwithimmunotherapy.org/wpcontent/uploads/2019/11/Stage3MelanomaDiagnosis_Germany_Final.pdf, нем.
- Robert B. Neue Ansätze in der Therapie von Hauttumoren// Im Fokus Onkologie. -2019.- № 22, С. 43, нем.
- Ascierto PA, Del Vecchio M, Robert C, et al. Ipilimumab 10 mg/kg versus ipilimumab 3 mg/kg in patients with unresectable or metastatic melanoma: a randomised, double-blind, multicentre, phase 3 trial// Lancet Oncol. — 2017. -№ 18(5). -С.611–622., англ.
- Caroline Robert, Antoni Ribas, Omid Hamid, et a. Durable Complete Response After Discontinuation of Pembrolizumab in Patients With Metastatic Melanoma// Journal of Clinical Oncology. — 2018. — № 36 (17). — С. 1668–1674., англ.
- Deeks E. D. Pembrolizumab: A Review in Advanced Melanoma. // Drugs. — 2016. — № 76(3). — С. 375–386., англ.
- Eggermont, A., Blank, C. U., Mandala, M., et a. Adjuvant Pembrolizumab versus Placebo in Resected Stage III Melanoma. The New England journal of medicine. — 2018. — № 378(19). — С. 1789–1801., англ.
- Hodi FS, O'Day SJ, McDermott DF, et al. Improved survival with ipilimumab in patients with metastatic melanoma. //N Engl J Med. — 2010. № 19;363. — С. 711–23., англ.
- James Larkin, M.D., Ph.D., Vanna Chiarion-Sileni, M.D., et al. Combined Nivolumab and Ipilimumab or Monotherapy in Untreated Melanoma// N Eng J Med. — 2015. — № 373. — С.23–34., англ.
- Jeffrey S Weber, Geoff Gibney, Ryan J Sullivan, et al. Sequential administration of nivolumab and ipilimumab with a planned switch in patients with advanced melanoma (CheckMate 064): an open-label, randomised, phase 2 trial//The Lancet Oncology. — 2016. — № 17. — С. 943–955., англ.
- Larkin J, Chiarion-Sileni V, Gonzalez R, et al. Five-Year Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma//N Engl J Med. -2019/ — № 17. — С.1535–1546., англ.
- Long G. V., Atkinson V., Cebon S., et al. Standard-dose pembrolizumab in combination with reduced-dose ipilimumab for patients with advanced melanoma (KEYNOTE-029): an open-label, phase 1b trial//The Lancet Oncology. — 2017. — № 18(9). — С. 1202–1210., англ.
- Michael A. Postow, M.D., Jason Chesney, M.D., et al. Nivolumab and Ipilimumab versus Ipilimumab in Untreated Melanoma// The New England journal of medicine. — 2015. № 372. С. 2006–2017., англ.
- Moser, J. C., Wei, G., Colonna, S. V., et al. Comparative-effectiveness of pembrolizumab vs. nivolumab for patients with metastatic melanoma. //Acta oncologica (Stockholm, Sweden). 2020. — № 59(4). — С. 434–437., англ.
- Ribas, A., Puzanov, I., Dummer, R., et al. Pembrolizumab versus investigator-choice chemotherapy for ipilimumab-refractory melanoma (KEYNOTE-002): a randomised, controlled, phase 2 trial. //The Lancet. Oncology. — 2019. — № 16(8). — С. 908–918., англ.
- Robert C, Ribas A, Schachter J, Arance A, et al. Pembrolizumab versus ipilimumab in advanced melanoma (KEYNOTE-006): post-hoc 5-year results from an open-label, multicentre, randomised, controlled, phase 3 study//Lancet Oncol. — 2019. № 20(9). — С. 1239–1251., англ.
- Schachter, J., Ribas, A., Long, G. V., et a. Pembrolizumab versus ipilimumab for advanced melanoma: final overall survival results of a multicentre, randomised, open-label phase 3 study (KEYNOTE-006).// Lancet (London, England). — 2017. — № 390(10105). — С. 1853–1862., англ.
- Topalian, S. L., Sznol, M., McDermott, D. F., et al. Survival, durable tumor remission, and long-term safety in patients with advanced melanoma receiving nivolumab. // Journal of clinical oncology: official journal of the American Society of Clinical Oncology. — 2014. — № 32(10). — С. 1020–1030., англ.
- Weber, J. S., D'Angelo, S. P., Minor, D., Nivolumab versus chemotherapy in patients with advanced melanoma who progressed after anti-CTLA-4 treatment (CheckMate 037): a randomised, controlled, open-label, phase 3 trial.// The Lancet. Oncology. — 2015. — № 16(4). — С. 375–384., англ.







