В статье приведены сведения о биологических и фармакологических эффектах флавоноидов. Показаны антиоксидантные и другие стороны биологической активности изучаемых веществ. Апробированы методики качественного и количественного определения их содержания в экстрактах из растительного сырья. Проведенное исследование позволило определить наиболее эффективный способ выделения флавоноидов.
Ключевые слова: флавоноиды, растительное сырье, качественнее и количественное определение, спектрофотометрия.
Здоровый образ жизни с каждым годом становится все более популярным. Все больше людей стараются поддерживать себя в форме, заниматься спортом и, самое главное, правильно питаться, отказываясь от вредных продуктов и заменяя их на здоровую, «живую», как ее называют, еду. Внимание многих исследователей постоянно привлекает растительное сырье, содержащее фенольные соединения, и, в первую очередь, флавоноиды. Интерес ученых различных специальностей к исследованию флавоноидов вызван многообразием биологических и фармакологических эффектов, которые эти соединения проявляют в организме человека и животных. Однако наибольшее внимание относительно действия флавоноидов на организм человека связано с их мощной антиоксидантной активностью [2, 3].
Флавоноиды — группа полифенольных соединений С 6 –С 3 –С 6 -ряда, которые синтезируются исключительно в высших растениях и обладают широким спектром действия на организм человека [1].
Многие гипотезы и экспериментальные данные о положительном влиянии флавоноидов на здоровье человека, включая действие на сердечно-сосудистую систему, а также наличие антиканцерогенной активности, основаны на их антиоксидантных свойствах [1,3].
Флавоноиды широко распространены в растительном мире. Ими богаты высшие растения, относящиеся к различным семействам и родам.
В некоторых литературных источниках есть сведения о том, что в проростках различных растений содержится большое количество флавоноидов [1,2]. Однако нигде не указываются конкретные величины, а результаты различаются в десятки раз.
Данные природные вещества являются эссенциальными для организма, требующими постоянного поступления с растительной пищей или в виде лекарств и пищевых добавок [4]. Поиск новых возможностей для расширения круга доступных биоактивных соединений, способных защитить организм и геном человека от агрессии многочисленных свободных радикалов, должен являться приоритетной задачей прикладных исследований.
Целью данного исследования является разработка эффективного способа выделения флавоноидов из проростков и их качественное и количественное определение.
В качестве объектов исследования была выбрана микрозелень — броколли, мицуна, кольраби, горчицы.
Поскольку для флавоноидов не существует универсального способа выделения из растительного сырья. В каждом конкретном случае прибегают к наиболее подходящему методу или сочетанию методов. При этом необходимо учитывать, как свойства веществ, так и особенности растительного сырья. В связи с этим мы пристальное внимание уделили приготовлению экстрактов. Нами были проанализированы различные литературные источники по проведению экстрагирования. В ходе работы обращали внимание на вид экстрагента, его концентрацию, массовое соотношение сырье/экстрагент, степень измельчения сырья, время экстракции. При этом основным показателем эффективности метода являлось содержание суммы флавоноидов в экстракте в пересчете на рутин [4].
Нами были испытаны два способа экстракции:
- Ступенчатая трехкратная экстракция с нагреванием;
- Однократная экстракция при комнатной температуре (настаивание).
Для качественного определения использовали цианидовые пробы (проба Чинода — Chinoda, химизм которой состоит в восстановлении флавоноидов атомарным водородом в кислой среде в присутствии магния или цинка).
Реакция основана на способности окисленных форм флавоноидов восстанавливаться водородом в момент выделения до антоцианидинов. В кислой среде образуются оксониевые соли, окраска которых зависит от структуры флавоноида. Флавоны дают оранжево-красные, флавонолы от розовой до малиновой окраски соли. Флавоноиды при восстановлении магнием или цинком в присутствии концентрированной хлористоводородной кислоты образуют красное окрашивание, обусловливаемое образованием антоцианидинов.
Реакция очень чувствительна и основана на восстановлении карбонильной группы и образовании антоцианида. В ходе реакции происходит восстановление водородом карбонилапиронового кольца и образование антоцианидинов, окрашивающихся в кислой среде от оранжевого до малиново-красного цвета [3,4].
Определение эффективного метода выделения флавоноидов
На основании анализа литературных данных и проведнных исследований были выбраны следующие особенности методов экстракции флавоноидов из растительного сырья (табл. 1).
Таблица 1
Условия проведения экстрагирования биологически активных веществ из растительного сырья
|
Кратность экстрагирования |
Степень измельчения сырья |
Вид экстрагента |
Концентрация экстрагента |
Соотношение сырье/ экстрагент |
Время реакции |
|
3 |
0,1 мм |
Водный раствор этанола |
95 % |
1:30 |
24 ч |
К спиртовому извлечению из сырья добавляют несколько капель концентрированный хлористоводородной кислоты и 20–30 мг порошка магния или цинка. При наличии флавоноловых веществ наступает окрашивание. Реакцию дают флавоны, флавонолы и флаваноны.
Для количественного определения флавоноидов использовали наиболее распространенный спектрофотометрический метод анализа, основанный на реакции комплексообразования флавоноидов с хлоридом алюминия. Метод достаточно прост в исполнении, является высокочувствительным и относительно недорогим, что делает его предпочтительным для использования в контрольно-аналитических лабораториях. Использование такого метода позволяет определить сумму флавоноидов в присутствии других полифенольных соединений, не образующих комплекса с хлоридом алюминия в среде 30–96 % спирта. Измерение оптической плотности проводили на спектрофотометре УФ-1200 в кюветах с толщиной слоя 10 мм.
Количественное определение флавоноидов
К 60 мкл этанольного экстракта в пробирку поочередно добавлять: 60 мкл 96 %-ного этанола; 120 мкл 2 %-ного спиртового раствора хлористого алюминия (AlCl 3 ); 1,26 мл 96 %-ного этанола.
Выдерживали 30 мин. Для определения содержания флавоноидов использовали спектрофотометр 1200 (поглощение при 415 нм).
Раствор сравнения — 60 мкл экстракта; 60 мкл 96 %-ного этанола; 120 мкл дистиллированной воды; 10 мкл ледяной уксусной кислоты; 1,25 мл 96 %-ного этанола.
Содержание флавоноидов рассчитывали по формуле:
С = (А 415 *k*P*Vэ) / (1000*m),
где: С — содержание флавоноидов, мг/г сухой массы; А 415 — оптическая плотность при длине волны 415 нм; k — пересчетный коэффициент (по рутину); P — разведение; Vэ — объем раствора, мл; m — масса навески, г.
Калибровочные кривые строили по рутину.
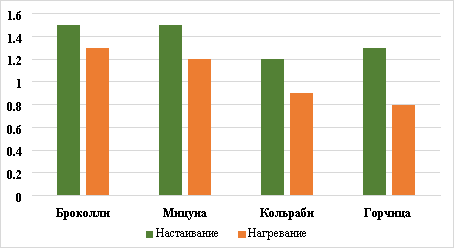
Рис. 1 Эффективность извлечения флавоноидов при разных способах экстракции
Представленные данные (рис. 1) позволяют сделать вывод о том, что во всех исследованных образцах эффективность экстракции была выше при настаивании. Это позволило определить наиболее эффективный способ выделения флавоноидов из растительного сырья.
Литература:
- Абдрасилов Б. С., Ким Ю. А., Музафаров Е. Н., Тараховский Ю. С. Флавоноиды: биохимия, биофизика, медицина. [отв. ред. Е. И. Маевский] — Пущино: Sуnchrobook, 2013. — 310 c.
- Гарифзянов А. Р., Жуков Н. Н., Иванищев В. В. Образование и физиологические реакции активных форм кислорода в клетках растений/ А. Р. Гарифзянов, Н. Н. Жуков, В. В. Иванищев // Современные проблемы науки и образования. — 2011. — № 2. 21с.; URL: www.science-education.ru/96–4600 (дата обращения: 02.09.2011).
- Левецкий А. П., Макаренко О. А. Физиологические функции флавоноидов в растениях культурных растений. / А. П. Левецкий, О. А. Макаренко // Физиология и биохимия культурных растений. — 2013. — Т. 45, № 2. — С. 100–112.
- Ломбоева С. С., Танхаева Л. М., Оленников Д. Н. Методика количественного определения суммарного содержания флавоноидов в надземной части ортилии однобокой / С. С. Ломбоева, Л. М. Танхаева, Д. Н. Оленников // Химия растит. сырья. — 2008. — № 2. — C. 65–68.











