Введение
Перед этим исследованием был проведен эксперимент, показывающий, что личинки ручейников могут иметь предпочтения в цвете при выборе грунта для домиков. [1] Один из способов проверить, обусловлено ли это генетически — измерить «важность» генов, отвечающих за восприятие разных цветов.
Опсины, участвующие в восприятии света, отражают эволюционные адаптации Trichoptera к двойной среде обитания: водной на стадии личинки и наземной во взрослом состоянии [2]. Их чувствительность к разным длинам волн может быть связана с экологическими условиями и адаптациями к освещённости [3, 4].
Это исследование направлено на оценку степени консервативности генов опсинов у ручейников как показателя их функциональной важности. Для этого были построены филогенетические деревья на основе опсинов, с использованием метода максимального правдоподобия (Maximum Likelihood), и проведено их сравнение с референтным деревом, основанным на последовательностях гистона H3. [5, 6] Чем ближе дерево опсинов к референтному дереву, тем выше предполагаемая степень консервации соответствующих опсинов.
Исследование имеет как фундаментальное, так и прикладное значение. Во-первых, знание спектральной чувствительности ручейников может способствовать минимизированию влияния антропогенного освещения. [7, 8] Во-вторых, предпочтения этих насекомых к определённым длинам волн могут быть полезны при создании ювелирных изделий с использованием их коконов. [9] В-третьих, ручейники — чувствительные биоиндикаторы качества воды. [10, 11]
Литературный обзор
Ручейники
Ручейники ( Trichoptera ) — отряд насекомых с полным превращением. На личиночной стадии они обитают в воде, а во взрослом состоянии — на суше [2, 11]. Такая смена среды обитания обусловила разнообразие опсинов и зрительных адаптаций. Trichoptera делятся на два подотряда: Integripalpia и Annulipalpia . Integripalpia защитные футляры, тогда как Annulipalpia использовались в исследовании в качестве внешней группы при построении деревьев [2].
Зрение насекомых
У насекомых имеется несколько органов зрения. У взрослых особей обычно развиты два типа глаз: фасеточные глаза (сложные) и простые глазки (оцеллии). Фасеточные глаза способны воспринимать свет в различных спектральных диапазонах, а также детектировать поляризацию, в то время как глазки, как правило, отвечают только за определение уровня освещенности. [3, 4]
У личинок имеются примитивные глазные структуры, стемматы (предшественники фасеточных глаз) однако их способность различать цвет ограничена. [4]
Филогения
Филогенетика изучает эволюционные взаимоотношения между организмами. Филогенетические деревья отражают дивергенцию видов и позволяют проследить генетические изменения, лежащие в основе видового разнообразия.
Такие деревья могут строиться на основе различных генов, в зависимости от целей анализа. Для изучения глубоких эволюционных связей обычно используются консервативные гены — например, гены рибосомной РНК (16S у прокариот, 18S у эукариот), гистоны или митохондриальные гены. [5]
Однако для исследования адаптаций к определённым экологическим факторам (например, к зрению) могут использоваться гены функционального значения, такие как опсины. [4]
Гистоны H3
Гистон H3 — это компонент нуклеосомы, структурной единицы хроматина в клетках эукариот. Он играет ключевую роль в упаковке ДНК и регуляции экспрессии генов. Благодаря своей функции в обеспечении структуры и стабильности генома, H3 демонстрирует высокий уровень консервативности на протяжении эволюции. [6]
В филогенетических исследованиях гистоны, включая H3, широко применяются в качестве молекулярных маркеров благодаря стабильности их последовательностей у различных видов. В данном исследовании филогенетические деревья, построенные на основе генов H3, рассматриваются как референтные, и сравниваются с деревьями, полученными на основе опсинов. [6]
Опсины и их биологическая функция
Опсины — это светочувствительные рецепторы, относящиеся к семейству G-белков-связанных рецепторов (GPCR). Они позволяют фоторецепторным клеткам преобразовывать световые сигналы в электрические импульсы, обеспечивая визуальное восприятие.
Этот процесс, называемый фототрансдукцией, лежит в основе способности организмов реагировать на световые стимулы. [3, 4]
Опсины делятся на несколько классов, включая опсины, чувствительные к коротковолновому (SW) и длинноволновому (LW) свету. В данной статье были рассмотрены несколько видов длинноволновых опсинов, ранее определенных в других исследованиях. [14] Каждый тип адаптирован к определённому диапазону длин волн, что может отражать экологические и поведенческие адаптации. [3, 4, 2]
Значение консервации опсинов
Оценка степени консервации генов опсинов среди различных видов позволяет судить об их функциональной значимости. Высококонсервативные участки указывают на эволюционные ограничения, связанные с необходимостью сохранения зрительной функции. [4]
Анализ этих закономерностей у Trichoptera может выявить селективное давление, оказавшее влияние на развитие зрительных адаптаций в водной и наземной среде, и подчеркнуть роль опсинов как ключевых молекул, определяющих светочувствительность. [2]
Предыдущие исследования
Было показано, что искусственное освещение, особенно в синем и поляризованном диапазоне, привлекает водных насекомых, формируя «эволюционные ловушки» [7, 8]. Недавние геномные исследования выявили значительное разнообразие длинноволновых (LW) опсинов и частое отсутствие коротковолновых (SW) у Trichoptera, что может быть связано с адаптацией к условиям низкой освещённости. Это подчёркивает связь между опсинным репертуаром и спектральной средой обитания [2, 12].
Методология
Для оценки степени консервации опсинов у Trichoptera были построены филогенетические деревья с использованием метода максимального правдоподобия (Maximum Likelihood, IQ-TREE) и сравнены с референтным деревом, основанным на гене гистона H3 — высококонсервативном элементе, широко применяемом в филогенетических исследованиях. [5, 13, 6] Предполагалось, что деревья, основанные на коротковолновых (SW) опсинах, будут ближе к референтному, чем деревья на основе длинноволновых (LW) опсинов, поскольку SW-опсины более широко распространены среди насекомых и, возможно, менее изменчивы. [3, 2, 14]
Для поиска гомологов генов опсина в неаннотированных геномах Trichoptera использовался tBLASTn, поскольку он позволяет сравнивать белковые последовательности с нуклеотидными базами данных. Геномные последовательности были получены из NCBI GenBank, как наиболее полная база по Trichoptera . [3] Референтные опсины — из OrthoDB, на основе подхода Guignard et al. (2022). Однако из-за ограниченности аннотаций у многих видов и вариативности опсинов, область анализа была ограничена видами с идентифицируемыми гомологами. [14]
Предсказание границ генов выполнялось в AUGUSTUS, используя модель Heliconius melpomene (Lepidoptera), как ближайшего аннотированного родственника. Хотя это не исключает возможных ошибок аннотации, альтернативные инструменты, такие как GeneMark и Glimmer, были менее подходящими из-за ориентации на прокариоты или потребности в аннотированных геномах. [14]
Выравнивание последовательностей выполнялось с помощью MAFFT — быстрого и точного инструмента, особенно эффективного при обработке большого числа последовательностей. [15] Другие программы, такие как MUSCLE или Clustal Omega, уступали в скорости и точности при работе с длинными и разнородными последовательностями. [16]
Построение филогенетических деревьев осуществлялось с использованием IQ-TREE, который обеспечивает высокую точность при разумных вычислительных затратах. [13] Метод Байесовского вывода (MrBayes) был отклонён из-за слишком высокой ресурсоёмкости. [5] Для сравнения деревьев использовались три подхода:
— евклидово расстояние (учитывает различия в длинах ветвей),
— расстояние Робинсона-Фоулдса (оценка различий в топологии),
— сравнение кладов (идентификация общих эволюционных узлов). [17]
Комбинированное использование этих метрик позволяет избежать искажения результатов, свойственного каждой из них по отдельности. Инструменты для их расчёта были интегрированы в онлайн-средства визуализации деревьев, что обеспечило удобство анализа.
Процедура:
- Выбор и подготовка последовательностей
Аминокислотные последовательности опсинов (типов SW, LW2a и LW2b) для Trichoptera были отобраны из опубликованных данных [14] и объединены для дальнейшего анализа. В качестве референса использовалась последовательность гистона H3, полученная из UniProt.
- Получение геномных данных
Геномы нескольких видов Trichoptera из семейства Limnephilidae были загружены из NCBI. Они использовались в качестве целевых геномов для поиска гомологов опсинов и гистона.
- Поиск гомологов и извлечение последовательностей
С помощью tBLASTn были найдены участки генома, соответствующие предполагаемым опсинам и гистону. На основе координат выравнивания были извлечены нуклеотидные последовательности, включая прилегающие регионы.
- Аннотация и проверка генов
Предсказание границ генов проводилось с использованием AUGUSTUS. Принадлежность полученных белков к семейству опсинов подтверждалась с помощью BLASTp, анализа доменов (InterPro) и структурного моделирования (AlphaFold2).
- Выравнивание и построение деревьев
Последовательности выравнивались с помощью MAFFT, после чего были построены филогенетические деревья методом максимального правдоподобия (IQ-TREE). В качестве внешней группы использовались представители подотряда Annulipalpia .
- Сравнение деревьев
Деревья, построенные по опсинам, сравнивались с деревом на основе гистона H3 для оценки степени их топологического сходства и, соответственно, уровня консервации опсинов. Для сравнения использовался интерфейс phylo.io
Визуализация
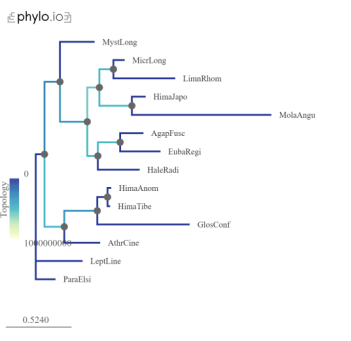
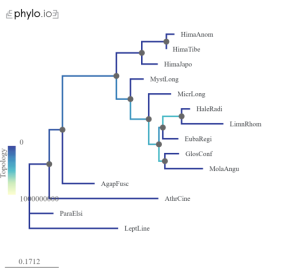
Рис. 1. Филогенетические деревья, основанные на гистонах H3 (референтное дерево). Виды, принадлежащие к подотряду Annulipalpia, были отмечены как внешняя группа. Цвета ветвей указывают на степень сохранности
|
|
|
||
|
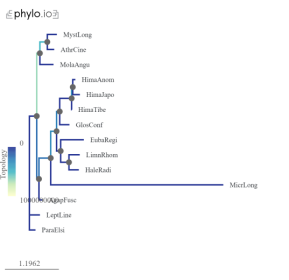
Рис. 2а. Филогенетическое дерево на основе SW-опсина |
Рис. 2б. Филогенетическое дерево на основе опсина LW2a |
||
|
|
|
||
|
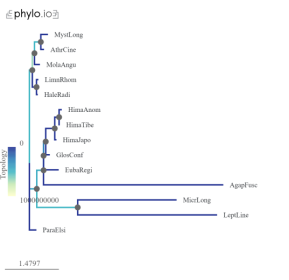
Рис. 2c. Филогенетическое дерево на основе опсина LW2b.1 |
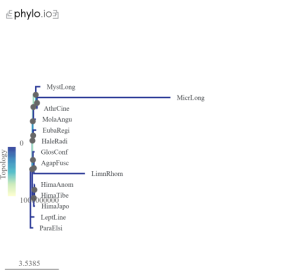
Рис. 2d. Филогенетическое дерево на основе опсина LW2b.2 |
||
Рис. 2. Виды, принадлежащие к подотряду Annulipalpia, были отмечены как внешняя группа. Цвета отражают уровень сходства ветвей с референтным деревом, более светлый цвет указывает на более низкое сходство
При визуальном сравнении деревьев на рис. 2 видно, что веток более светлого цвета больше в деревьях LWa и LWb.1. Кроме того, имеются значительные выбросы, особенно у вида Mystacides longicornis . Это может указывать на проблемы с идентификацией и изоляцией генов опсинов.
Результаты
Таблица 1
Результаты сравнения опсинов и деревьев H3
|
Степень сходства, условные единицы |
||||
|
Тип опсина |
Робинсон-Фоулдс |
Клад |
Поддержка клады |
Евклидово расстояние |
|
ЮЗ |
17,00 |
19,00 |
25 % |
4,90 |
|
LW2a |
15,00 |
17,00 |
33 % |
13,62 |
|
LW2b.1 |
13,00 |
15,00 |
42 % |
6,64 |
|
LW2b.2 |
15,00 |
17,00 |
33 % |
12,92 |
Интерпретация результатов:
Степень топологического сходства между филогенетическими деревьями оценивалась с использованием нескольких метрик, включая расстояние Робинсона-Фоулдса (RF), евклидово расстояние и процент совпадения клад.
Расстояние Робинсона-Фоулдса (RF) измеряет количество двухразделений (bipartitions), отличающихся между двумя деревьями. Чем выше RF, тем больше различий в структуре деревьев. Однако важно учитывать, что эта метрика склонна переоценивать различия, особенно при незначительных перестройках. Поэтому значения RF в пределах 17–19 не могут однозначно интерпретироваться как свидетельство сильного несходства. [17]
Евклидово расстояние отражает различия в длинах ветвей, тогда как сходство клад характеризует степень совпадения эволюционных группировок. Во всех случаях большие значения метрик указывают на большее различие между деревьями. [4]
— SW-дерево продемонстрировало низкое сходство клад и умеренное евклидово расстояние, что указывает на слабое соответствие как по структуре, так и по длинам ветвей.
— LW2a.1 характеризуется умеренным совпадением клад, но высоким евклидовым расстоянием — вероятно, структура дерева частично совпадает с референтной, но длины ветвей существенно различаются.
— LW2b.1 продемонстрировало наивысшее сходство клад и умеренное евклидово расстояние, что свидетельствует о хорошем структурном соответствии и сопоставимых ветвях.
— LW2b.2 показало умеренное сходство клад при высоком евклидовом расстоянии, что предполагает частичное топологическое совпадение при значительных различиях по длине ветвей.
Таким образом, LW2b.1 оказалось наиболее близким к референтному дереву на основе гистона H3 как по структуре (42 % совпадения клад), так и по длине ветвей (евклидово расстояние 6,61). Напротив, деревья SW и LW2b.2 продемонстрировали наименьшее соответствие по всем показателям.
Обсуждение
Полученные результаты частично подтвердили гипотезу о высокой консервации коротковолновых (SW) опсинов у Trichoptera . SW-опсины показали наименьшее евклидово расстояние, но топологическое сходство у LW2b.1 было выше, означая большую консервативность LW2b.1.
Ранее было показано, что SW-опсины отсутствуют у половины исследованных видов Trichoptera , что, вероятно, отражает адаптацию к условиям низкой освещенности, при этом сохраняя коротковолновый диапазон за счет UV-опсинов [2, 4]. Одна из возможных причин высокой консервации LW2b.1 — это селективное давление, связанное с проникновением длинноволнового света в водную среду. [4, 12]. Также возможен эффект функциональной избыточности, при котором LW2b.1 может компенсировать функции других [3].
Методологические ограничения включают отсутствие аннотированных геномов, возможные ошибки в идентификации генов и использование одного референтного вида. Тем не менее, применение нескольких метрик (RF, евклидово расстояние, совпадение клад) и валидация белков с помощью BLASTp и AlphaFold2 повышают надёжность полученных результатов. [3, 13]
Выводы
Опсины LW2b.1 продемонстрировали наиболее высокую степень топологического сходства с референтным деревом и могут играть важную функциональную роль у Trichoptera . Консервация опсинов, по-видимому, определяется не только длиной волны, но и условиями среды, функциональной избыточностью и структурными ограничениями.
Ограничения исследования, включая отсутствие аннотированных геномов, возможные ошибки в определении границ генов и ограниченность референтных последовательностей, могут влиять на точность выводов. Будущие исследования должны включать расширение выборки видов, экспериментальное подтверждение функций опсинов LW2b.1 и улучшение качества аннотации геномов Trichoptera с помощью секвенирования или ПЦР.
Литература:
- Трифонова Е. С. Изучение восприятия цвета личинками ручейников на примере выбора грунта для построения «домиков» (поселок Буково Карачаево-Черкесской Республики) // Юный учёный. — 2025. — № 4 (89). — Апрель.
- Frandsen P. B., Walden K. K. O., Espeland M., Pauls S. U., Zhou X., Meusemann K., Misof B., Kohli M. K. Evolution of Opsin Genes in Caddisflies (Insecta: Trichoptera) // Genome Biology and Evolution. 2024. Vol. 16, № 9. Article evae185.
- Akihisa T. Functional Properties of Opsins and their Contribution to Light-Sensing // Zoological Science. 2014. Vol. 31, № 10. P. 653–662. DOI: https://doi.org/10.2108/zs140094
- Emeis J. J., Morizumi T., Dartnall H. J. A. Evolution of Opsins and Phototransduction // Nature Reviews Molecular Cell Biology. 2009. Vol. 10, № 2. P. 1–12. DOI: https://doi.org/10.1038/nrm2781
- Felsenstein J. Inferring Phylogenies. Sunderland, MA: Sinauer Associates Inc., 2004.
- Szenker E. The Double Face of the Histone Variant H3.3 // Cell Research. 2011. Vol. 21, № 1. P. 421–434. DOI: https://doi.org/10.1038/cr.2011.14
- Gaston K. J., Bennie J., Davies T. W., Hopkins J. Reducing the Ecological Consequences of Night-Time Light Pollution: Options and Developments // Journal of Applied Ecology. 2018. Vol. 55, № 6. P. 309–319. DOI: https://doi.org/10.1111/1365–2664.13145
- Harrison T. A., Perkins S. L., Smithson M. D. Effects of LED Wavelengths on Insect Communities and Resource Flux between Aquatic and Terrestrial Ecosystems // Ecological Applications. 2023. Vol. 33, № 1. Article e02567. DOI: https://doi.org/10.1002/eap.2567
- Benke A. C., Wallace J. B. Trophic Basis of Production among Riverine Caddisflies: Implications for Food Web Analysis // Ecology. 1997. Vol. 78, № 4. P. 1132–1145.
- Thamsenanupap P., Seetapan K., Prommi T. Caddisflies (Trichoptera, Insecta) as Bioindicator of Water Quality Assessment in a Small Stream in Northern Thailand // Sains Malaysiana. 2021. Vol. 50, № 3. P. 655–665. DOI: http://dx.doi.org/10.17576/jsm-2021–5003–08
- Mackay R. J., Wiggins G. B. Ecological Diversity in Trichoptera // Annual Review of Entomology. 1979. Vol. 24. P. 185–208.
- López J. A., González M. C., Morales A. Nanostructures in Gyrinidae Beetle Eyes: Adaptations for Vision in Dual Environments // Journal of Experimental Biology. 2014. Vol. 217, № 12. P. 2125–2133. DOI: https://doi.org/10.1242/jeb.101345
- Nguyen L.-T., Schmidt H. A., von Haeseler A., Minh B. Q. IQ-TREE: A Fast and Effective Stochastic Algorithm for Estimating Maximum-Likelihood Phylogenies // Molecular Biology and Evolution. 2015. Vol. 32, № 1. P. 268–274. DOI: https://doi.org/10.1093/molbev/msu300
- Guignard Q. The Evolution of Insect Visual Opsin Genes with Specific Consideration of the Influence of Ocelli and Life History Traits. 2022.
- Katoh K., Toh H. Recent Developments in the MAFFT Multiple Sequence Alignment Program // Briefings in Bioinformatics. 2008. Vol. 9, № 4. P. 286–298. DOI: https://doi.org/10.1093/bib/bbn013
- Edgar R. C. MUSCLE: Multiple Sequence Alignment with High Accuracy and High Throughput // Nucleic Acids Research. 2004. Vol. 32, № 5. P. 1792–1797. DOI: https://doi.org/10.1093/nar/gkh340
- Smith M. R. Information Theoretic Generalized Robinson–Foulds Metrics for Comparing Phylogenetic Trees // Bioinformatics. 2020. Vol. 36, № 20. P. 5007–5013. DOI: https://doi.org/10.1093/bioinformatics/btaa614